後発薬22成分・441品目薬、すべてが規格をクリア―14年度の品質検査
2015.3.27.(金)
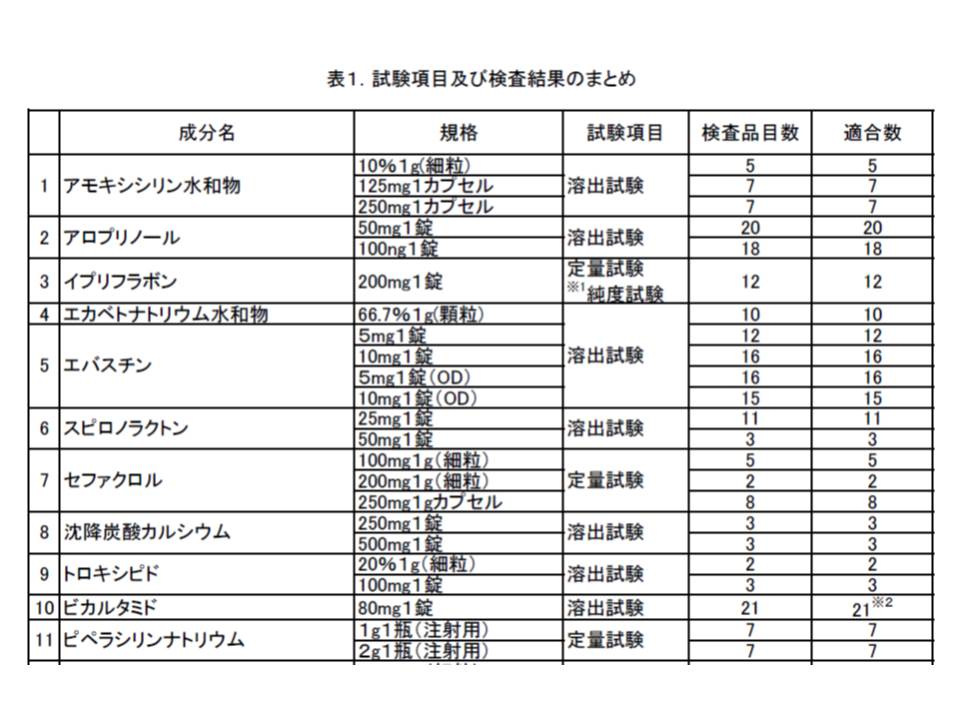
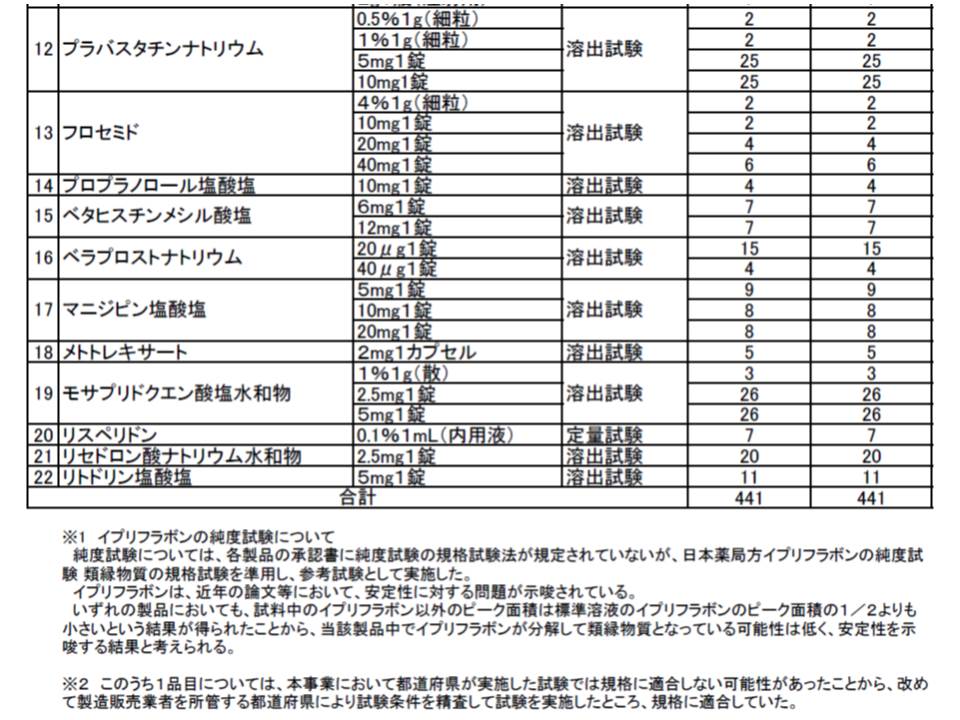
厚生労働省が27日に発表した、2014年度の「後発医薬品品質確保対策事業」検査結果によりますと、対象となった22成分・441品目のすべてが承認書に定められた規格に適合していることが分かりました。
前年度の検査では、1品目の規格不適合品が見つかっていました。
溶出試験、定量試験など、検査対象の全後発薬がクリア
医療費適正化の一環として後発薬の使用促進が求められていますが、実際にはなかなか目標通りには進んでいません。背景には、一部の医療関係者や患者の間に、後発薬に対する不信感があるとの調査結果も出ています。
このため厚労省は後発薬への信頼を確保するために「後発医薬品品質確保対策事業」を毎年度実施し、その結果を公表しています。具体的には、抗菌薬の「アモキシシリン水和物」や通風治療薬の「アロプリノール」など22成分・441品目の後発薬について、溶出試験や定量試験などの品質検査が行われました。
溶出試験は「決められた時間内に、決められた量の有効成分が溶け出すか」を調べるもので、今回は16成分・364品目を対象に実施されました。その結果、すべての後発薬が規格を満たしていることが分かりました。16成分・364品目を対象に実施した前年度の調査では、1品目で規格不適合が判明しています。
なお、前立腺がん治療剤のビカルタミド錠80ミリグラム「アメル」(共和薬品)について規格不適合の可能性がありましたが、試験器具の違いによるものと判明しています。
このほか、6成分・77品目について▽定量試験(有効成分が定められた分量含まれているか)▽確認試験(有効成分が実際に含まれているか)▽純度試験(混ざりものがどの程度含まれているか)―が実施されました。その結果、やはりすべてが規格に適合していることが判明しています。