来年4月の「患者申出療養」施行に向け、9月までに運用の詳細を詰める―中医協総会
2015.7.8.(水)
2016年4月から「患者申出療養」制度がスタートします。厚生労働省は、現場の準備などを考慮して今年10月には関係省令などを整備する予定を立てており、制度の運用面などを中央社会保険医療協議会の総会で詰める考えです。
8日に開かれた中医協総会では、▽インフォームド・コンセントの内容や手続き▽技術の有効性や安全性を審査する会議の進め方―などについて厚労省から論点が示され、本格的な議論が始まりました。今年9月には中医協の意見がまとめられる見込みです。
患者申出療養は、安倍首相が創設を決定した新たな保険外併用療養制度です。「困難な病気と闘う患者からの申し出」を起点とする新たな仕組みで、患者が最先端の医療技術などを希望した場合に、安全性・有効性等を確認したうえで、新規の技術については申請から6週間、前例のある技術については申請から2週間で「保険外の診療と保険診療との併用を認める」かどうかの結論を出します。
今般の医療保険制度改革で法的な枠組みが整い(改正健康保険法第63第2項第4号ほか)、来年4月から施行されます。
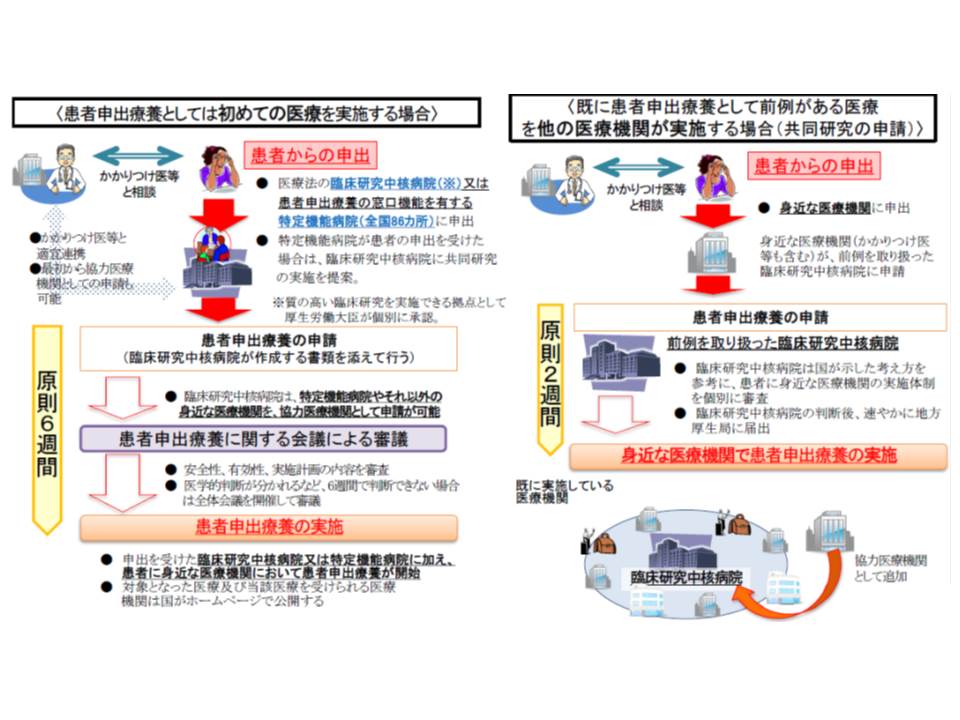
まず、患者申出療養の流れを確認すると、新規の技術については次のようになっています。
(1)患者がかかりつけ医などと相談し、保険外の最先端医療技術を保険診療と併用することを希望した場合、臨床研究中核病院(医療法第4条の3)などに申し出る
↓
(2)臨床研究中核病院などから示される「有効性や安全性に関する資料」とともに、患者が国に患者申出療養の申請を行う
↓
(3)国に設置される「患者申出療養に関する会議」で有効性や安全性、患者がリスクを理解しているかなどを審議する(原則6週間)
↓
(4)申請が認められた場合、その医療技術が当該臨床研究中核病院などで実施される
また患者申出療養として前例のある技術については、その前例を取り扱った臨床研究中核病院が「患者に身近な医療機関で実施できるかどうか」を審査し(原則2週間)、その上で当該「身近な医療機関」での実施が可能となるケースも出てきます。
それぞれのプロセスで重要な論点があり、(1)では「製薬企業などから誘導されて申し出を行うことがないようにする」ことが求められます。厚労省は、▽患者の署名入りの申請書▽患者と臨床研究中核病院の面談記録▽インフォームド・コンセントの書類―などを申請時に添付することを求めてはどうかと提案しました。
また、臨床研究中核病院などでは、患者からの「新規技術」に関する相談に対応する体制を敷いておく必要があります。厚労省は、▽相談窓口の設置▽マニュアルの整備や研修の実施▽情報共有の体制整備▽国へ報告する仕組み―などを例示しました。この点、万代恭嗣委員(日本病院会常任理事)は「相談窓口がいくつもあると患者に分かりにくい。専門かつ総合的な1つの窓口を整備する必要があるのではないか」と要望しています。
(3)の「患者申出療養に関する会議」は、医療技術の有効性や安全性などを審査するので、先進医療会議や先進医療技術審査部会に倣って設置される可能性が高そうです。
ただし、迅速な審査(新規で6週間、前例があるものは2週間)を行う必要があり、持ち回り開催の頻度が高くなることが予想されます。
また、審議内容は「医療技術の有効性・安全性」はもちろんのこと、(1)で見たように「患者が理解・納得して申し出たかどうか」も議論することになります。
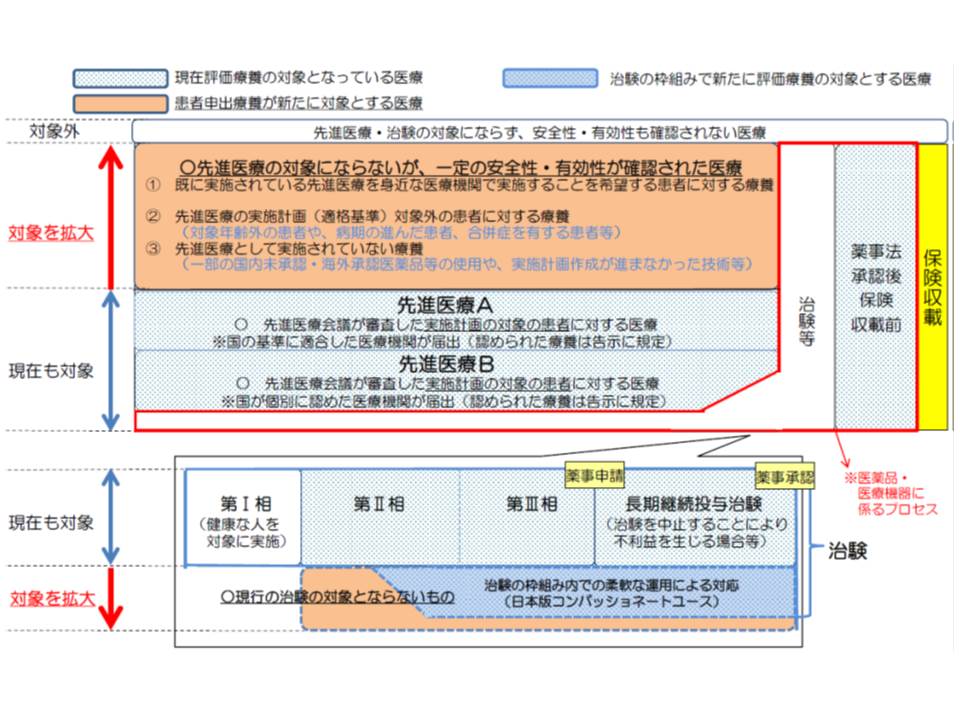
ところで、患者申出療養は「個別患者からの申し出」を起点としますが、最終的にはその医療技術を保険収載し、広く国民一般に利益をもたらすことを目指しており、保険収載目指さないものは患者申出療養の対象となりません。
そのため「人を対象とする医学系研究に関する倫理指針」に基づく「臨床研究」として実施されることが原則となります。個別の申し出を1つ1つ「有効か、安全化か」と審査するわけではなく、「個別患者の申し出を契機として、その医療技術を保険収載するに相応しい臨床研修計画が適切(有効かつ安全)に作成されているか」といった視点で審査されるイメージです。
臨床研修計画には、対象となる患者の年齢や合併症の有無などが当然盛り込まれるので、個別の申し出によっては、計画に合致せず、かつ計画の変更などでは対処し切れないケースが出てくると想定されます。例えば、A疾病に対して適応外薬αを用いるに当たり「対象患者は15-60歳、合併症なし」といった計画が策定されたとして、70歳で合併症のある患者がαの使用を患者申出療養として申請した場合などです。
ここで「15-70歳、合併症の有無を問わず」と計画を変更できればよいですが、これが難しく、かつ新たに「60歳以上、合併症あり」の計画を作成することが難しいケースも想定されます。
この場合には、例外的に「臨床研究計画を含まない実施計画を作成する」ことになり、審査も「持ち回り」ではなく、個別に「患者申出療養に関する会議」(全体会議)を開くことが必要となるでしょう。
この点について中川俊男委員(日本医師会副会長)や花井十伍委員(日本労働組合総連合会「患者本位の医療を確立する連絡会」委員)らの間で見解やイメージの相違があったため、厚労省保険局医療課の佐々木健企画官は「次回以降、整理した資料を提示する」と述べています。
また、保険収載を目指すものゆえ、取り組みが不十分な医療機関に対しては▽追加報告の要請▽患者申出療養からの除外―などを行う考えも厚労省から示されています。
【関連記事】
16年度から、紹介状なしの大病院受診に定額負担を導入―医療保険改革案
大病院受診、紹介状なしの定額負担など16年度から-医療保険部会で改革案まとまる