患者申出療養の提案受けた臨床研究中核病院、「人道的見地からの治験」の有無をまず確認―中医協総会
2015.8.27.(木)
患者申出療養は「臨床研究」として実施し、最終的には当該医療技術の保険収載を目指す―。このような考え方が、26日に開かれた中央社会保険医療協議会の総会で確認されました。
来年(2016年)4月からの患者申出療養の稼働に向け、厚生労働省は9月中に制度の詳細を詰める考えです。早ければ10月にも関連省令や告示の公布、通知の発出などが行われる見込です。
患者申出療養は、評価療養(先進医療など)や選定療養(個室など)に次ぐ、新たな保険外併用療養制度です。「困難な病気と闘う患者からの申し出」を受け、安全性・有効性などを確認したうえで、新規の技術については申請から6週間、前例のある技術については申請から2週間で「保険外の診療と保険診療との併用を認めるか否か」の結論を出します。
改正医療保険法に規定されており16年4月からスタートします。このため、中医協では制度の詳細を固める議論を7月8日から行っており(関連記事はこちら)、26日にはより具体的な検討が行われました。
新規に行われる(患者申出療養として前例のない)場合には、次のような流れとなります。
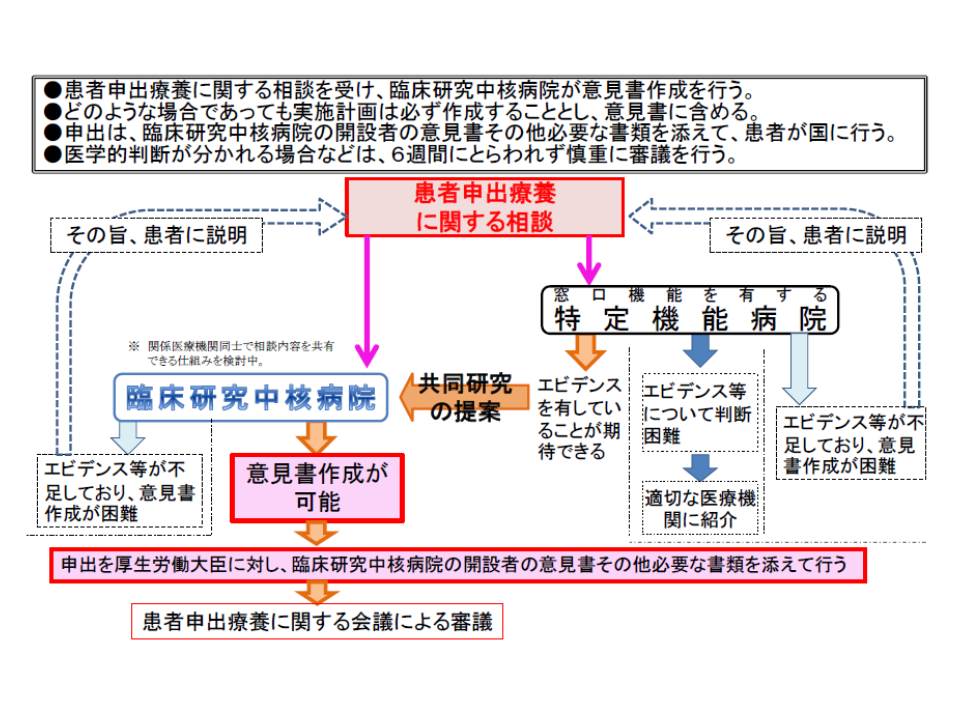
(1)患者がかかりつけ医などと相談し、「保険外の最先端医療技術」と「保険診療」との併用を希望した場合、臨床研究中核病院(医療法第4条の3)などに申し出る
↓
(2)臨床研究中核病院などから示される「有効性や安全性に関する資料」とともに、患者が国に患者申出療養の申請を行う
↓
(3)国に設置される「患者申出療養に関する会議」で有効性や安全性、患者がリスクを理解しているかなどを審議する(原則6週間)
↓
(4)申請が認められた場合、その医療技術が当該臨床研究中核病院などで実施される
厚労省保険局医療課の佐々木健企画官は、「患者申出療養は原則『臨床研究』として実施される」ことを明確にしました。当該医療技術の「迅速な保険収載」を目指すためです。したがって、(2)の申請にあたり、臨床研究中核病院などが臨床研究の実施計画を「人を対象とする医学系研究に関する倫理指針」に基づいて作成しなければなりません。
実施計画には、▽実施届出書(仮称)▽臨床研究計画書▽患者説明同意文書▽医療技術の概要図▽薬事承認または保険収載までのロードマップ―を盛り込む必要があります。
また「実施計画の対象外の患者」から申し出があった場合には、▽実施計画の変更▽新たな実施計画の作成―を行うことになりますが、厚労省は「臨床研究形式での実施が難しい場合には、臨床研究計画を含まない実施計画を作成することになる」との考えを示しています。
患者申出療養の対象となる医療として、厚労省は下図の5パターンを想定しています。
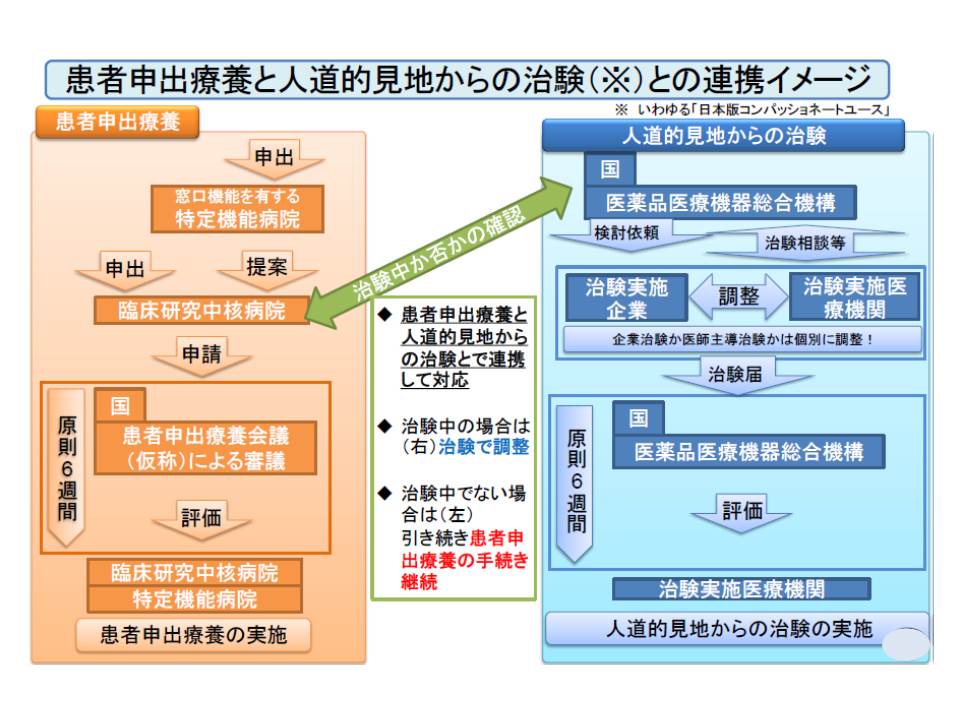
ここで気になるのが、例えば未承認医薬品を用いた医療技術と保険診療との併用を患者が希望した場合(上図の3)、「患者申出療養」によるべきなのか、それとも「治験」によるべきなのかという点です。
これについて厚労省は、患者申出療養の実施希望を受けた臨床研究中核病院に対して、国やPMDA(医薬品医療機器総合機構)に「人道的見地からの治験」(日本版コンパッショネートユース)として実施されているかどうかを確認するよう求めています。
その結果「人道的見地からの治験」で当該医療技術が実施されていればそこで対応し、実施されていなければ「患者申出療養」としての審査を行うことになります。
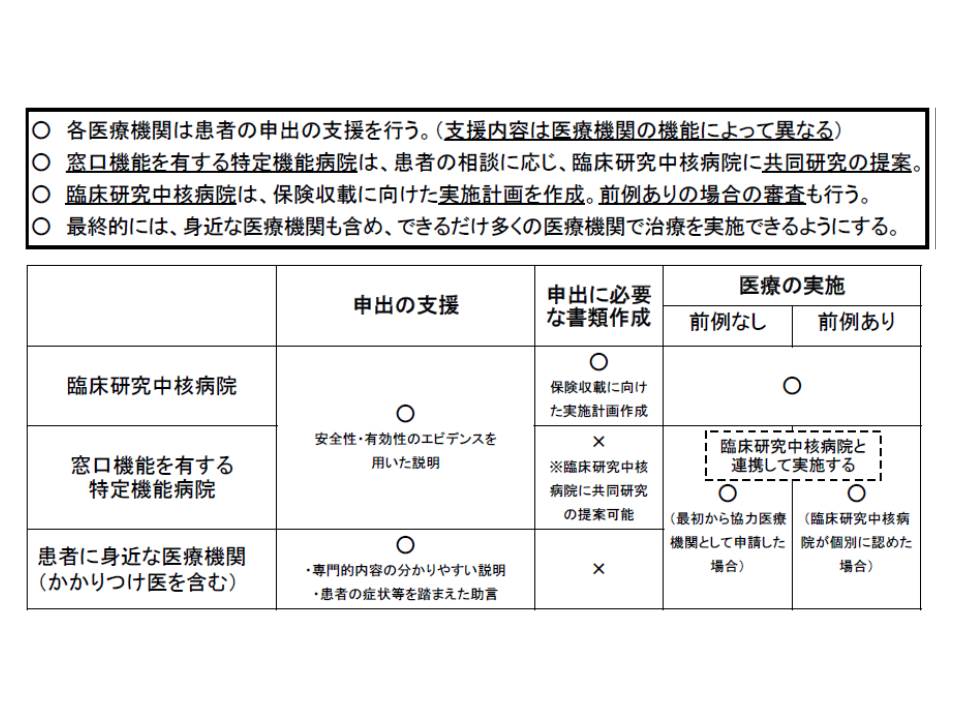
患者申出療養として前例のある医療技術を、「別の身近な医療機関などで行うことを希望する場合」や「実施計画対象外の患者を加える場合」などには、先ほどの「新規に行われる場合」とは異なり、国ではなく、臨床研究中核病院に「その身近な医療機関が、当該医療技術を実施できるか否か』などの判断を求めることになります。厚労省は、下図のように法律上の位置づけや医療機関の役割分担を整理しました。
ここでは臨床研究中核病院が「身近な医療機関の体制」などを判断するため、一定の判断基準を事前に準備しておくことが必要となります。佐々木企画官は「(判断に当たっての)指針のようなもの」を整備する考えを述べており、例えば「臨床研究である患者申出療養を行うための最低基準」(一般的基準)や「個別技術を実施するための基準」が整理される見込みです。
このように患者申出療養の枠組みや運用方法がかなり明確になってきましたが、起点となる「患者」にとっては複雑な仕組みです。
支払側の花井圭子委員(日本労働組合総連合会総合政策局長)は、「医療機関に相談する費用は患者負担なのか、健康保険から給付されるのかなどが分かりにくい」と指摘。佐々木企画官は「整理して示す」ことを約束しています。
また同じく支払側の花井十伍委員(日本労働組合総連合会「患者本位の医療を確立する連絡会」委員)は、「これまで詰めてきた内容などについて患者側の意見を聞いてはどうか」と提案しました。厚労省保険局医療課の宮嵜雅則課長はこの提案を「前向きに検討する」と述べて受け入れており、近く、中医協で患者団体などからのヒアリングが行われる見込みです。
【関連記事】