後発品の薬価、16年度改定で更なる引き下げ、詳細は薬価調査待ち―中医協・薬価専門部会
2015.10.29.(木)
2016年度の次期薬価改定で、後発医薬品の価格引き下げにつながるようなルール(薬価算定基準)見直しを行ってどうか―。こういった方向が、28日に開かれた中央社会保険医療協議会の薬価専門部会でおおむね固まりました。
後発品の薬価は、現在、次のようなルールに基づいて設定されます。
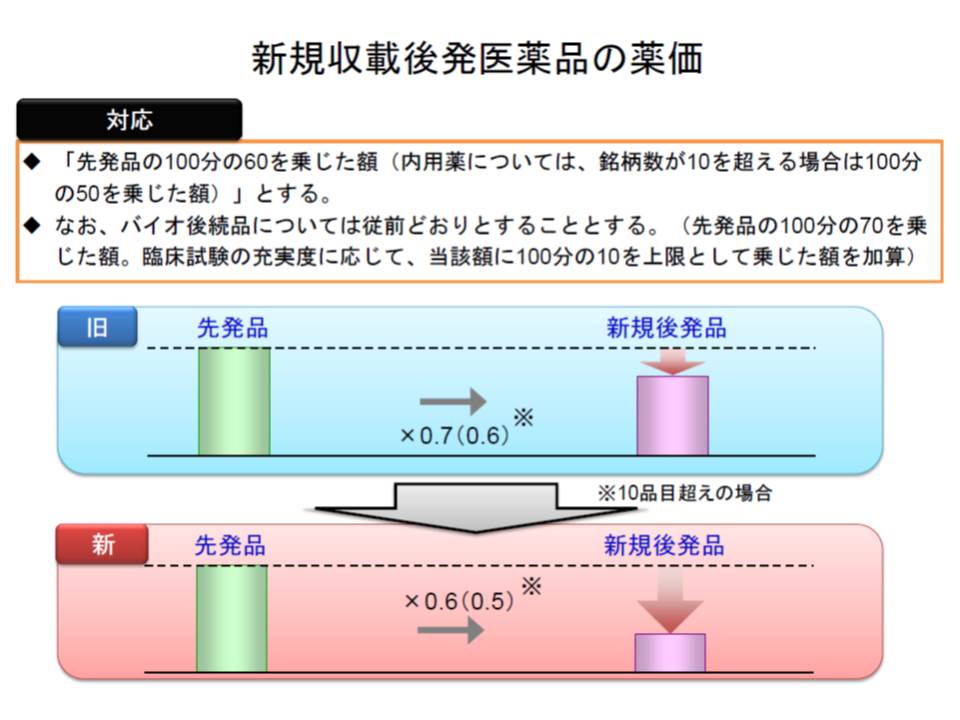
(1)新規に収載する後発品の薬価は、先発品の6割とする
(2)新規に収載される後発品が内用薬で、銘柄数が10以上の場合には、先発品の5割とする
(3)新規に収載されるバイオ後続品(バイオシミラー)の薬価は、先発品の7割とする
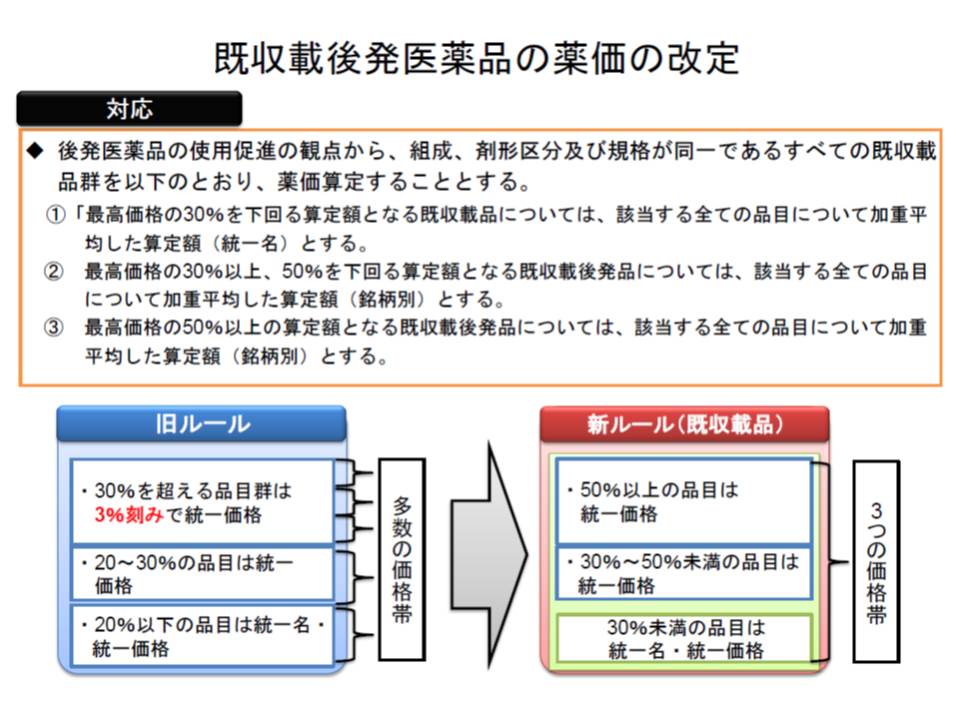
(4)既収載の後発品については、最高価格からの乖離に着目して3つの価格帯に分け、それぞれの区分で価格を統一する
薬価専門部会では、このルールを次期改定に向けてどう見直していくかを議論していきます。
まず(1)については、従前「先発品の7割」とされていましたが、前回改定では「薬価と実勢価格との乖離が大きい(19.2%の乖離)」ことから、6割に引き下げられました。
次期改定で、更に引き下げられるかどうかは、12月上旬に公表される予定の薬価調査結果を待つ必要があります。
この点について加茂谷佳明専門委員(塩野義製薬株式会社常務執行役員)は「14年度の前回改定では、内用薬で19.5%、注射薬で10%、外用薬で9.8%の引き下げが行われた。乖離率については慎重に吟味する必要がある」と述べ、後発品全体の価格を●%引き下げるという大雑把な手法に懸念を示しています。
また(2)の多数の銘柄が存在する場合、現行ルールを踏襲すると、「(1)の基準値-10%」となりそうですが、この点については、中医協の支払側・診療側双方の委員から厳しい意見が出されています。
支払側の白川修二委員(健康保険組合連合会副会長)は「多数銘柄の場合の特例について、後発品メーカーの市場参入制限を強める方向で見直してはどうか」と提案。
診療側の中川俊男委員(日本医師会副会長)も白川委員と同じく「後発品メーカーの再編・統合が進むような仕組みが考えられないか」と指摘し、「現在、10銘柄以上の場合には一律で『先発品の5割』だが、20銘柄以上であれば『先発品の4割』、30銘柄以上であれば『先発品の3割』といった仕組みを検討してもよい」と提案しています。
後にも述べるように、中医協では「同一成分・同一規格の後発品が多すぎ、価格も大きくばらついている。これが医療関係者や患者から後発品が今一つ信頼されない要因になっているのではないか」との指摘がかねてからあります。今回も集約化に向けた、いわばペナルティを強化したいという思いが、中医協委員には強いことが伺えます。
(4)の価格帯による薬価の集約も、(2)で見たように「あまりに多すぎる後発品銘柄を整理したい」という考えの現れと言えます。
現在は「最高価格(つまり先発品)」に着目して、次の3つの区分が設定されています。
▽最高価格の30%未満の算定額となる既収載品は、該当品目すべての加重平均に薬価を統一し、名称も統一する
▽最高価格の30%以上50%未満の算定額となる既収載品は、該当品目すべての加重平均に薬価を統一する
▽最高価格の50%以上の算定額となる既収載品は、該当品目すべての加重平均に薬価を統一する
このルールは14年度の前回改定で導入されましたが、これにより価格のばらつきは大幅に減少しました。
16年度の次期改定で、3価格帯を継続するのか、さらなる集約を図ったいくのかが気になりますが、診療側・支払側の双方ともに「集約の推進」を要望しています。
診療側の松本純一委員(日本医師会常任理事)は「薬局の多くは1価格帯を望んでいる。3価格帯から1価格帯に集約すべき」と指摘。
また、支払側の白川委員は「支払側はかねてから1価格帯を主張してきた」とした上で、「薬価調査の結果を見て、1価格帯にすべきか、2価格帯にとどめるのか判断したい」との考えを表明しました。
この点について製薬メーカー代表である加茂谷専門委員は、「価格帯の集約は進めるべき」としたものの、「現在は集約化の過渡期にある。当面は、上限の外れ値は別の価格帯とすべきではないか」と述べ、3価格帯の維持を求めています。
ところで、価格帯を設定する際の基準値について、現在は「最高価格(先発品の価格)」が用いられていますが、後発品メーカーからは「後発品の市場実勢価格に着目するように変更してほしい」との要望が出ています(関連記事はこちら)。
この要望に対して白川委員は、「先発品価格との乖離に着目することも重要である」と述べ、現行ルールを維持すべきとの考えを示しました。
なお、28日の薬価専門部会では、「複数の単剤の組み合わせを比較薬とした場合の薬価算定」ルールを次のように改めることも了承しました。16年度からの新薬価算定基準に盛り込まれる見込みです。
▽「臨床上併用されない単剤を組み合わせ」て比較薬とし、配合剤の薬価を算定する場合は、それぞれの単剤の1日薬価の合計額を、当該配合剤の1日薬価の上限とする(抗HIV薬を除く)。
▽この場合、投与期間が既存治療よりも短くなる新薬について、必要に応じてその有用性を補正加算で考慮する
これは8月26日に保険収載された慢性C型肝炎治療薬の「ハーボニー配合錠」の薬価について、現行ルールに不都合があったことを受け、見直しとなるものです(関連記事はこちら)。
【関連記事】
後発品の初収載時の薬価、「先発品の60%」維持をジェネリック製薬協が要望―中医協・薬価部会
先駆導入加算、「先駆け審査指定制度」の要件に見直しへ―中医協