医療上必要な基礎的医薬品、16年度から「薬価を維持する仕組み」を導入―中医協・薬価専門部会
2015.11.12.(木)
医療現場で欠かせない基礎的な医薬品の製造・販売を継続するために、試行的に「薬価を維持する」仕組みを2016年度の薬価制度改革で導入してはどうか―。こうした方向が、11日に開かれた中央社会保険医療協議会の薬価専門部会で固まりました。
薬価は2年に一度、市場実勢価格に基づいた見直し(原則、引き下げ)が行われるので、保険収載されてから時間が経つほど薬価は低くなります。このため製品によっては、価格が低下し「採算割れ」となるものもあると言います。
厚労省は、こうした医薬品の価格を下支えするために「最低薬価(それ以上は価格を引き下げないという基準価格が剤形ごとに設定されている)」「不採算品再算定(一定の基準を満たした場合、薬価を引き上げる)」というルールを設けていますが、製薬メーカーは「より安定した価格下支えルールを設けてほしい」と強く要望していました。
厚労省は、この要望を踏まえて次のような新ルールを設けることを提案しています。
▽類似の改定を受けて「市場実勢価格と薬価が乖離していない」医薬品で、「古くから医療の基盤となっている治療領域の医薬品」や、「過去に不採算品再算定を受けたことのある医薬品」を対象に、薬価を維持する仕組みを試行的に導入する
▽ただし、「一般的なガイドラインにも記載されていないもの」や「特定の医療機関のみで使用されているもの」など、汎用性のない医薬品などは除く
厚労省は、この仕組みを「不採算品再算定の対象や、最低薬価になる」前のネットと位置付けています。
また具体的な対象品目については、薬価算定組織で該当性を確認した上で、中医協で決定することも提案されました。
この提案について中医協委員からは特段の反論は出ておらず、2016年度の次期改定での試行導入が固まっています。ただし、支払側の幸野庄司委員(健康保険組合連合会理事)は「基礎的医薬品や製薬メーカーを取り巻く状況が数年で変わるとは考えにくい。半永久的に価格を維持する仕組みとなってはいけない」と注文を付けています。
11日の薬価部会では、医薬品の市場拡大再算定も議題に上がりました。市場拡大再算定は「保険収載時の予測よりも大幅に市場が拡大した(爆発的に売れた)」医薬品について価格を引き下げる(再算定)仕組みです。
中医協では、再算定の対象となる基準に「年間売り上げが巨額」という視点を加えてはどうかという方向で議論が進められていますが、具体的な金額の設定には更に時間がかかりそうです。
ところで、この市場拡大再算定は、いわば「売れた製品について、価格を引き下げる」もので、製薬メーカーからは「優れた製品を開発するインセンティブを阻害する」という強い批判が出ています。
この日も加茂谷谷佳明専門委員(塩野義製薬株式会社常務執行役員)から「イノベーションの否定につながる仕組みには反対である。そもそも再算定は、保険収載時の条件が変更になった場合、例えば『効能効果の追加』などに行われるべき仕組みである」との批判が出されました。
この指摘について、診療側の松原謙二委員(日本医師会副会長)は一定の理解を示した上で、「今の医療用医薬品の市場は、医療保険制度があって成立するものである。利益が大きくなった場合の価格引き下げは『保険制度を維持するためのもの』と考えてほしい」と求めました。
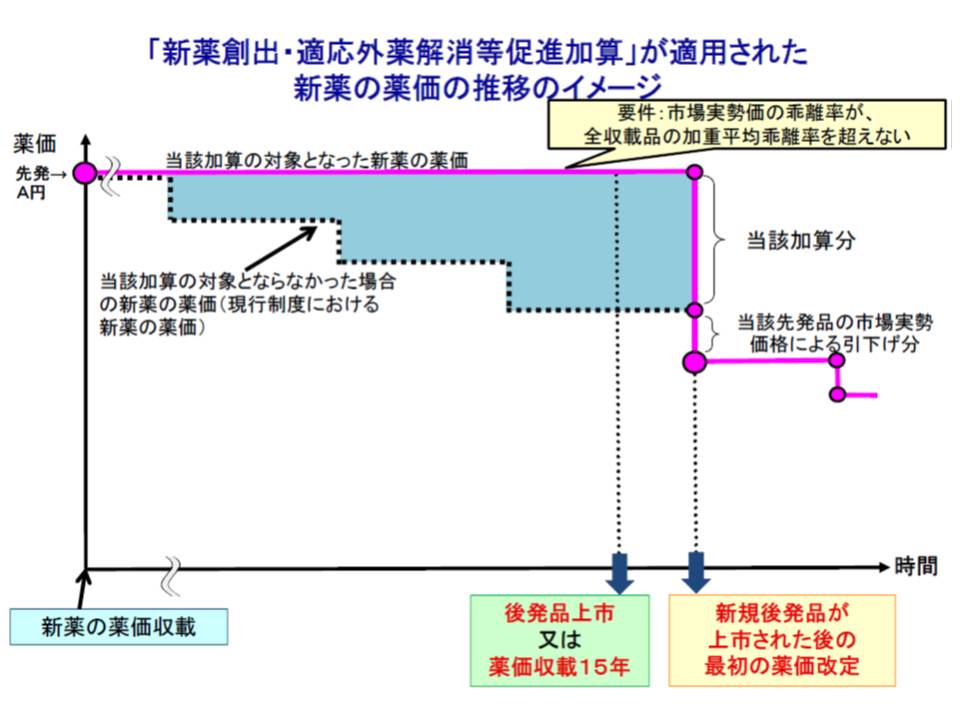
医療の質を高めるためには、優れた医薬品の開発も不可欠です。そこで現在は製薬メーカーにおける新薬開発を促進するために、次の要件を満たす医薬品の価格を下支え(改定前の80%を維持する)する新薬創出・適応外薬解消等促進加算(新薬創出等加算)が試行導入されています。
▽新薬として薬価収載された既収載品で、後発医薬品が薬価収載されていないもの(ただし薬価収載から15年を経過した後の最初の薬価改定を経ていないものに限る)
▽当該既収載品の市場実勢価格の薬価に対する乖離率が、全収載品の加重平均かい離率を超えないもの
▽再算定の対象でない
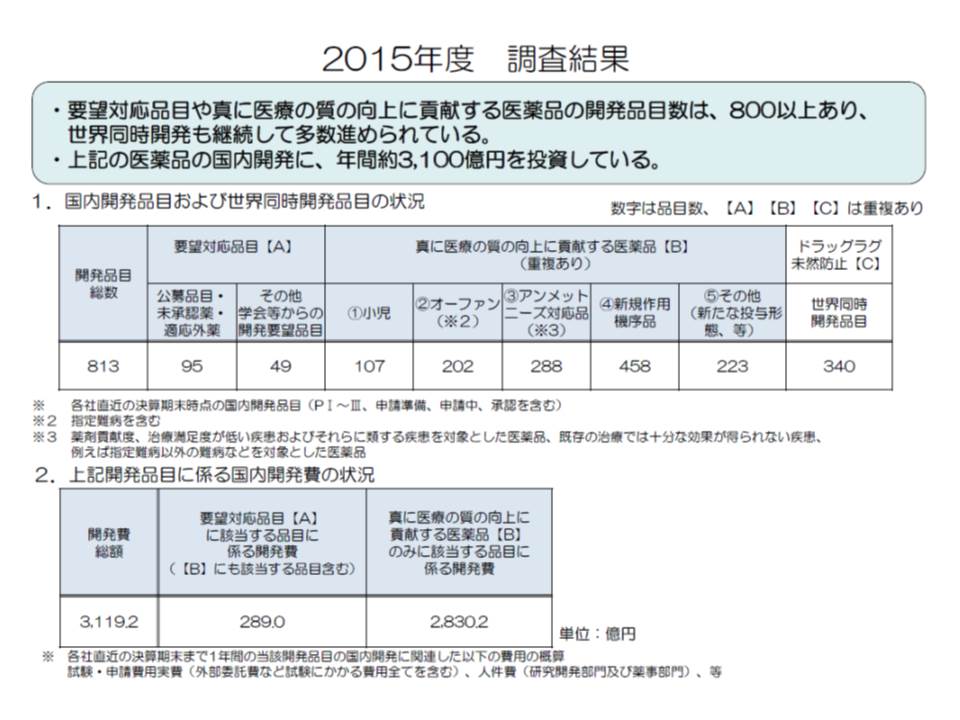
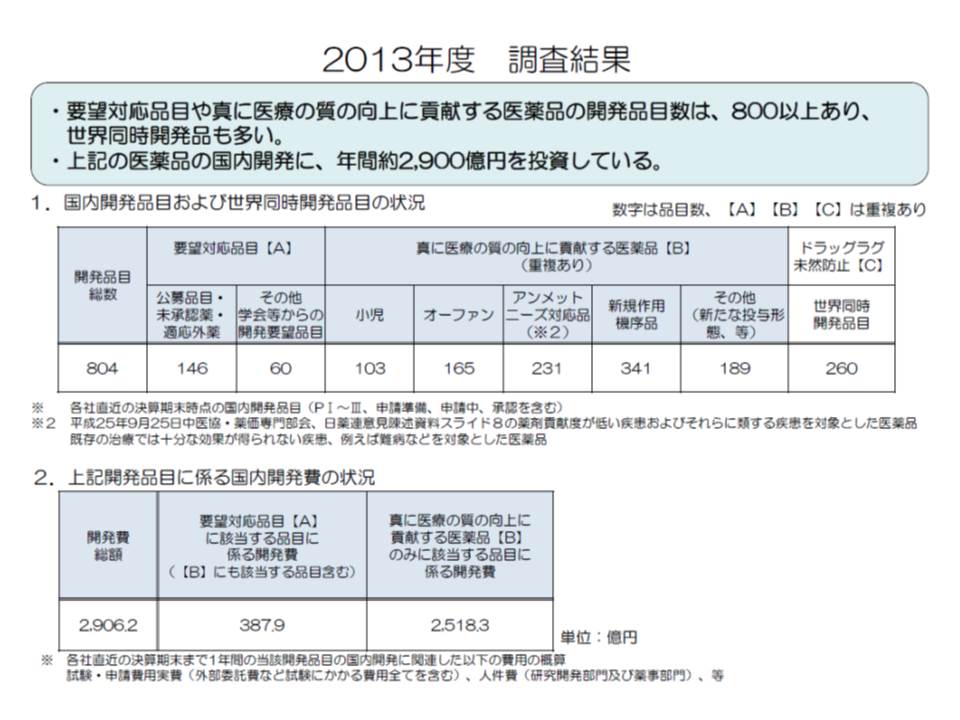
製薬メーカーサイドは「新薬の開発には原資が必要である」ことや「新薬創出等加算の試行導入によって、未承認や適応外薬の開発が進んでいる」ことなどを強調し、試行の継続を強く求めています。
中医協委員からは試行継続に明確に反対する意見は出ていませんが、支払側の幸野委員は「新薬創出等加算の効果を検証することが重要だが、効果は『製薬メーカーの投資額』で図るべきではない」と指摘。
これに対して厚労省保険局医療課の中井清人薬剤管理官は、個人的な感想と前置きをした上で、「定量評価はできないが創薬が進んでいる感触がある」とコメント。さらに「厚労省はドラッグラグの解消だけでなく、日本が世界に先駆けて優れた新薬を創出できるようになることが重要と考えている」と説明しています。
【関連記事】
長期収載品から後発品へのシフト促すZ2ルール、支払側は厳格化を要望―中医協・薬価専門部会
後発品の薬価、16年度改定で更なる引き下げ、詳細は薬価調査待ち―中医協・薬価専門部会
先駆導入加算、「先駆け審査指定制度」の要件に見直しへ―中医協