一般病院にも「高度な医療技術実施の際の安全管理体制」整備の努力義務を課す―社保審・医療部会
2016.2.19.(金)
高難度新規医療技術(その医療機関で事前に行ったことのない手術・手技で、人体への影響が大きいもの)を行うに当たって、特定機能病院に必要な体制の整備と導入プロセスの遵守を義務付けるが、一般の病院にも同様の努力義務を課す―。こういった方針が、18日に開かれた社会保障審議会の医療部会で了承されました。
厚生労働省は、関係省令の改正や必要な通知の発出などを近く行います。
お伝えしているとおり、東京女子医科大学病院と群馬大学附属病院で重大な医療事故が相次いで発生し、かつ病院管理者が事態を的確に把握していないことが判明しました。厚生労働省は、事態を重く見て、すべての特定機能病院に立ち入り検査を行ったところ、病院のガバナンスに問題点があることが判明しました(関連記事はこちらとこちら)。
そこで塩崎恭久厚生労働大臣は昨年(2015年)、厚労省幹部からなるタスクフォースを省内に組織、そこで「特定機能病院における医療安全対策強化」の方向性を検討。さらに、「特定機能病院及び地域医療支援病院のあり方に関する検討会」(以下、検討会)は1月28日に、この方向性を具体化した「承認要件見直し案」を取りまとめました(後述)。
見直し案の中には、「高度な医療技術を初めて実施する場合」あるいは「未承認の医薬品などを使用する場合」に次のような体制を敷くことも盛り込まれました。事前のリスク評価や事後の検証などが欠かせないためです。
【高難度新規医療技術への対応】
▽特定機能病院の管理者は、当該医療機関で事前に行ったことのない手術・手技(軽微な術式変更などを除く)であって、人体への影響が大きいもの(高難度新規医療技術)による医療を行う場合に、高難度医療技術の実施の適否を確認する部門を設置する。(新規)
▽特定機能病院の管理者は、別に厚生労働大臣が定める基準に従い、高難度新規医療技術による医療を行う場合に職員が遵守すべき事項および当該部門が確認すべき事項を定めた規程を作成する。(新規)
▽特定機能病院の管理者は、当該部門に、職員の当該規程に定められた事項の遵守状況を確認させる。(新規)
【未承認の医薬品などへの対応】
▽特定機能病院の管理者は、当該医療機関で事前に行ったことのない未承認の医薬品等による医療を行う場合に、実施の適否を確認する部門を設置し、そのリスクに応じて、必要な確認を行う。(新規)
▽特定機能病院の管理者は、別に厚生労働大臣が定める基準に従い、未承認の医薬品等による医療を行う場合に職員が遵守すべき事項及び当該部門が確認すべき事項を定めた規程を作成する。(新規)
▽特定機能病院の管理者は、当該部門に、職員の当該規程に定められた事項の遵守状況を確認させる。(新規)
こうした体制整備などは「特定機能病院の承認要件」となるので、逆に言えば、特定機能病院は体制整備義務を負うことになります。ただし適用は2017年4月からで、また既に特定機能病院の承認を受けている場合には、一定期間「新承認基準を満たしているとみなす」という経過措置も設けられます。
ところで、「高度な医療技術を初めて実施する」場面は特定機能病院に限りません。わが国には、特定機能病院ではない「高機能の一般病院」が数多く存在し、高度な医療技術の提供や未承認の医薬品などを用いた医療の提供が行われています。このため検討会では、「一般の病院でも、高度な医療技術を初めて提供する場合などには、特定機能病院と同様の体制整備などを求めるべきではないか」との指摘が出されました。
厚労省はこれを受け、「特定機能病院以外の病院では、特定機能病院に対する規定(上記)を参考に、同様の取り組みに努めること」という努力義務を課すことを提案。医療部会はこれを了承しました。
この点について厚労省医政局総務課の中村博治課長は、「すべての一般の病院に、特定機能病院と同じ体制を敷いてもらうことは無理だが、高度な医療技術を実施する病院では特定機能病院の規定を参考に体制を敷く努力をしてほしい」と説明しています。
ただし相澤孝夫委員(日本病院会副会長)は、「高度な医療の抑制につながらないように考える必要がある。例えば『高難度新規医療技術の実施の適否を確認する部門』は、医療の質が担保できるのであれば、院内ではなく外部に設置しても良いと考えられる」と指摘。これに対し中村総務課長は、「確認部門については、一般の病院では外部に設置したほうが客観的な判断ができるとも考えられる。運用面で配慮したい」と答弁し、関係通知などで相澤委員の指摘を踏まえた運用方法を記載する考えを示しました。
ところで、現在、すべての医療機関には(1)医療安全管理のための指針作成(2)医薬品業務手順書の作成―が義務付けられています(医療法施行規則第1条の11第1項および第2項)。
厚労省は医療の安全性をより高めるために、この指針と手順書の内容を充実する必要があると考え、(1)の指針と(2)の手順書の中に、次のような事項の記載するよう求めることにしています(新たに通知で規定)。
▽医療安全管理のための指針において、「学会から示される高難度新規医療技術の導入に当たっての『医療安全に関する基本的な考え方』を参考に実施する」ことを明記する
▽医薬品業務手順書において、「未承認の医薬品などの処方の妥当性について、学会ガイドラインなどの医学的知見を確認する」ことを明記する
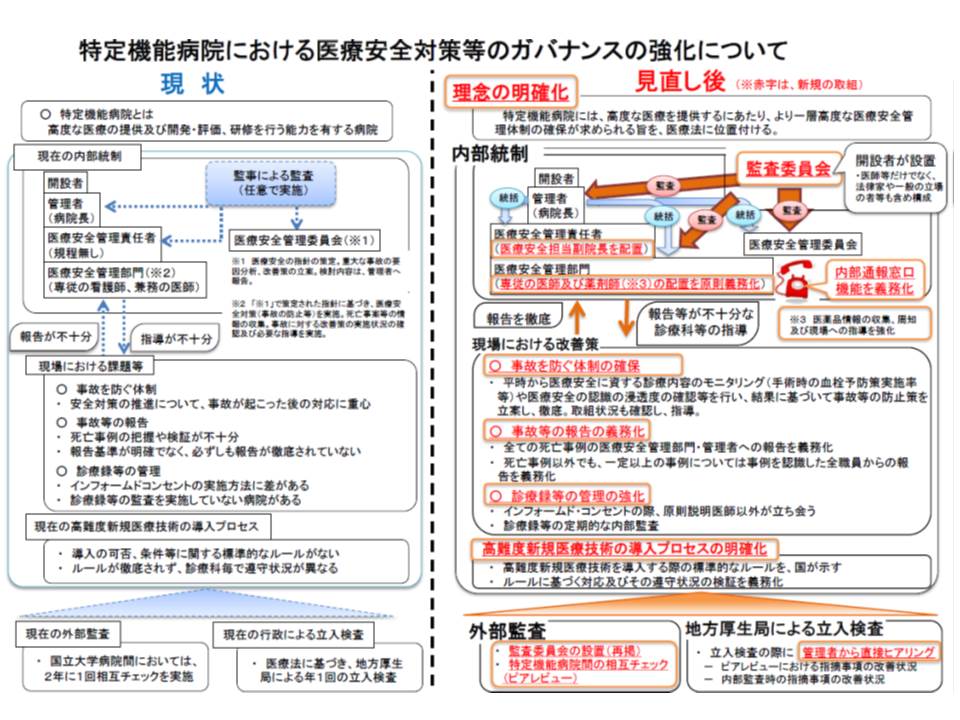
特定機能病院の承認要件見直し案も、18日の医療部会で了承されています。見直し内容をおさらいすると、次のような点がポイントと言えるでしょう。ただし体制整備などには一定期間が必要なため、経過措置も設けられています(関連記事はこちら)。
【内部統制の強化】
▽管理者(病院長)には「医療安全業務の経験」を必須化する
▽医療安全管理責任者(副院長が想定)の配置を必須化する。医療安全管理責任者は、「医療安全管理部門」「医療安全管理委員会」「医薬品安全管理責任者」「医療機器安全管理責任者」の業務を統括する
▽医療安全管理部門には、専従の「医師、薬剤師および看護師」の配置を求める
▽事故(予測可能な死亡事例なども含む)報告や、内部通報窓口の設置を義務化する
▽高難度新規医療技術の導入プロセスを明確化する
【外部監査】
▽過半数が外部委員(医療関係者だけでなく、法律家や一般国民も含める)で構成される監査委員会を設置する
▽特定機能病院間の相互チェック(ピラレビュー)を義務化する
▽地方厚生局による立入検査を充実する
ところで承認要件の見直しが目的なのではなく、最終目的は「医療安全の確保」です。この点について山崎學委員(日本精神科病院協会会長)からは「各種の委員会などを作成するだけで安全が確保できるのか」との心配の声が出されましたが、邉見公雄委員(全国自治体病院協議会会長)らは、「医療安全業務経験がなければ院長になれず、医療安全管理責任者には副院長が就くなど、医療安全業務がエリートコースになる。職員の意識も高まるので、実効性があると考えられる」との考えを示しています。
【関連記事】
特定機能病院に医療安全管理体制強化や外部監査委設置などの要件追加―厚労省
特定機能病院に、「監査委員会」設置や「医療安全担当の副院長」配置を義務付け―厚労省
特定機能病院への集中立入検査を6月から実施、目的は「実態把握」―厚生労働省
女子医大病院と群馬大病院の特定機能病院の承認取り消し決定、特定機能病院の承認要件見直しも検討―塩崎厚労相