特定機能病院や臨床研究中核病院、「医療安全管理部門の設置」などを承認要件に追加―厚労省
2016.6.17.(金)
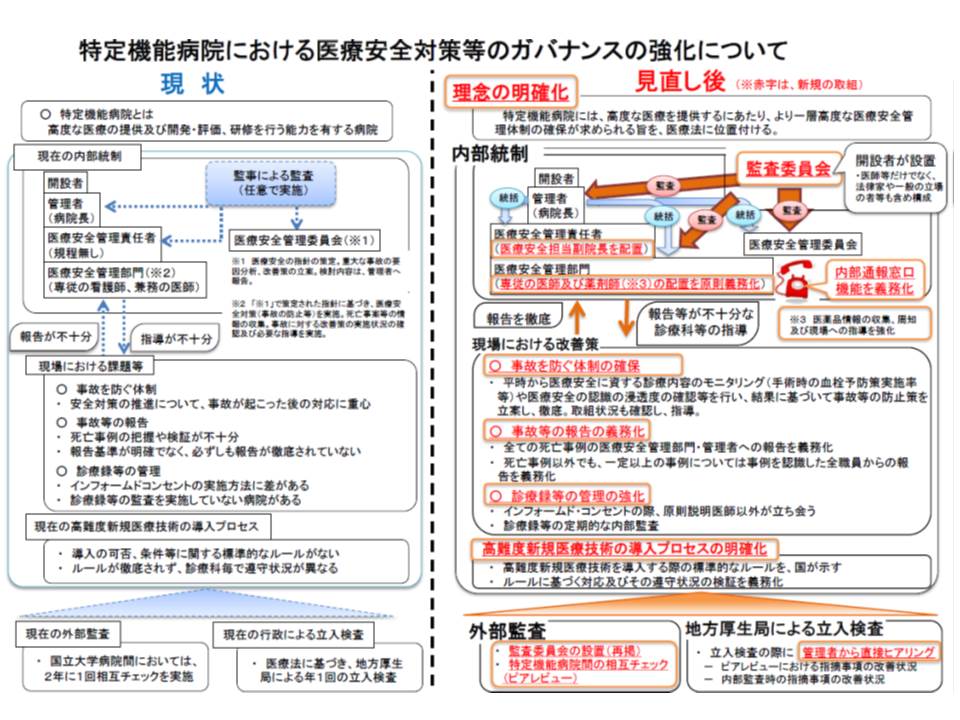
特定機能病院において「医療安全管理責任者」の配置や、過半数を外部委員とする「監査委員会」の設置を義務づける(承認要件とする)とともに、一般の病院においても「高難度新規医療技術を用いた医療を提供するにあたって、必要な措置をとる」努力義務を課す―。
厚生労働省は10日に、こうした内容を柱とする医療法施行規則の改正を行い、その内容を通知「医療法施行規則の一部を改正する症例の施行について」で都道府県知事らに周知しました。
目次
委員長と委員の過半数を「病院と利害関係のない者」とする監査委員会の設置も義務化
東京女子医科大学病院と群馬大学附属病院の2つの特定機能病院で重大な医療事故が発生し、そこでは病院のガバナンスに問題点があることが分かったことから、塩崎恭久厚生労働大臣は、特定機能病院の承認要件見直し案をまとめました(関連記事はこちらとこちら)。
さらに「特定機能病院及び地域医療支援病院のあり方に関する検討会」でも、塩崎案をベースに見直し要件をまとめ、今般、医療法施行規則(省令)の見直しが行われたものです。
特定機能病院の承認要件については、次のような見直しが行われました。
(1)医療安全管理責任者を配置する。責任者は、▽医療安全管理部門▽医療安全管理委員会▽医薬品安全管理責任者▽医療機器安全管理責任者―を統括する
(2)医療安全管理部門(専従の医師、薬剤師、看護師を配置)を設置する。ここでは、医療事故などが発生した場合に▽診療録などの確認▽患者・家族への説明▽発生原因の究明▽対応状況の確認▽従事者への必要な指導―などを実施する
(3)高難度新規医療技術・未承認医薬品を用いた医療提供の適否などを決定する部門を設置し、これらの医療提供を行う場合に遵守すべき事項などを定めた規定を作成する。
▼高難度新規医療技術とは、「当該病院で実施したことのない医療技術で、実施によって患者の死亡その他の重大な影響が想定されるもの」をさす
(4)監査委員会(3名以上で、委員長と委員の過半数は「病院と利害関係のない者」から選任)を設置する。委員の名簿と選定理由を厚生労働大臣に提出し、公表する
(5)入院患者が「死亡した場合」や「死亡はしていないものの、通常の経過では必要ない処置・治療が必要になった場合(特定機能病院の管理者が定める水準以上の事象に限る)」には、(2)の医療安全管理部門に事実と発生状況を報告する
(6)他の特定機能病院と連携し、年に1回以上、他の特定機能病院に職員を立ち入らせ、必要に応じて医療安全管理の改善に向けた技術的助言を行う(合わせて立ち入りを受け、助言を受ける)
また、特的機能病院の開設者に、「医療安全管理業務経験」などが求められるようになります。
あわせて臨床研究中核病院の承認要件についても、「医療安全管理部門(専従の医師、薬剤師、看護師を配置)の設置」や「医療事故などが生じた場合の医療安全管理部門の取り組み」などが盛り込まれています。
これらの見直しには経過措置も設けられていますが、できるだけ早期に体制を整える事が必要でしょう。
一般病院にも、高難度新規医療技術を実施する際には「必要な措置」を行う努力義務
一方、特定機能病院・臨床研究中核病院以外の「一般の病院」であっても、高難度新規医療技術を実施する場合には、特定機能病院に準じた「必要な措置を講じる」努力義務が課されます(関連記事は一般病院にも「高度な医療技術実施の際の安全管理体制」整備の努力義務を課す―社保審・医療部会)。
また、精神疾患を有する者が「身体疾患の治療」を行うために精神病床以外の病室(一般病床など)に入院できることなども、今般の医療法施行規則改正によって明確にされています。
高難度新規医療技術、各診療科と担当部門、評価委員会で実施の適否を判断
ところで、厚生労働省は同じく10日に、前記(3)の高難度新規医療技術の実施に関する基準も定めています。特定機能病院などでは、この基準に沿い、高難度新規医療技術を実施するに当たって遵守すべき事項などの規定を作成することになります(さらに10月に関係学会からガイドラインが示される見込み)。
基準では、(a)診療科(b)担当部門(c)高難度新規医療技術評価委員会―などに関する事項を明確にしています。ただし、現在承認されている特定機能病院においては、2017年4月以降に以下の規定が適用されます(そうでない場合には、2016年6月10日から適用)。
まず(a)の各診療科においては、その「長」が、▽高難度新規医療技術の既存技術に比べての優位性(合併症の重篤性や発生可能性などを含む)▽高難度新規医療技術を提供するために必要な設備・体制(ICUや麻酔科医師都の連携など)▽医師などの経験▽患者に対する説明と同意の取得方法―などを予め定めておくことが必要です。
また各診療科の「長」は、高難度新規医療技術を適用した全症例について、定期的に、かつ必要に応じて(患者が死亡した場合など)、担当部門に報告を行わなければいけません。
(b)の担当部門には、医療安全管理部門などを活用することも可能ですが、高難度新規医療技術を用いた医療の経験・知識をもつ医師・歯科医師を責任者として配置し、手術部門所属者を含めて構成することが必要です(専従でなくとも可)。
担当部門の「長」には、▽高難度新規医療技術評価委員会(適否などの意見を述べる)の設置▽評価委員会の意見を踏まえて実施の適否を決定▽規定の遵守状況の確認▽管理者への報告―などを行います。
(c)の評価委員会は、(i)高難度新規医療技術に関連する診療科の医師・歯科医師(ii)(i)と別診療科の医師・歯科医師(iii)医療安全管理部門の医師・歯科医師―を含めた3名以上で構成します。
評価委員会の「長」は、高難度新規医療技術の提供が「倫理的・科学的に妥当か」「寺院での提供が適切か」「科学的根拠が確立していない場合には、有効性や安全性が担保されているのか」などを審査し、担当部門長に実施の適否に関する意見を述べます。なお、特定機能病院以外の病院においては、「院外の委員会」(別の特定機能病院の評価委員会など)に審査を委託する事が可能です。
【関連記事】
特定機能病院に医療安全管理体制強化や外部監査委設置などの要件追加―厚労省
特定機能病院に、「監査委員会」設置や「医療安全担当の副院長」配置を義務付け―厚労省
特定機能病院への集中立入検査を6月から実施、目的は「実態把握」―厚生労働省
女子医大病院と群馬大病院の特定機能病院の承認取り消し決定、特定機能病院の承認要件見直しも検討―塩崎厚労相