費用対効果の良し悪しを判断する基準値、2016年度改定では定めず―費用対効果評価専門部会
2015.12.16.(水)
2016年度の次期診療報酬改定では、医薬品や医療機器などの価格について「費用対効果を評価する」仕組みが試行導入されますが、「費用対効果の良し悪しを判断する基準値」は次期改定では定めない―。こういった方針が、16日に開かれた中央社会保険医療協議会の費用対効果評価専門部会、続いで開かれた総会で了承されました。
費用対効果評価に基づく実際の価格調整は、2018年度の次々期改定以降に行われるため、16年度からの試行の中で事例を蓄積しながら、判断基準をどう考えるか、具体的な価格調整方法をどう設定するのかなどを探っていくことになります。
費用対効果評価の大枠をおさらいすると、次のように整理できます。
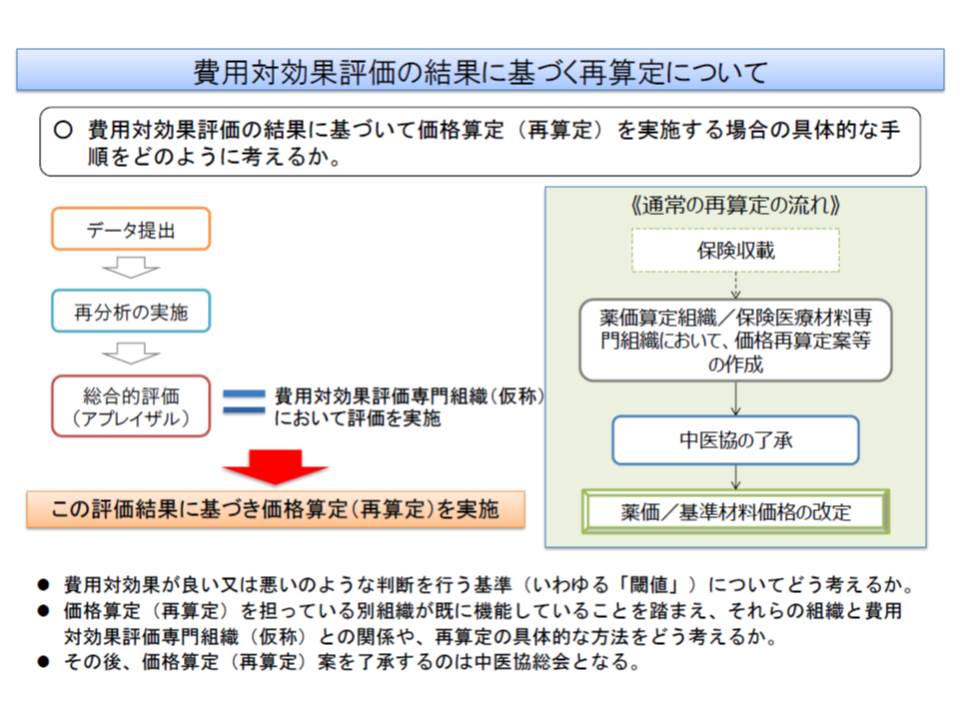
(1)製薬メーカー、医療機器メーカーが費用と効果に関するデータ、自社による費用対効果評価の分析結果を提出する
↓
(2)厚生労働省内に設置される専門体制(再分析グループ)が、中立的な立場から再分析を行う
↓
(3)新たに設置される費用対効果評価専門組織(仮称、中医協の下部組織)で、企業・再分析グループの分析結果について総合的評価(アプレイザル)を行う
↓
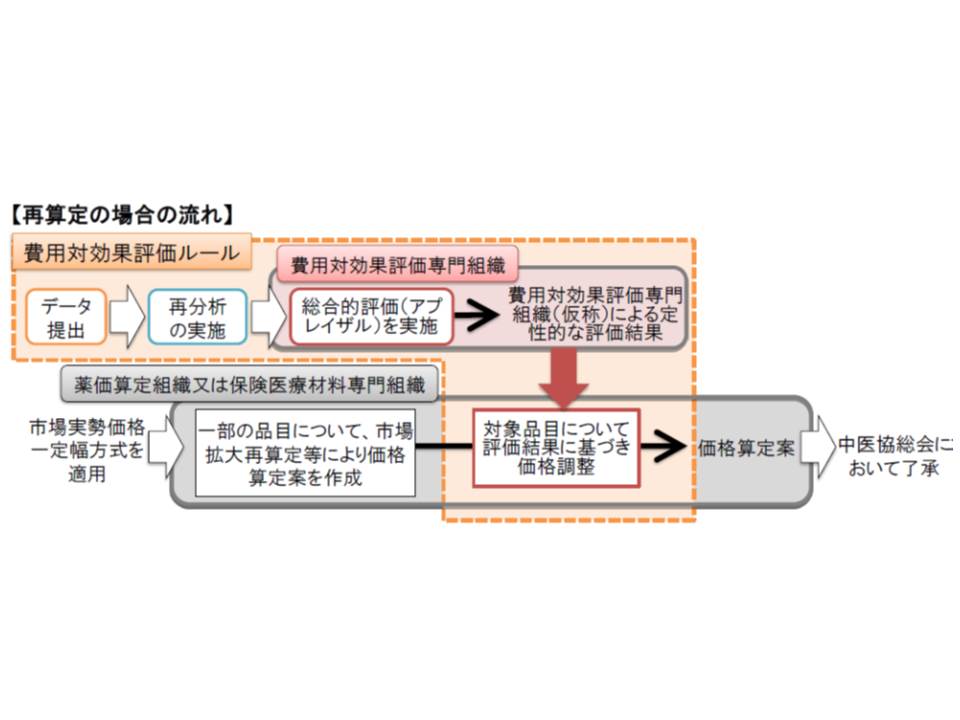
(4)費用対効果評価専門組織の評価結果をもとに、薬価算定組織と保険医療材料専門組織で価格調整を行う(再算定)
(1)のデータ提出が求められる医薬品・医療機器は、「売上高の高い」「保険収載後1-2回の改定を経て、市場で価格がこなれている」などの選定基準に基づいて指定されます。具体的な基準は年明け(2016年)の1月から検討され、2015年度内に設定されます。
(3)の総合的評価は、▽科学的な観点▽倫理的、社会的影響などに関する観点―の2つの側面から実施されます。
前者の「科学的な観点」とは、「分析が標準的な方法によるものか」「用いたデータが適切か」といった点からの検証を意味します。
後者の「倫理的、社会的影響など」については、例えば「小児が対象か」などが思い浮かびますが、具体的にどういった項目を考慮するかは、事例を蓄積しながら検討していくことになりました。
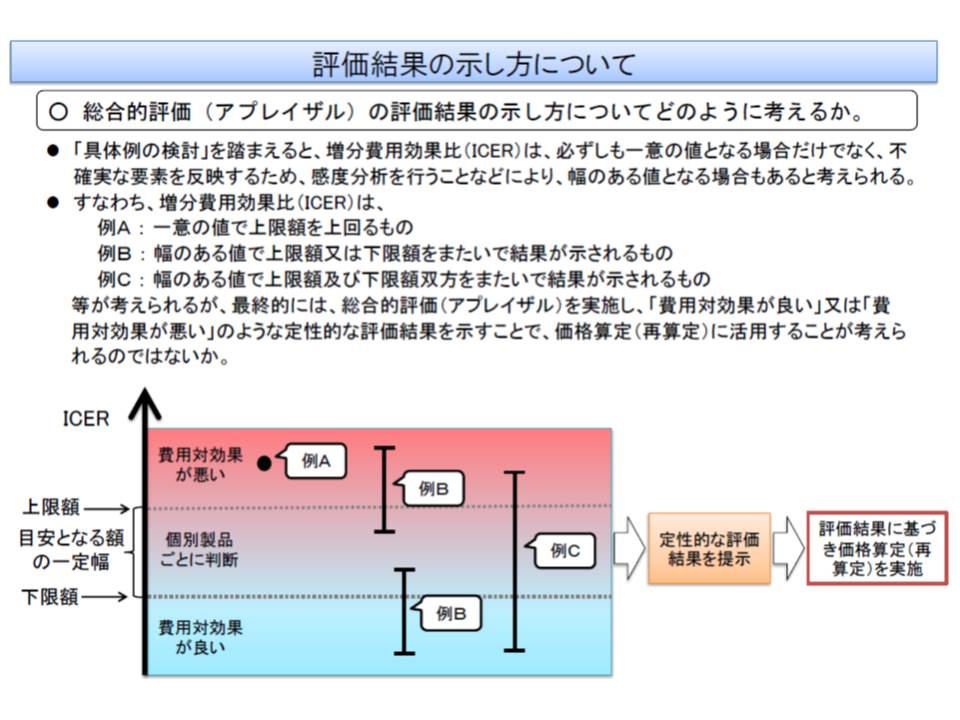
この総合的評価において、「当該製品の費用対効果が良いのか悪いのか」の判断を行います(最終決定は中医協)。ここで、「どのような基準で費用対効果の良し悪しを判断するのか」が気になります。
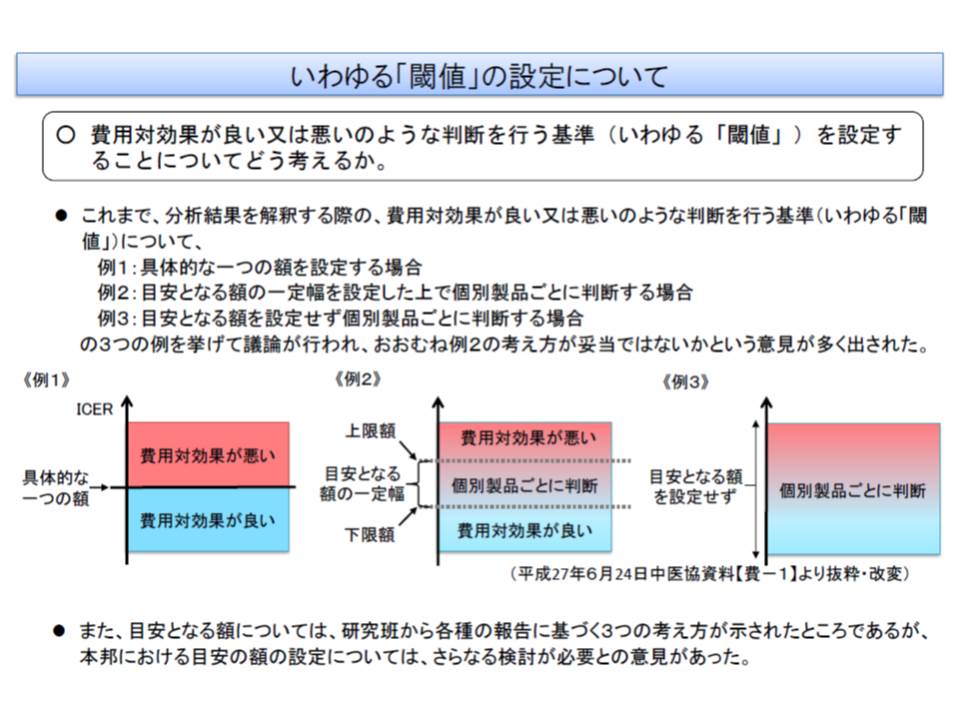
厚労省は11月20日の専門部会に「一定の幅を持たせた基準値(閾値)」を設定しては同かとの考えを示しました。例えば、最低値と最高値を定め、最高値より高ければ「費用対効果が良い」、最低値より低ければ「費用対効果が悪い」と判断でき、最高値と最低値の間にある場合には「個別製品ごとに判断する」という具合に活用するものです(関連記事はこちら)。
しかし委員の中には「基準値の設定は好ましくない」といった考えも強かったことから、16日には「基準値は、今回の試行導入においては定めない」と方針転換しています。
確かに基準値を設定するための基礎資料も十分ではなく、「いくら」と決めるのは時期尚早とも考えられます。今後、「わが国の国民が、ある病気の治療にどの程度の費用であれば支払えると考えるのか」(支払意思額)などの調査も行い、事例の蓄積状況も見ながら、皆が納得した基準値の設定を目指すことになるでしょう。
ちなみに費用対効果評価の先進国であるイギリスでは、増分費用効果比(ICER:費用の増加/効果の増加)を基に「2万―3万ポンド」という判断の基準値(閾値)を設けています。例えば新薬の価格が2万ポンドより低ければ「費用対効果が高く、公的保障の対象に推奨する」といった判断が下されます。
ところで費用対効果評価専門組織は、「費用対効果が良い」「悪い」という定性的判断しか下しません。
これを価格調整に反映させるのは、(4)で示したように「薬価専門組織」「保険医療材料専門組織」の業務になります(両組織では、ルールに則って薬価と材料価格を設定する)。
そのため、費用対効果評価の結果をどのように価格に反映させるのかというルールを決めておく必要があり、厚労省保険局医療課の眞鍋馨企画官は「2018年度の診療報酬改定時に併せて検討する」という考えを示しました。
ここで気になるのが、「費用対効果が極めて高い」ことが明らかになった場合、価格の引き下げは行われるのだろうか、という点です。厚労省保険局医療課の担当者はこの点について明確な考えを示していませんが、メーカー側は「価格引き上げルールの設定」も求めると考えられます。
前述のように費用対効果評価の結果を「価格調整」(再算定)に用いるのは、「既収載品」に限定されます。
それは、「新薬や新規医療機器についてデータの分析などを必須とし、それを価格算定に用いるとすれば、保険収載が遅くなってしまい。患者の優れた医薬品・医療機器へのアクセスを阻害してしまう」からです。
ただし、眞鍋企画官は新薬・新規医療機器の中でも「ピーク時の売上高が高い原価計算方式の品目」などについては、費用と効果のデータ提出(ただし可能な範囲で)をメーカーに求めるとしています。
さらに既収載品と同様に「専門家による再分析」や「専門組織によるアプレイザル」も行われますが、その結果は価格算定には用いられません。
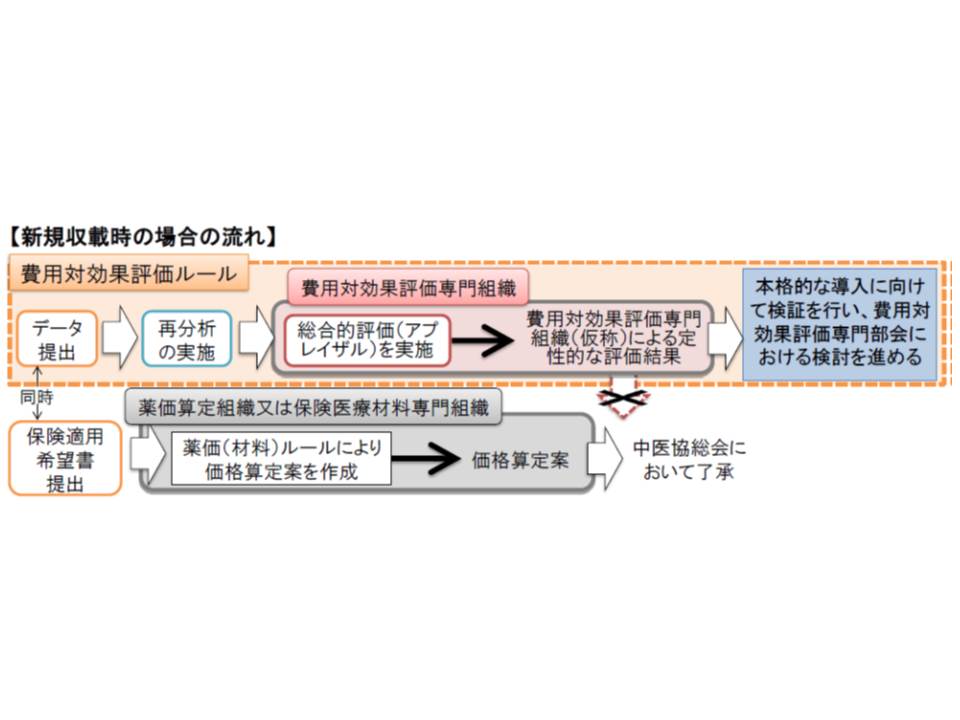
もっとも前述の「保険収載が遅れてしまう」という点が解決されれば、新薬・新規医療機器の価格算定にも費用対効果評価の仕組みが導入される可能性もあるでしょう。眞鍋企画官は、「迅速は評価に必要な体制」「新規収載時に提出されるデータの質や内容」などについて検討していく方針を明確にしています。
専門部会では、今後「対象品目の選定基準」が「評価に向けた具体的な運用方法」などを詰めていきます。
【関連記事】
費用対効果評価、対象は「保険収載後、1-2回の改定を経たもの」に―費用対効果評価専門部会
費用対効果評価、試行段階では社会的影響を評価する特別ルールは定めず―費用対効果評価専門部会
費用対効果評価の結果は医薬品・医療機器の再算定に活用―費用対効果評価専門部会
費用対効果評価はQALYを基本に実施、他の指標の使用も認める―中医協・専門部会
薬などの費用対効果、まず既収載品の再算定に活用、価格への反映は18年度改定時か―中医協・専門部会