2016年4月以降、費用対効果評価の対象として補正加算が高いものなど8品目程度を選定―中医協総会
2016.1.20.(水)
2016年度の次期診療報酬改定では、費用対効果評価を試行導入されます。当面は、既収載の医薬品・医療機器を対象にデータを収集し、2018年度の薬価改定・材料価格改定に反映させる(価格の再算定に用いる)こととなっていますが、その対象品目を選定するための基準が、20日に開かれた中央社会保険医療協議会の費用対効果評価専門部会と総会で了承されました。
2016年4月にも8品目程度が選定され、医薬品・医療機器メーカーは費用と効果に関するデータの準備をすることになります。
費用対効果評価の大枠と、2016年度からの大まかなスケジュールは、次のようになっています。
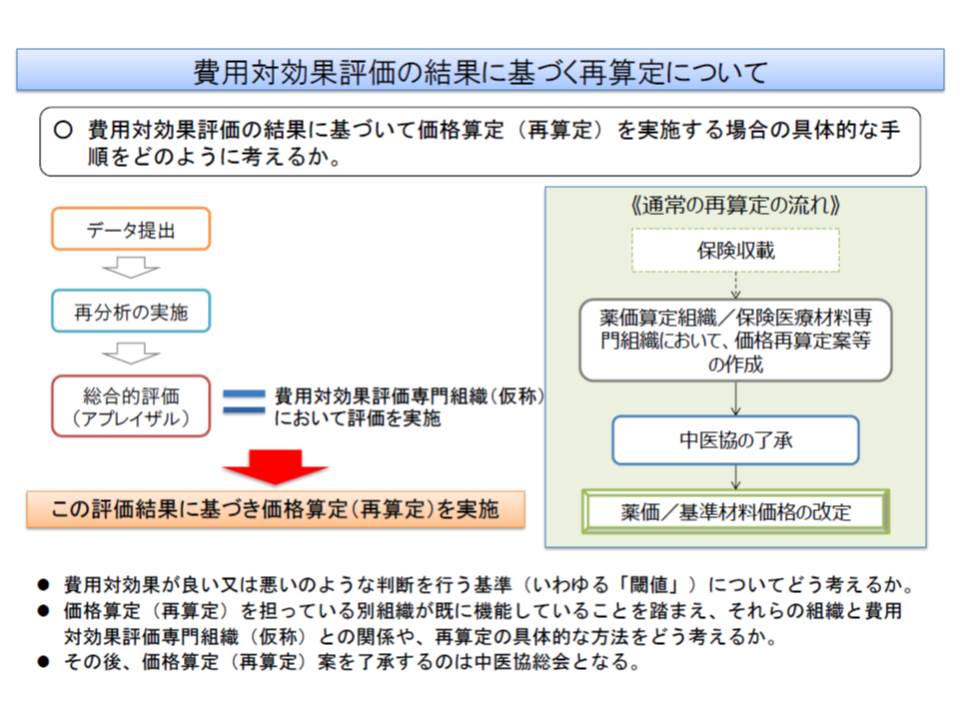
(1)製薬メーカー、医療機器メーカーが費用と効果に関するデータ、自社による費用対効果評価の分析結果を提出する(2016年4月から2017年3月にかけて)
↓
(2)厚生労働省内に設置される専門体制(再分析グループ)が、メーカー提出の分析結果について中立的な立場から再分析を行う(2016年度中)
↓
(3)新たに設置される費用対効果評価専門組織(仮称、中医協の下部組織)で、企業・再分析グループの分析結果について総合的評価(アプレイザル)を行う(2017年度以降)
↓
(4)費用対効果評価専門組織の評価結果をもとに、薬価算定組織と保険医療材料専門組織で価格調整を行う(再算定)(2018年2-3月)
20日の専門部会・総会では、(1)のデータ提出が義務付けられる品目を選定する際の基準が了承されました。基準に則って、類似薬効比較方式(類似機能区分比較方式)で保険収載されたもののうち4品目(医薬品2品目、医療機器2品目)、原価計算方式で保険収載されたもののうち4品目(医薬品2品目、医療機器2品目)に加えて、選定されたものと薬作用が類似する医薬品、同一機能区分に該当する医療機器が対象になります(関連記事はこちら)。
具体的な選定基準は次のとおりです。
【類似薬効比較方式・類似機能区分比較方式で収載されたもの】
○2012-15年度までの間に保険適用された品目のうち、「補正加算の加算率がもっとも高いもの」と「10%以上の補正加算が認められたものの中で、医薬品についてはピーク時予測売上高がもっとも高いもの、医療機器については保険償還価格がもっとも高いもの」を、それぞれ1品目(都合2品目)選定する(前者と後者が一致する場合は都合1品目となる)
【原価計算方式で収載されたもの】
○2012-15年度までの間に保険適用された品目のうち、「営業利益率の加算率がもっとも高いもの」と「10%以上の加算が認められたものの中で、医薬品についてはピーク時予測売上高がもっとも高いもの、医療機器については保険償還価格がもっとも高いもの」を、それぞれ1品目(都合2品目)選定する(前者と後者が一致する場合は都合1品目となる)
ただし、▽希少疾患(指定難病や血友病、HIV感染症など)用である▽医療ニーズが高いとして厚労省検討会からの開発要請・公募に応じて開発された―医薬品・医療機器は対象から除外されます。患者の適切な医療へのアクセスを確保するためです。
中医協では、「2016年度明け(つまり2016年4月)以降に選定を行う」ことが決まっており、選定された品目は公表されます。
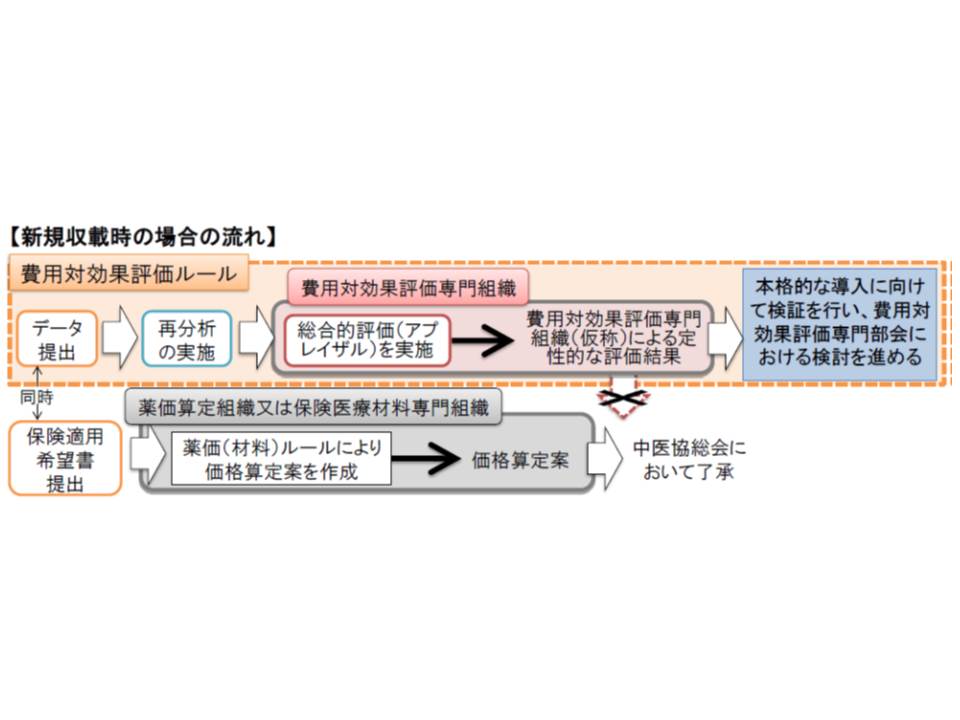
費用対効果評価に基づいて価格見直しが行われるのは、当面「既収載品」に限られます。新規収載時にデータを準備し、それを分析していたのでは、保険収載までに長期間がかかり、その医薬品・医療機器を待ち望んでいる患者に不利益を及ぼしてしまうからです。
しかし中医協では、「新規収載時にもデータ提出を求める」(価格設定には用いない)ことを決めており、20日の専門部会・総会では「データ提出が求められる新規収載品の選定基準」の大枠が固まりました。具体的には次のとおりで、「高い評価を希望する場合には、その根拠をメーカー自ら示してほしい」という厚労省の考えが見えてきます。
▽類似薬効比較方式・類似機能区分比較方式で「10%以上の補正加算を希望する」品目であって、別に定めるピーク時予測売上高以上のもの
▽原価計算方式で「10%以上の営業利益率の加算を希望する」品目であって、別に定めるピーク時予測売上高以上のもの
ただし、▽希少疾患用▽開発要請・公募品目―である医薬品・医療機器は、やはりデータ提出の対象から除外されます。
上記の基準にある「別に定めるピーク時予測売上高」は、前述の「費用対効果評価の対象となる既収載品」を指定する際に定められます(2016年4月以降)。
厚労省では、「新規収載品の選定基準(別に定めるピーク時予測売上高)が定まった後に保険適用希望書を提出する品目」について、保険適用希望書の提出時にデータ提出を求めることとしています。この点、20日の専門部会では「選定基準が定まった時点で、薬事法の承認間近な品目などはデータの準備が難しい。柔軟な対応をしてほしい」との要望も出されており、厚労省保険局医療課の眞鍋馨企画官は「検討する」考えを示しました。一定の場合には、データ提出が保険適用希望書の提出時点より遅くなることが認められる可能性があります。
【関連記事】
費用対効果の良し悪しを判断する基準値、2016年度改定では定めず―費用対効果評価専門部会
費用対効果評価、対象は「保険収載後、1-2回の改定を経たもの」に―費用対効果評価専門部会
費用対効果評価、試行段階では社会的影響を評価する特別ルールは定めず―費用対効果評価専門部会
費用対効果評価の結果は医薬品・医療機器の再算定に活用―費用対効果評価専門部会
費用対効果評価はQALYを基本に実施、他の指標の使用も認める―中医協・専門部会
薬などの費用対効果、まず既収載品の再算定に活用、価格への反映は18年度改定時か―中医協・専門部会