2016年度の薬価・材料価格制度改革、イノベーション評価などの骨子を中医協総会が了承
2015.12.25.(金)
2016年度の次期薬価制度改革、材料価格制度改革に向け、25日に開かれた中央社会保険医療協議会の総会では、それぞれについて改革の骨子が了承されました。
薬価については、画期的な新薬の開発意欲を向上させるために▽先駆け審査指定制度加算の創設(先駆導入加算からの見直し)▽新薬創出・適応外薬解消等促進加算の試行継続―などを行うほか、国民皆保険を維持するための「市場拡大再算定の特例」創設などが目立ちます。
一方、材料価格については、優れた医療機器の開発を促進するために、「医療ニーズの高い医療機器等の早期導入に関する検討会」からの開発要請・公募に応じて開発された製品についてさまざまな特例を設ける点が特筆できます。
薬価・材料価格制度については骨子をベースに厚生労働省が具体的な見直し案を策定し、年明けに改めて議論されることになります。
薬価制度改革については、次のような点が見直しのポイントと言えます(関連記事はこちら)。
▽2014年度改革で新設された先駆導入加算を、「先駆け審査指定制度加算」へ見直す(要件を見直し、加算率を最大20%にまで引き上げる)(関連記事はこちら)
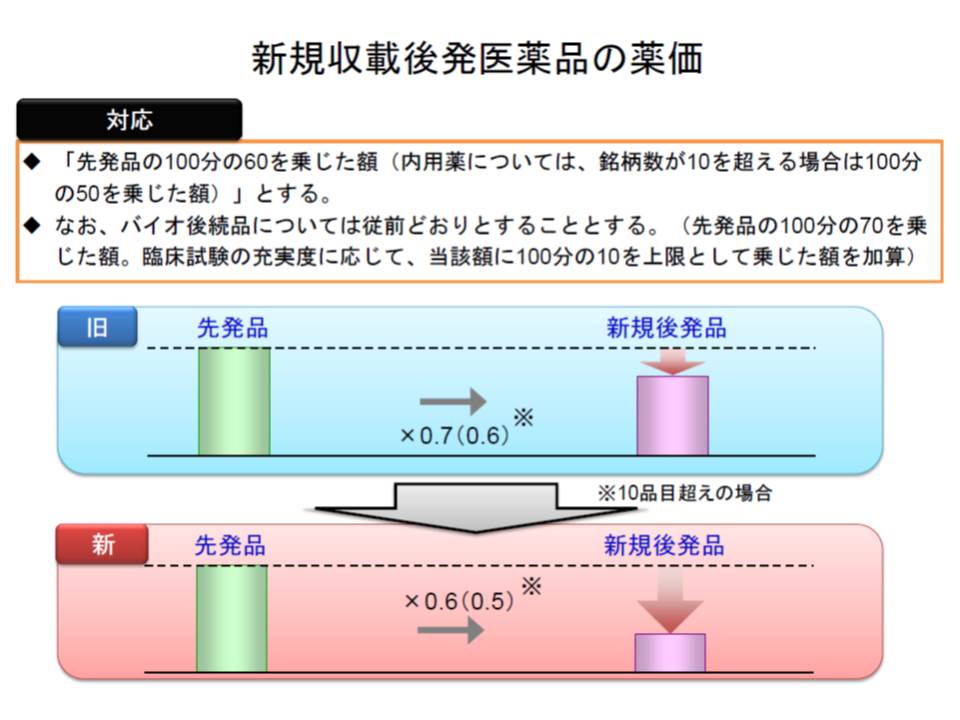
▽新規後発医薬品価格を、先発品の50%(銘柄数が10を超える内用薬は40%)とする(関連記事はこちら)
▽基礎的医薬品の価格を下支えする新ルールを試行導入する(関連記事はこちら)
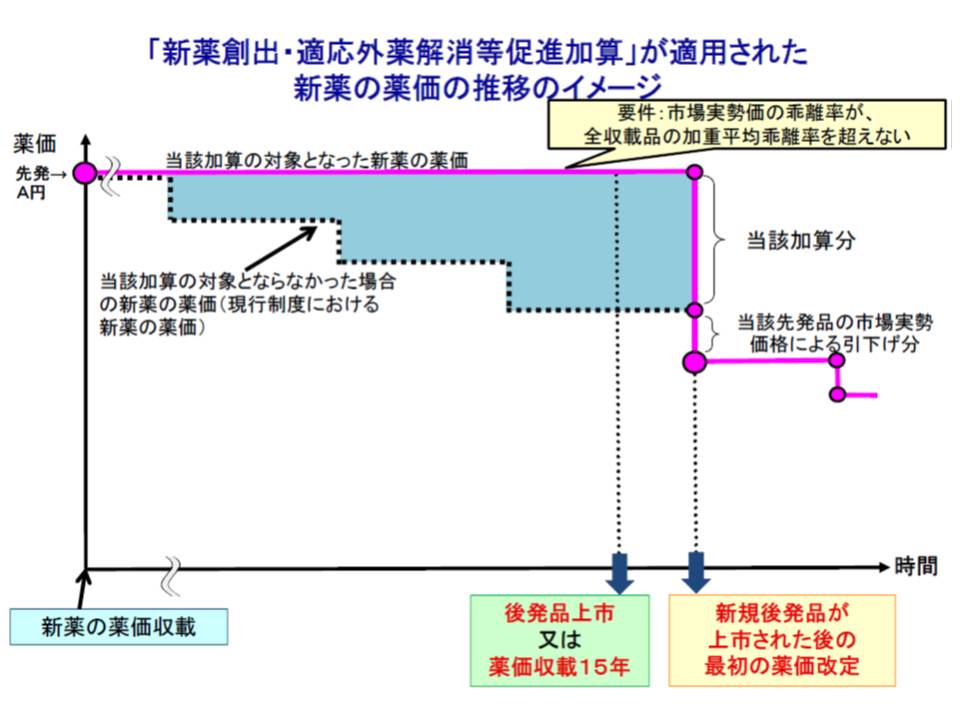
▽新薬創出・適応外薬創出加算の試行を継続する
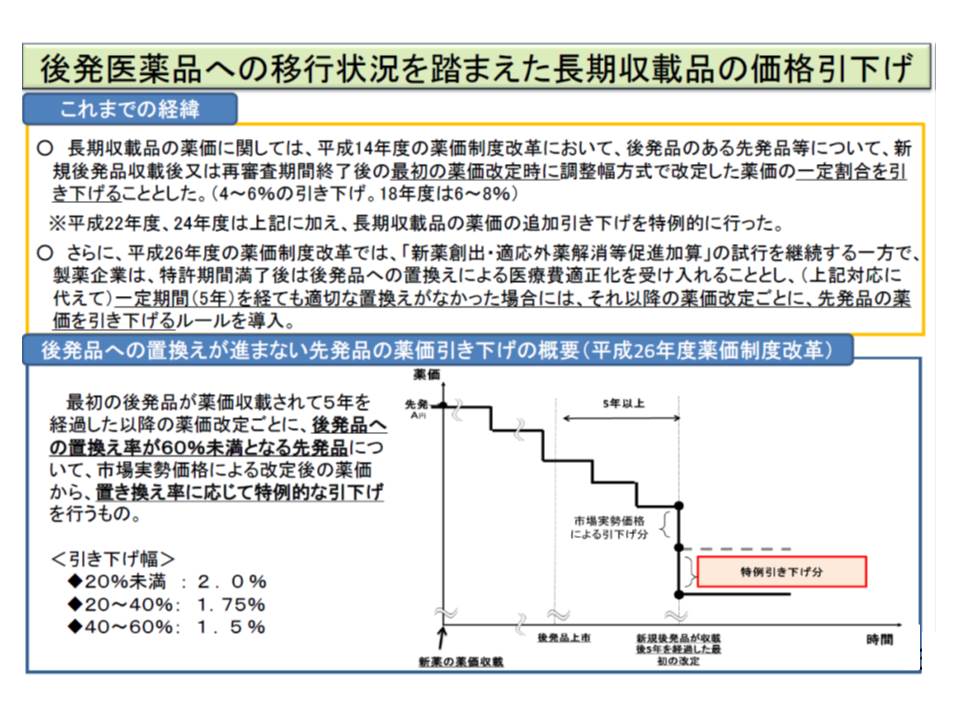
▽先発品から後発品への置き換えを進めるためのルール(いわゆるZ2)の要件を厳しくする(関連記事はこちら)
▽市場拡大再算定に関して、市場規模が巨額(年間販売額が1000億円超、かつ予想販売額の1.3倍以上など)な医薬品について、皆保険を維持するための特例再算定ルールを新設する(関連記事はこちら)
このうち「市場拡大再算定の特例」について、製薬メーカーサイドは「イノベーションを阻害するもの」と反発しています。25日の中医協・薬価専門部会では加茂谷佳明専門委員(塩野義製薬株式会社常務執行役員)から「効能・効果の追加など、薬価収載時からの条件変更がなく、市場規模が巨額という点のみに着目した価格引き下げは妥当ではない」との見解が改めて披露されました。その上で加茂谷専門委員は「特定の製薬企業に大きな負担を課す可能性がある。個別事情を勘案した対応をとってほしい」と強く求めています。
材料価格制度については、前述のように「医療ニーズの高い医療機器等の早期導入に関する検討会」(ニーズ検討会)からの開発要請・公募に応じて開発された製品についてさまざまな特例を設ける点がポイントです。デバイスラグの解消に向け、保険サイドからどのようなアプローチができるのかを熟慮した内容と言えるでしょう(関連記事はこちら)。具体的には、次のように整理できます。
▽通常であれば「外国平均価格の1.3倍超の場合、価格を1.3倍に引き下げる」ことになるが、ニーズ検討会の要請などに応じて開発された製品については「外国平均価格の1.5倍超の場合には、1.5倍に引き下げる」に止める
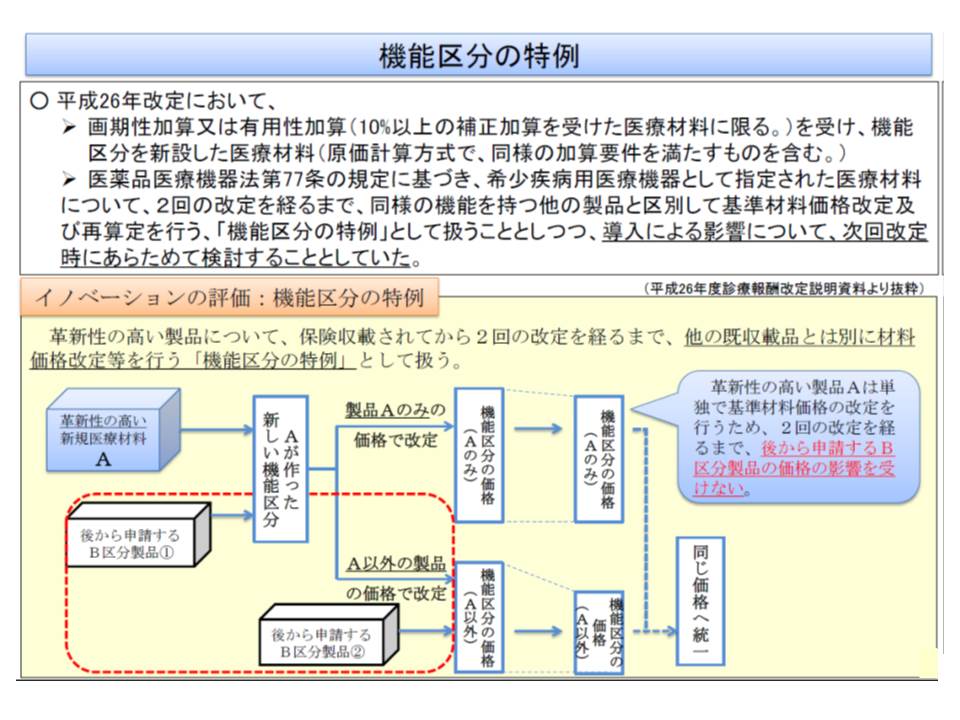
▽ニーズ検討会からの公募に応じて開発された品目のうち、「医療ニーズが高いものと選定されてから3年以内に薬事承認申請がなされている」などの要件を満たす場合には、機能区分の特例の対象とする(事実上の単一機能区分を設定し、2回の改定を経るまで高価格を維持できる)(関連記事はこちら)
▽ニーズ検討会からの公募に応じて一定の要件を満たす製品を開発した企業から、その次に保険適用希望書が出された製品について、「審査期間のうち申請者側の期間が一定以内」などの要件を満たす場合には、機能区分の特例の対象とする(関連記事はこちら)
【関連記事】
2016年度薬価制度改革の大枠固まる、後発品の価格は更なる引き下げ―薬価専門部会
市場拡大再算定、年間販売額1000億円超などの医薬品が対象に―薬価専門部会
医療上必要な基礎的医薬品、16年度から「薬価を維持する仕組み」を導入―中医協・薬価専門部会
長期収載品から後発品へのシフト促すZ2ルール、支払側は厳格化を要望―中医協・薬価専門部会
後発品の薬価、16年度改定で更なる引き下げ、詳細は薬価調査待ち―中医協・薬価専門部会
先駆導入加算、「先駆け審査指定制度」の要件に見直しへ―中医協
償還価格と実勢価格の乖離率、医薬品は8.8%、医療材料は7.9%―中医協総会
2016年度材料価格制度改革、骨子案了承し年明けから細部調整―中医協・材料専門部会
医療材料への市場拡大再算定導入を見据え、16年度改定で下準備進める―中医協・材料専門部会
医療ニーズが高く開発公募がなされた医療機器、開発した企業は高く評価する―中医協・材料専門部会