2023年度の薬価中間年改定に医薬品業界は反対!実施する場合でも特許期間中品目や安定確保品目は除外を要望—中医協・薬価専門部会
2022.10.27.(木)
来年度(2023年度)に予定される薬価改定(毎年度改定、中間改定)であるが、昨今の物価高騰や円安の影響を考慮すると、さらに、日本の医薬品市場の魅力低下に鑑みると、実施すべき状況にはない—。
仮に2023年度に中間年改定を行う場合であっても、「特許期間中の品目」や「医療上必要性の高い安定確保医薬品、不採算品再算定品目」などは対象から除外すべきである—。
10月26日の中央社会保険医療協議会・薬価専門部会で、製薬メーカー・医薬品卸業者からこういった意見が出されました。
日本の医薬品市場の無力は頻回な薬価制度改革で失われ、ドラッグ・ラグが再燃している
薬価制度の抜本改革が2018年度に行われ(関連記事はこちら(2018年度改革)とこちら(2020年度改革))、その一環として「毎年度の薬価改定実施」が行われています(ここで言う薬価改定は、公的価格・保険償還価格である「薬価」を、取引価格・市場実勢価格(卸-医療機関・薬局間での購入・販売価格)を踏まえて見直していくことを意味する)。
ほとんどの医薬品について、医療機関や薬局は「薬価よりも低い価格」で購入(市場実勢価格、取引価格)し、保険者や患者へは公定価格である「薬価」で請求を行います(両者の差が、いわゆる「薬価差」である)。医療保険財政の健全化などを目的に「市場実勢価格を踏まえて、薬価を引き下げていく」ことが求められ、従前からの「診療報酬改定に合わせて2年に1度行う薬価改定」を、「中間年にも行う」ことになったものです。
10月5日の薬価専門部会で、2023年度薬価改定のキックオフ論議が行われ(関連記事はこちら)、10月26日には▼日本製薬団体連合会▼日本製薬工業協会▼日本ジェネリック製薬協会▼米国研究製薬工業協会(PhRMA)▼欧州製薬団体連合会(EFPIA)▼日本医薬品卸売業連合会—から意見聴取が行われました。業界団体の意見は次のような内容でほぼ一致しています。
(1)2023年度の中間年改定は慎重に検討すべきである(端的に「見合わせる」べきである)
(2)仮に中間年改定を行う場合でも「特許期間中の品目」や「医療上必要性の高い安定確保医薬品、不採算品再算定品目」などは対象から除外すべきである
こうした意見の根拠・背景として、▼物価高騰・円安の影響で医薬品業界の大きなダメージを受けており、2023年度にも薬価引き下げを行えば、さらなる厳しい状況に陥ってしまう▼とわけ2018年度以降「日本の医薬品市場」の魅力が大きく低下しており、2023年度にも薬価引き下げを行えば、さらなる魅力低下となり、深刻なドラッグ・ラグが生じてしまう—という2点が掲げられています。
前者については、例えば「原薬・原材料などの価格高騰」や「海外での治験等の臨床研究コストなどの高騰」などがあげられます。一般製造業であれば「価格の引き上げ」(コストの価格への転嫁)という手段を選択できますが、医薬品製造業においては「薬価という公定価格が決まっており、販売価格への転嫁が難しい」「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律により製造工程の見直し・効率化(例えば原材料を安価なものに切り替える)や製造量の調整などが行えない」、つまり「コスト増を吸収できない」という制約があるのです。この問題は、とりわけ「低価格の医薬品」(後発品など)において深刻な影響を及ぼします。
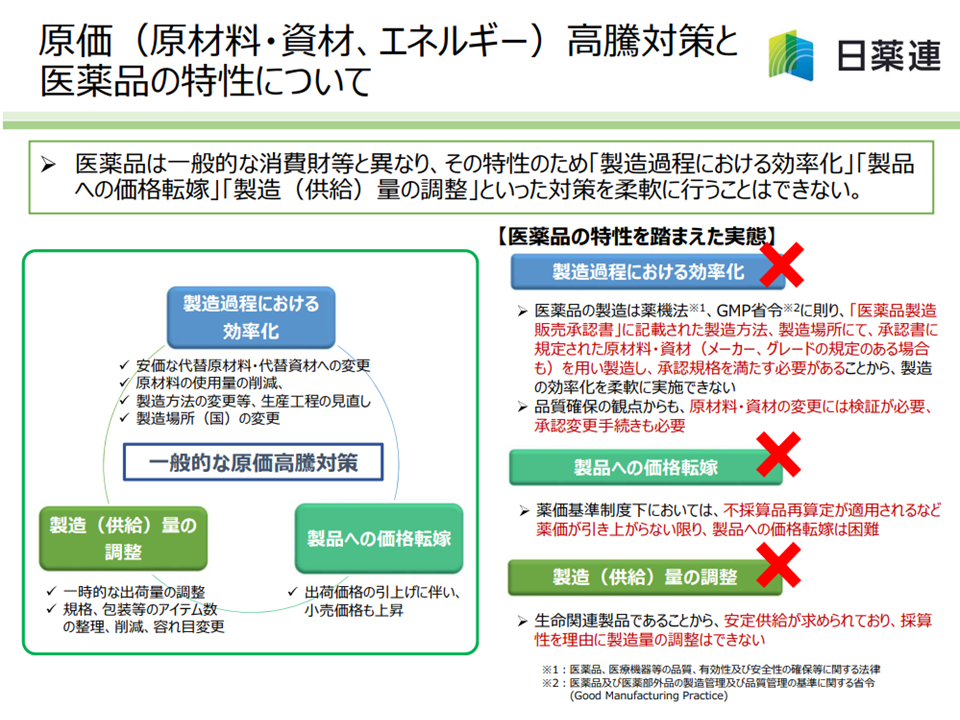
コスト高騰分を価格転嫁することなどは、ただちにはできない
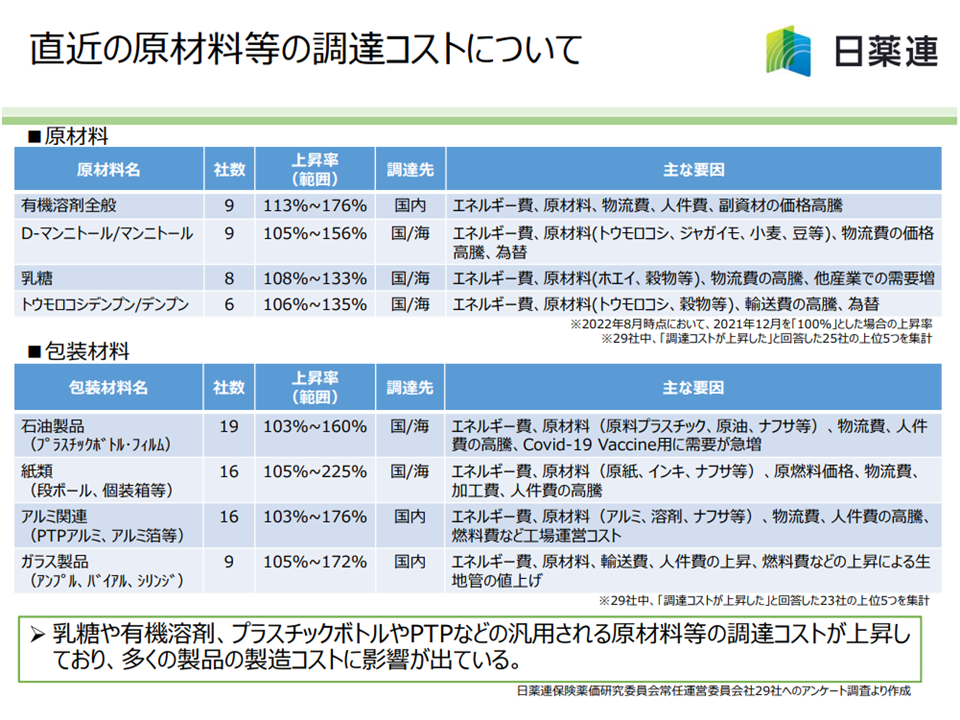
原材料等のコストが高騰している
一方、後者は、我が国において「薬価制度の頻回な見直し」により市場の魅力が失われ、製薬メーカーにそっぽを向かれかねないという問題です。
例えば、▼【新薬創出・適応外薬解消等促進加算】により画期的医薬品の薬価下支えが行われているが、対象企業・品目要件が厳格化され「恩恵」にあずかれるケースが極めて限定的になってしまった(加算額全体の規模も縮小している)▼【市場拡大再算定】により「優れている」と市場(医療機関)に判断された医薬品の価格が強制的に引き下げられてしまっている▼頻回な薬価制度改革により、製薬メーカーにとって「先が見通せない」状況に陥ってしまっている—ことなどにより、「日本での研究開発・上市に向けて投資を行うべきだろうか?日本では薬価制度が頻繁に変わるため、先が見通せない。優れた医薬品を開発しても、狙い撃ち的な薬価の引き下げが行われ、投下コストを回収できない。日本への投資財源を、別国での投資に充てるべきである」とメガファーマなどで判断されてしまっていると指摘されます。
日本の医薬品市場には、「国民皆保険制度が整備され、安全性・有効性が確認された医薬品は基本的に保険適用されるため、非常に大きな市場である」という優れた面がありますが、昨今の薬価制度改革により「その優れた面が帳消しになってしまっている」との指摘もあります。営利企業から見れば、「利益の出やすい市場」(=魅力的な市場)を優先し、「利益の出にくい市場」(=魅力のない市場)が劣後するのは当然とも言えます。
現に、次のようなデータが示されており、すでに「日本国民は、世界的な優れた医薬品、長期間にわたって安全性・有効性が確立されてきた安価な医薬品の双方にアクセスできない」事態が生じているのです。
▽2020年における世界での売り上げ上位300品目(いわばメジャー医薬品)について
▼「最初に我が国に上市」される医薬品の割合は僅か6%で、米国65.3%、欧州31.0%に大きく劣っている
▼上位300位医薬品の17.7%は我が国では未上市である
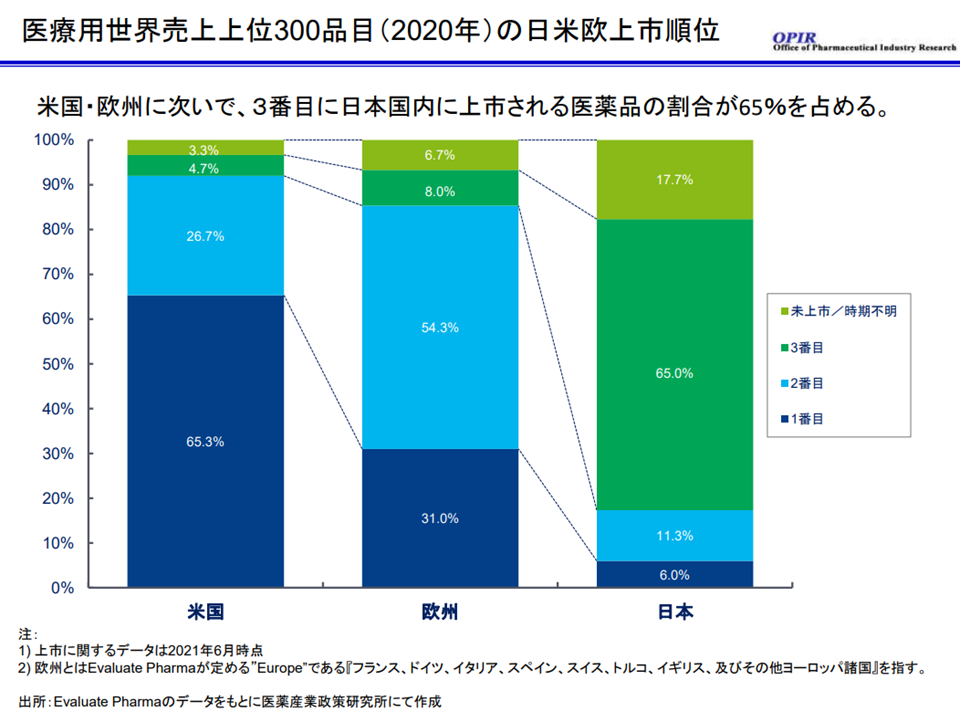
我が国では、世界のメジャー300医薬品のうち2割が未承認であり、我が国で最初に上市される嫌医薬品は非常に少ない(医薬品安定供給検討会1 220831)
▽2020年度において「直近5年間に欧米で承認された医薬品」のうち、72%が我が国で未承認である
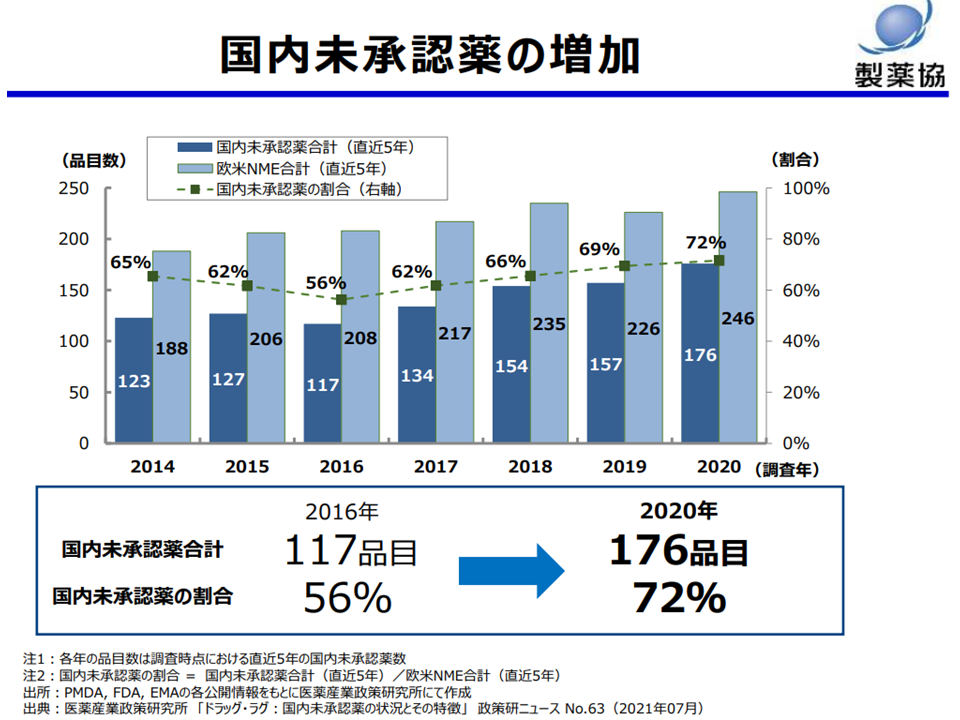
我が国では、ここ5年間において外国で承認されてきている医薬品のうち72%が未承認である(医薬品安定供給検討会2 220831)
後者の、いわゆる「ドラッグ・ラグの再燃」は「日本国民の健康・生命に悪影響を及ぼす」という最悪の事態を招いてしまうため、「真剣に対応策を考えなければいけない」状況と言えます(関連記事はこちら)。
こうした意見・状況に診療側の有澤賢二委員(日本薬剤師会常務理事)は理解を示しましたが、同じく診療側委員の長島公之委員(日本医師会常任理事)は「特許期間中の品目を2023年度改定から除外すべきとの点については議論の余地があると思う」(「特許期間中」であっても、優れた価値を持つものと、そうでないものとがある)、「物価上昇などが個別医薬品の製造コストをどのように引き上げているのかなど、より詳しいデータを出してほしい」とコメントしています。
他方、支払側の松本真人委員(健康保険組合連合会理事)は「皆保険体制を敷いている我が国の医薬品市場が『魅力なし』と言われても、即座には納得しがたい」と反論しています。しかし、上記のようなドラッグ・ラグに関するデータも出ており、客観的な視点で「我が国の医薬品市場が、諸外国と比べて優れているのか、劣っているのか」を早急に見極める必要があるでしょう。「こうに違いない」という思い込みに基づく議論は極めて危険です。
また松本委員は、業界団体の要望する「2023年度の中間年改定を行わない」との選択肢について、「中医協の所掌の範疇を超えている」(政府が高次の判断で検討すべき事項である)と指摘しています。厚生労働省の担当者も「2023年度の中間年改定を行うという前提で、中医協論議を進める」との考えを示しており、当面は「2023年度中間年改定の是非」ではなく「2023年度中間年改定をどのような形で行うか」が議題となる見込みです。
長島委員の要望した「詳細なデータ」への回答に期待が集まります。
【関連記事】
2023年度の薬価中間年改定に向けた本格議論開始、対象品目・引き下げ幅・適用ルールなどをどう考えていくか—中医協・薬価専門部会
2023年度の中間年度薬価改定、「医薬品を取り巻く状況の大きな変化」をどう勘案するかが今後の論点に—中医協
2021年度に初の中間年度「薬価改定」、市場実勢価格連動ルールのみ適用するなどの骨子了承―中医協総会(2)
2020年薬価調査結果は従前と同水準、21年度改定の実施は予算編成過程で政府が決定―中医協・薬価専門部会
2020年薬価調査実施とその内容を決定、2021年度改定の是非は改めて検討—中医協総会(1)・薬価専門部会
薬価・材料価格制度の見直し案を決定、14成分の医薬品が市場拡大算定―中医協総会 第384回(2)
2020年度薬価制度改革を了承、類似薬効方式(I)で新薬創出等加算対象外の新薬は一定期間後に大幅薬価引き下げ―中医協総会(2)





