神経麻酔分野の小口径コネクタ製品、新規格と既存規格との変換コネクタは原則使用不可―厚労省
2017.12.30.(土)
神経麻酔分野の小口径コネクタ製品について、相互接続防止のための国際規格に準拠した製品(新規格製品)が順次、上市されていく。この点、新規格製品と既存規格製品とが併存し、医療事故が発生しかねないため、既存規格製品から新規格製品への切り替え期間などを設定する—。
厚生労働省は12月27日に、こういった内容の通知「神経麻酔分野の小口径コネクタ製品の切替えについて」を発出しました。厚労省は「医療現場で支障が生じる」として医療機関から要請がある場合を除き、新規格製品と既存規格製品との変換コネクタを使用してはならない旨を指示しています。
既存規格製品の販売は2020年2月まで、新規格製品への速やかな切り替えを
医療現場では、さまざまなチューブやラインを患者に接続します。その際、例えば「経腸栄養剤を、誤って血管内に注入してしまう」といった事故が発生しかねないため、製品分野間の相互接続を防止するコネクタに係る国際規格(ISO(IEC)80369シリーズ、以下「新規格」)の制定が進められています。
新規格では、ベッドサイドで起こりうるコネクタ接続を、(1)呼吸器システムおよび気体移送(2)経腸栄養(3)皮下注射および血管系等(4)神経麻酔(脊椎麻酔、硬膜外麻酔および神経ブロック)(5)四肢のカフ拡張(6)泌尿器—の6種類に分類し(現時点)、異なる種類間では相互接続できない(非嵌合性)ように、形状を規定します。
ただし、新規格製品と既存規格製品とが併存した場合、両者を接続できない事態が生じてしまい、医療現場でトラブルが発生することが想定されます。そこで厚労省は今般、(4)の「神経麻酔(脊椎麻酔、硬膜外麻酔および神経ブロック)」分野の小口径コネクタ製品について、トラブル防止のために、次のように切替え期間などを定めています。
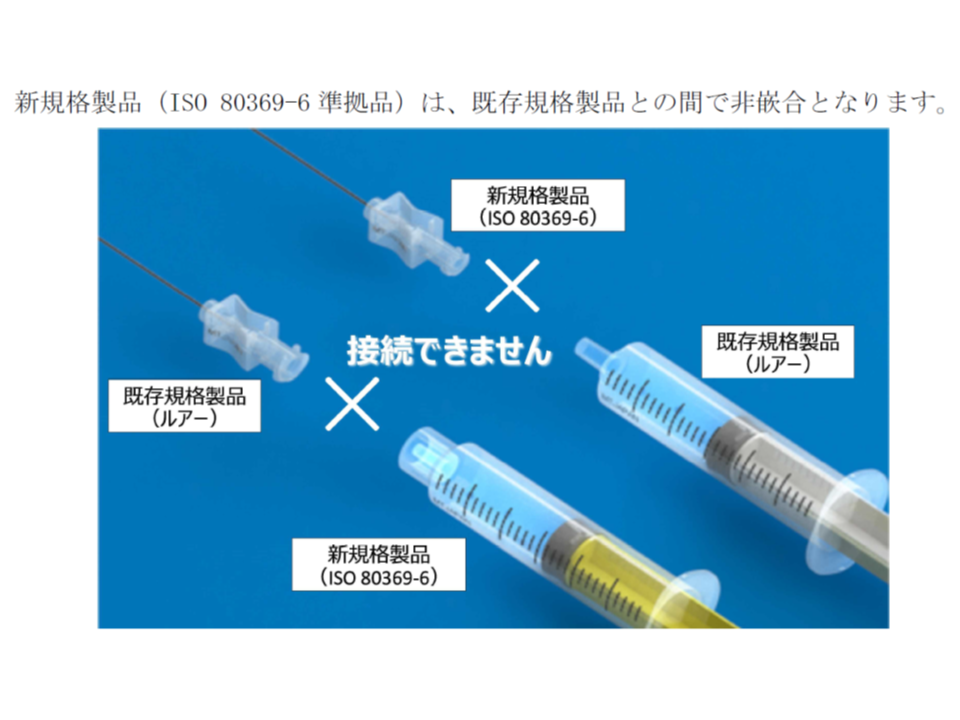
新規格製品と既存規格製品をつなぐことはできない。
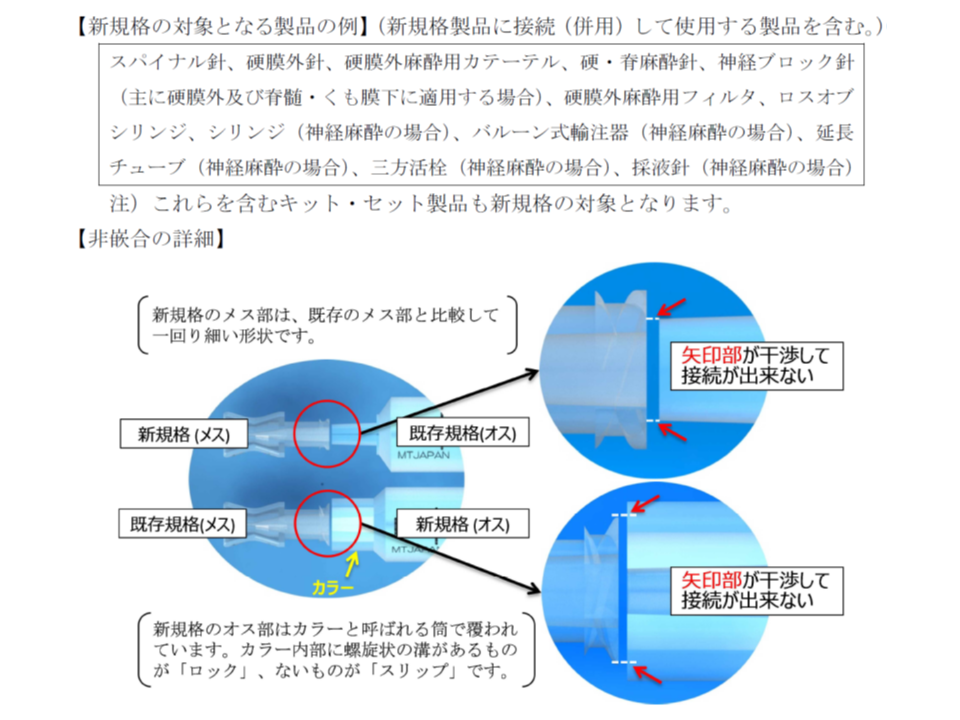
新規格の対象となる神経麻酔分野の製品の例
まず、既存規格製品メーカーは、承認基準等(例えば「麻酔用滅菌済み穿刺針承認基準」など、下表参照)の改正日以降、既存規格製品から新規格製品の変更に必要な手続きを速やかに行うことが求められます。さらに、医療現場における新規格製品への切替えを速やかに行うため、既存規格製品の出荷期間は「承認基準等の改正日から2年を経過した月末(2020年2月末)まで」と限定されました。

神経麻酔分野で、新規格への切り替えが進められる品目
また、新規格製品と既存規格製品の混同を防止するため、新規格製品には「ISO80369-6」の文字を記載するなど、製品の「二次包装」に識別のための表示を行うことが求められます。さらに、取り違え防止などの観点からは、▼医療機器本体▼一次包装—についても識別表示を行うことが望ましいと厚労省は要望しています。
ところで、既存規格製品と新規格製品を接続するためのコネクタ(変換コネクタ)については、誤接続を招くため、「原則、使用しないこと」とされました。これを容認すれば、そもそも国際規格を定めた意味がなくなってしまうからです。
ただし、医療機関から「医療現場において治療等に支障を来してしまう。既存規格製品から新規格製品へ接続する変換コネクタを準備してほしい」との要望があった場合には、「必要最小限量の変換コネクタを提供する」ことは認められます。メーカー等が変換コネクタを提供できる期間は、既存規格製品の出荷期間と同様、つまり2020年2月末までと定められました。
医療現場においては、事故防止のために▼製品が既存規格製品なのか、新規格製品なのかを逐次、確認する▼むやみに変換コネクタを用いず、新規格製品への切り替えを可能な限り速やかに進める—ことが求められるでしょう。
【関連記事】





