遺伝子パネル検査に基づく「適応外抗がん剤」使用、患者申出療養での実施を承認―患者申出療養評価会議
2019.9.13.(金)
遺伝子パネル検査・エキスパートパネル(専門家会議)での解釈などを経て、「適応外の抗がん剤」使用を患者申出療養として実施するためのプロトコルが整備された。今般、このプロトコルを活用した患者申出療養の申し出がなされ、「適」と判断する―。
9月12日に開催された「患者申出療養評価会議」(以下、評価会議)で、こうした点が了承されました。
目次
がんゲノム医療の推進に向け、遺伝子パネル検査の保険適用など進む
患者申出療養は、2016年4月1日からスタートした新たな保険外併用療養制度(保険診療と、保険外診療との併用を認める仕組み)です。傷病と闘う患者の「海外で開発された未承認(保険外)等の医薬品や医療機器を使用したい」などの希望・申し出を起点として、安全性・有効性を評価会議で確認した上で、保険診療との併用を可能とするものです。
これまでに、次の7種類の患者申出療養が認められています。
(1)腹膜播種・進行性胃がん患者への「パクリタキセル腹腔内投与および静脈内投与ならびにS-1内服併用療法」
(2)心移植不適応な重症心不全患者への「耳介後部コネクターを用いた植込み型補助人工心臓による療法」(関連記事はこちら)
(3)難治性天疱瘡患者への「リツキシマブ静脈内投与療法」(関連記事はこちら)
(4)髄芽腫、原始神経外胚葉性腫瘍または非定型奇形腫様ラブドイド腫瘍患者への「チオテパ静脈内投与、カルボプラチン静脈内投与およびエトポシド静脈内投与ならびに自家末梢血幹細胞移植術の併用療法」(関連記事はこちら)
(5)ジェノタイプ1型C型肝炎ウイルス感染に伴う非代償性肝硬変患者への「レジパスビル・ソホスブビル経口投与療法」(関連記事はこちら)
(6)進行固形がん(線維芽細胞増殖因子受容体に変化を認め、従来治療法が無効、かつインフィグラチニブによる治療を行っているものに限る)患者への「インフィグラチニブ経口投与療法」(関連記事はこちら)
(7)早期乳がん患者への「ラジオ波熱焼灼療法」(関連記事はこちら)
今般、8つめの患者申出療養として、「遺伝子パネル検査による遺伝子プロファイリングに基づく複数の分子標的治療」が認められました。
我が国でも「A遺伝子に変異が生じたがん患者にはαという抗がん剤が効果的である」といった科学的知見に基づく「がんゲノム医療」が進められています(関連記事はこちら)。
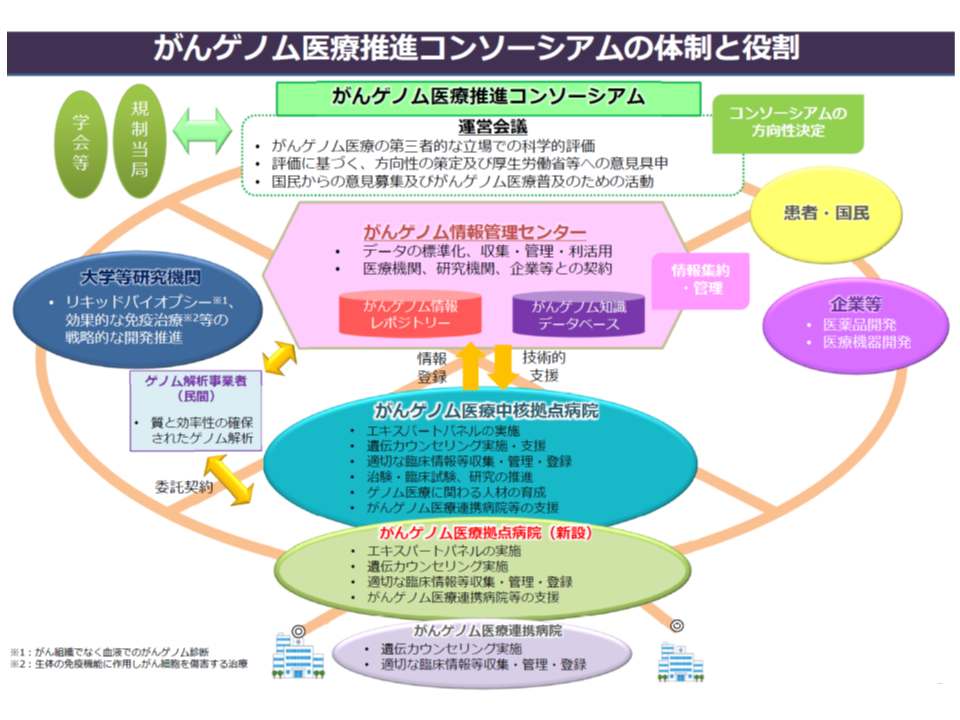
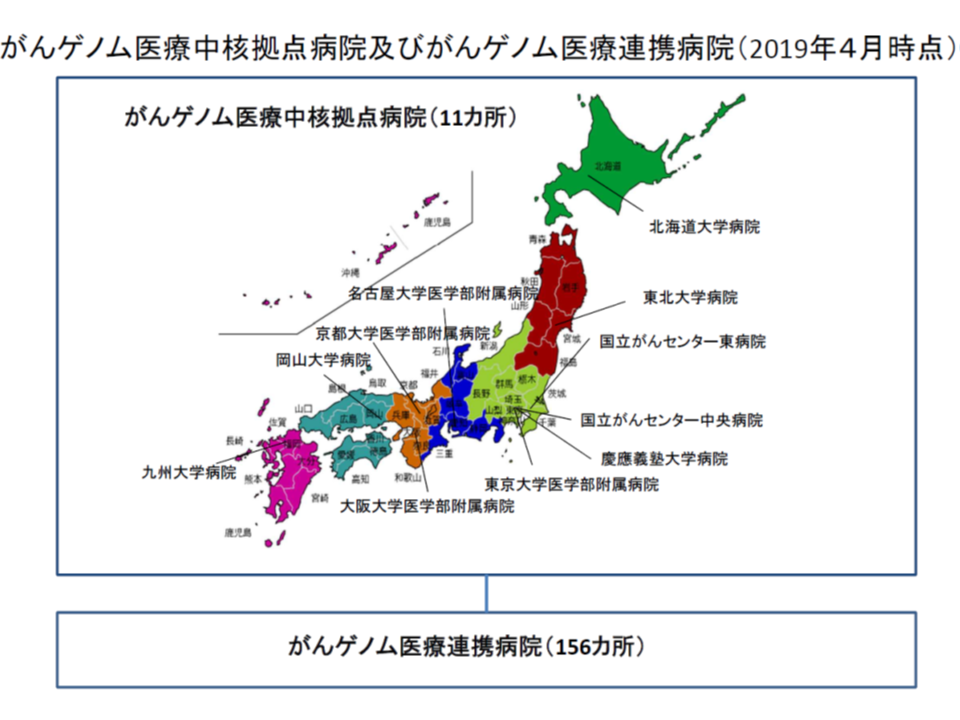
例えば、昨年(2018年)2月には、遺伝子変異の情報を解釈する専門家会議(エキスパートパネル)を設置して自らがんゲノム医療を完結でき、かつ人材育成等の役割を持つ「がんゲノム医療中核拠点病院」を11か所設置(▼北海道大学病院▼東北大学病院▼国立がんセンター東病院▼国立がんセンター中央病院▼慶應義塾大学病院▼東京大学医学部附属病院▼名古屋大学医学部附属病院▼京都大学医学部附属病院▼大阪大学医学部附属病院▼岡山大学病院▼九州大学病院―)(関連記事はこちら)。
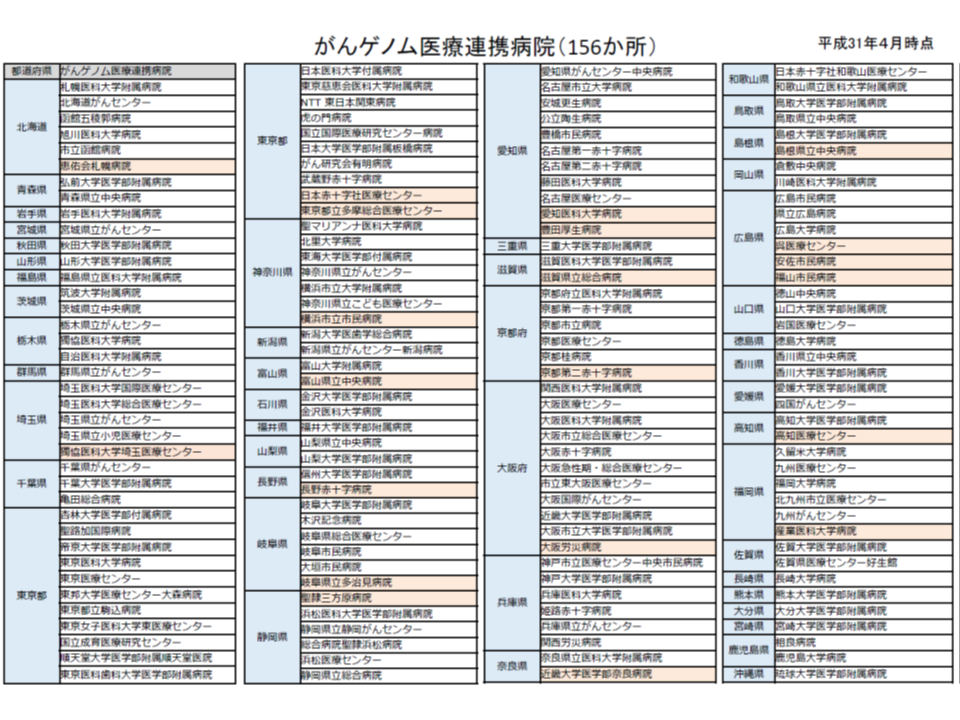
今年(2019年)6月には、多数の遺伝子変異の有無を一括して検出する「遺伝子パネル検査」を2種類、保険適用しました(▼FoundationOne CDx がんゲノムプロファイル▼OncoGuide NCC オンコパネル システム―)(関連記事はこちらとこちらとこちらとこちら)。
がんゲノム医療は、こうした体制整備の下で、大きく次のような流れで進められます。
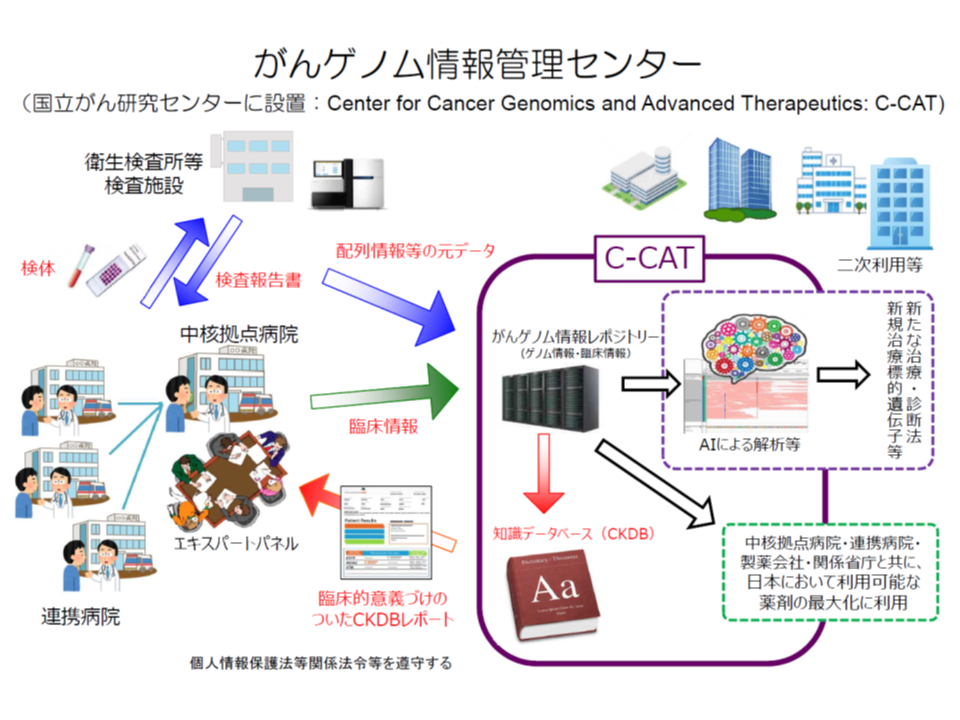
▽がんゲノム医療を希望する患者に対し、がんゲノム医療中核拠点病院等が十分な説明を行い、同意を得た上で、▼遺伝子情報(塩基配列など)▼患者の臨床情報(患者の年齢や性別、がんの種類、化学療法の内容と効果、有害事象の有無、病理検査情報など)―を、「がんゲノム情報管理センター」(C-CAT、国立がん研究センターに設置)に送付する
↓
▽C-CATで、保有するがんゲノム情報のデータベース(がんゲノム情報レポジトリー・がん知識データベース)に照らし、当該患者のがん治療に有効と考えられる抗がん剤候補や臨床試験・治験情報などの情報をがんゲノム医療中核拠点病院の専門家会議(エキスパートパネル)に返送する
↓
▽がんゲノム医療中核拠点病院の専門家会議(エキスパートパネル)において、当該患者に最適な治療法を選択し、これに基づいた医療をがんゲノム医療中核拠点病院等で提供する
がん再発患者等の意向に迅速に対応すべく、「適応外抗がん剤」使用プロトコルを事前整備
ただし、現時点では最適な抗がん剤が見つかるケースは全体の10-20%にとどまり(米国の研究では▼「既承認の抗がん剤が効く」ケース:9%程度▼「既承認の抗がん剤を適応外使用(例えば「肺がん」治療に効果が認められている抗がん剤を、効果が未確認の「胃がん」治療に用いるなど)することが考えられる」ケース:9%程度▼「未承認の抗がん剤が候補となるであろう」ケースが18%程度―と推計)、また、見つかったとしても「その抗がん剤が、当該患者のがん種について、薬事承認が得られていない」ケースも少なくありません(X1抗がん剤はx遺伝子変異のがんに効果があるが、効能効果が「肺がん」に限られている、など)(関連記事はこちらとこちら)。
薬事承認が得られていない抗がん剤を使用する手法の1つとして「患者申出療養」があります。標準治療を終えた、あるいは標準治療の確立していないがん患者の「未承認の抗がん剤を使用したい」という藁にも縋る思いに応えるものです。
もっとも、患者申出療養の申請をするためには、▼かかりつけ医との相談▼臨床研究中核病院への相談▼臨床研究中核病院における診療計画(プロトコル)作成―などが必要で、これらの手続きに少なくとも数か月かかってしまいます。
現時点では、遺伝子パネル検査の対象は「標準治療を終えた、終える見込みの患者」(再発や難治のがん患者)とされ(関連記事はこちらとこちらとこちら)、一刻も早く、効果の可能性の高い治療法にアクセスできる環境を整備することが必要です。
そこで評価会議では、次のような「迅速に患者申出療養を申請できる仕組み」整備しました。「複数のがん種」「多くの抗がん剤」を事前に想定しておき、「想定の範囲の中で患者申出療養を実施する」場合には、簡易な手続きで実施を認めるというイメージです(関連記事はこちら)。
▽がん遺伝子パネル検査の結果、既承認薬(固形がん約10種類の遺伝子異常と、それに対応する約20種類の分子標的薬)の「適応外使用」を希望して患者申出療養を申請する患者を想定し、臨床研究中核病院との協議の上で、▼複数のがん腫や遺伝子異常に対応できる「研究計画書」(プロトコル)を予め作成し、臨床研究審査委員会等の審査を経ておく▼臨床研究中核病院で研究計画書を共有する▼患者の同意を得た上で「症例データを一括保存」し、活用をする―
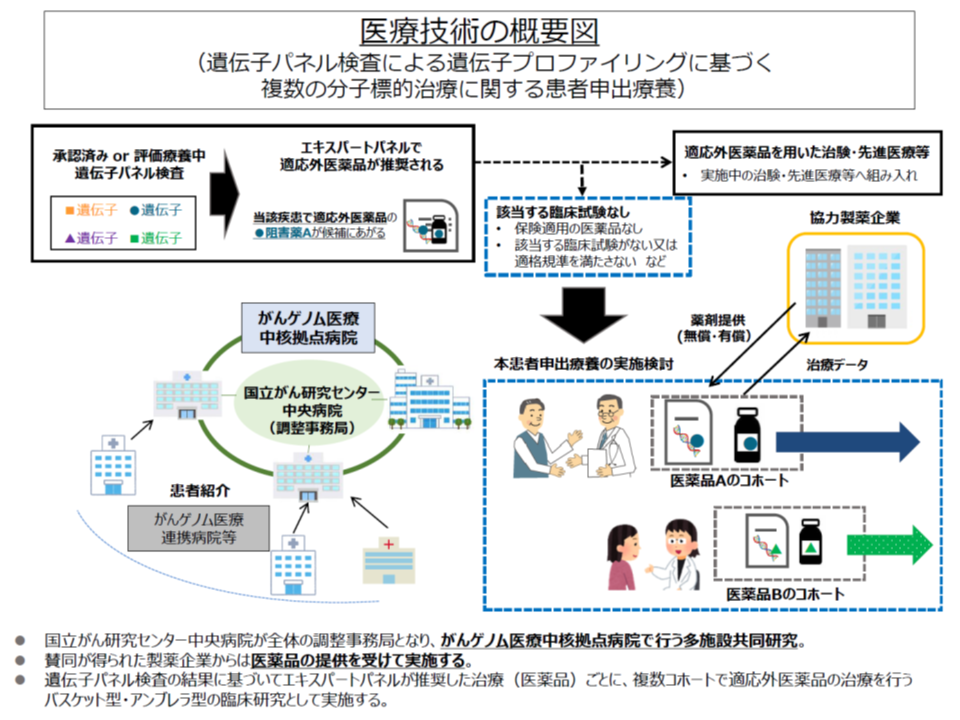
さらに、国立がん研究センターが「プロトコル」の言わば雛型を作成(関連記事はこちら)。今般、この雛型に沿った初めての患者申出療養の申請となり、標準治療を終了したある固形がん患者が、先進医療の中で遺伝子パネル検査を行い、エキスパートパネルが「効果の可能性のある抗がん剤」を見つけたものの、保険適用外であったことから「患者申出療養として使用したい」と申し出たものです。プロトコル作成から間もない申し出から、がん患者がゲノム医療に強く期待している状況が伺えます。
評価会議では、この申し出を審査し8つ目の患者申出療養とすることを承認しました。患者負担は約42万4000円(保険診療における自己負担が約5万7000円、患者申出療養に係る自己負担が約36万7000円)とされていますが、患者の状態により異なってくる点に留意が必要です。審査を担当した山口俊靖委員(がん研究所有明病院名誉院長)は、▼地理的な問題、病院のキャパシティの問題が生じる可能性があり、早急に実施施設拡大の方向で検討すべき▼企業への遺伝情報などの提供に関し、その範囲、期限などを明確にするとともに、患者が正しく理解できるよう丁寧かつ平易に説明する必要がある―とのコメントを付しています。
今後、「遺伝子パネル検査で、保険適用外の抗がん剤に効果の可能性があると判明した。当該抗がん剤を患者申出療養として使用したい」と考えた患者に対しては、それがプロトコルの範囲内である限り(例えば血液がんなどは、プロトコルに含まれていない)、今回の患者申出療養を「前例」として、国立がん研究センター病院あるいは他のがんゲノム医療拠点病院(追加実施医療機関となる)でより迅速に実施することが可能となります(申請から2週間以内)。
なお、現時点ではプロトコルにはノバルティスファーマ社の抗がん剤(同社から無償提供)のみが記載されていますが、国立がん研究センターでは、他社とも交渉を行っており、今後、「プロトコルの中で使用可能な抗がん剤」は徐々に増えていく見込みです。がんゲノム医療が着々と進んでいる状況が伺えます。
患者申出療養に適切にアクセスできているか、医療現場から聞き取りも
9月11日の評価会議では、これまでに患者からなされた全ての「申し出」の状況が厚生労働省から報告されました。
2016年4月から今年(2019年)8月末までに129件の「患者からの申し出」があり、うち7件(5.4%)が新規の「患者申出療養」として実施することが認められました。
ほか122件の状況を見ると、(i)拡大治験(日本版コンパッショネートユース)等の治験、先進医療等、他の臨床試験へ参加:20件(ii)既承認の患者申出療養に参加:4件(iii)相談継続中:4件(iv)制度一般に関する照会など、具体的な技術に関する相談ではなかったもの:44件(v)一度相談があったが、その後、現在までに相談がないもの:25件(vi)医療機関等で「患者申出療養として実施困難」と判断したもの:25件―となっています。
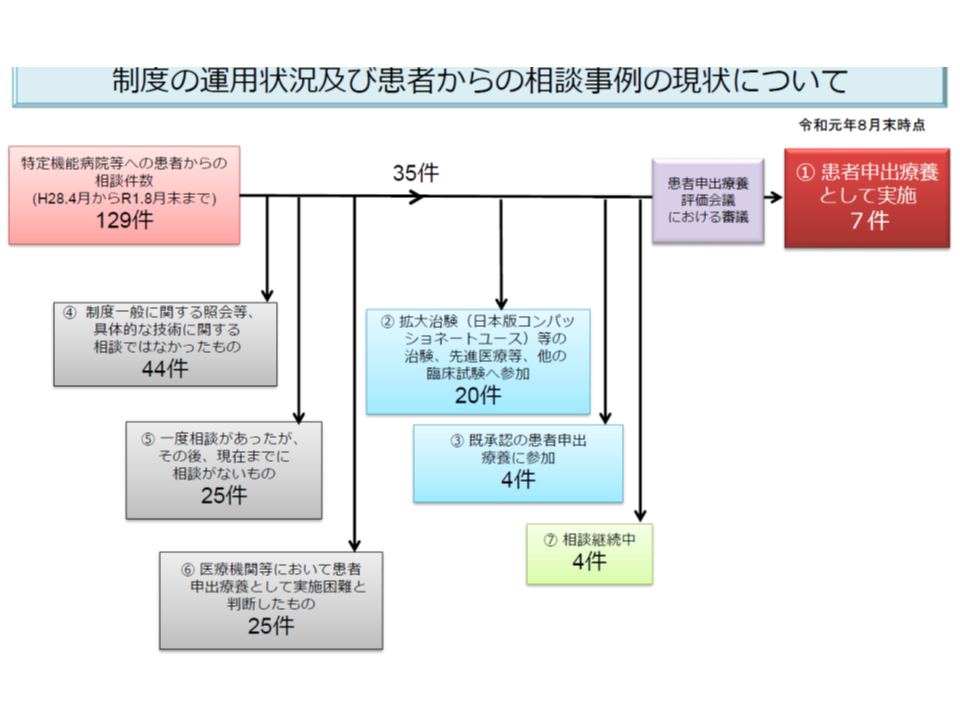
(vi)の「患者申出療養として実施困難」と判断された理由を見ると、「患者の状態から安全性等に問題があった」「医薬品の入手が困難であった」「費用面から患者が断念した」「他の治験等への参加を検討した」などさまざまです。
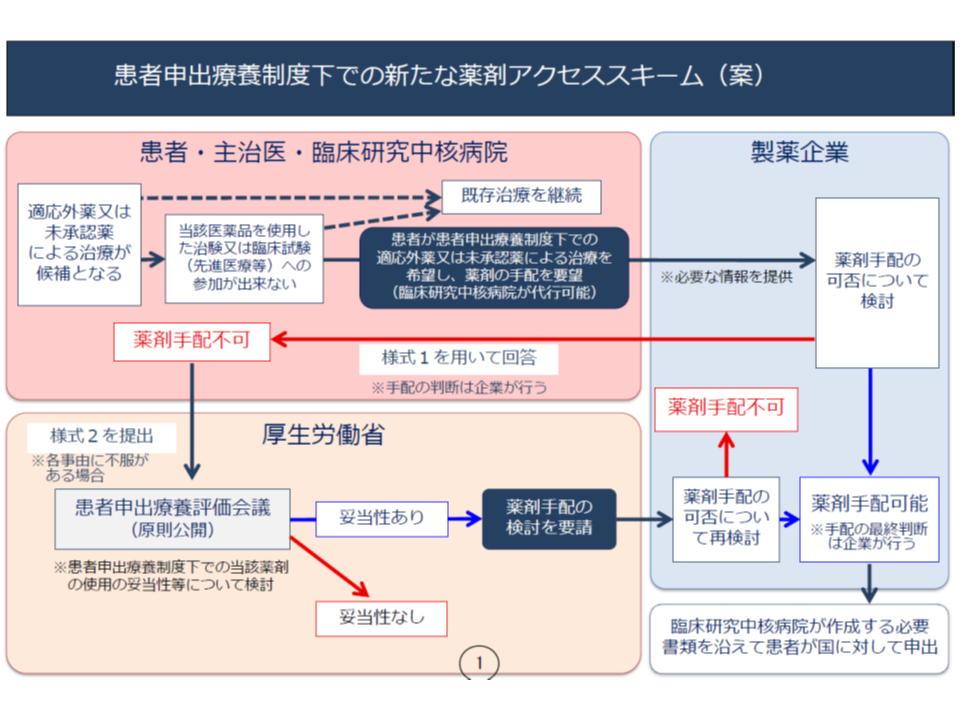
ただし、このうち「医薬品の入手が困難」という課題に対応するため、評価会議では今春(2019年3月)に、評価会議からメーカーに対して薬剤等供給への協力を要請する仕組み(薬剤アクセススキーム)を固めています。個別医療機関では、製薬メーカー等に薬剤等供給に関する交渉が難しいこともある点に鑑み、国・評価会議を通じて製薬メーカー等に働きかけるものです。近く、関連通知が厚労省から発出される見込みです(関連記事はこちら)。
なお、上記データを踏まえて評価会議構成員からは「患者申出療養が必要な患者であっても、十分に患者申出療養制度にアクセスできてないケースもありそうだ」(一度しか相談のなかった25件など)といった旨の指摘がなされました。厚労省保険局医療課の森光敬子課長は、「患者申出療養が必要となる患者を十分にピックアップできているか、医療関係者から聞き取りを行い、評価会議に報告する」考えを示しています。さらなる制度周知にも力を入れていく必要がありそうです。
このほか、9月12日の評価会議には、次のような事項が報告されています。
▽(7)「早期乳がん患者へのラジオ波熱焼灼療法」(国立がん研究センター中央病院)について、国立病院機構東京医療センターを追加実施医療機関とする
▽(1)「腹膜播種・進行性胃がん患者へのパクリタキセル腹腔内投与および静脈内投与ならびにS-1内服併用療法」について、実施期間を2020年10月まで延長する(治療継続中の患者がいるため)
▽(4)「髄芽腫、原始神経外胚葉性腫瘍または非定型奇形腫様ラブドイド腫瘍患者へのチオテパ静脈内投与、カルボプラチン静脈内投与およびエトポシド静脈内投与ならびに自家末梢血幹細胞移植術の併用療法」を取り下げる(計画した臨床試験が終了したため)
▽(5)「ジェノタイプ1型C型肝炎ウイルス感染に伴う非代償性肝硬変患者へのレジパスビル・ソホスブビル経口投与療法」を取り下げる(当該疾患治療薬(ソホスブビル/ベルパタスビル配合剤「エプクルーサ」)が保険適用されたため)
なお、(2)「心移植不適応な重症心不全患者への耳介後部コネクターを用いた植込み型補助人工心臓による療法」について、安全性確保のために患者適格基準を厳格化することが了承されていますが、松井健志構成員(国立がん研究センター生命倫理部長、生命倫理・医事法研究部長)から「患者適格基準において、『右室機能が重度に低下』など曖昧な表現があり、定量的な規定へ見直すべき」との指摘がありました。次回会合で改めて検討することになっています。

【関連記事】
遺伝子パネル検査に基づく抗がん剤の適応外使用想定した事前準備、国がんで進む―患者申出療養評価会議
患者申出療養評価会議からメーカーに「薬剤等供給」協力を要請する仕組み設ける―患者申出療養評価会議
早期乳がんのラジオ波熱焼灼治療を患者申出療養に導入、再発リスク説明等が必要―患者申出療養評価会議
遺伝子パネル検査で「適応外の抗がん剤治療」の可能性ある場合、迅速に治療開始できる準備進める―患者申出療養評価会議
「非代償性肝硬変へのハーボニー投与」、5種類目の患者申出療養に―患者申出療養評価会議
阪大病院での患者申出療養すべてで死亡含む重篤事象が発生、適切な患者選択を―患者申出療養評価会議
有効性・安全性の確立していない患者申出療養、必要最低限の患者に実施を—患者申出療養評価会議
心移植不適応患者への植込み型人工心臓DT療法、2例目の患者申出療養に―患者申出療養評価会議
2018年度改定に向けて、入院患者に対する「医師による診察(処置、判断含む)の頻度」などを調査―中医協総会
患者申出療養、座長が審議の場を判断するが、事例が一定程度集積されるまでは本会議で審議―患者申出療養評価会議
患者申出療養評価会議が初会合、厚労省「まずは既存の先進医療や治験の活用を」
患者申出療養の詳細固まる、原則「臨床研究」として実施し、保険収載を目指す―中医協
患者申出療養の提案受けた臨床研究中核病院、「人道的見地からの治験」の有無をまず確認―中医協総会
大病院受診、紹介状なしの定額負担など16年度から-医療保険部会で改革案まとまる
がん遺伝子パネル検査、「主治医が標準治療終了見込み」と判断した患者にも保険で実施可能―疑義解釈16【2018年度診療報酬改定】
がん遺伝子パネル検査、米国病理医協会(CAP)の第三者認定を受けた病院・検査機関で実施を―疑義解釈15【2018年度診療報酬改定】
がん遺伝子パネル検査等、保険診療上の留意事項を整理―厚労省
がんゲノム医療の推進に向け、遺伝子パネル検査を6月から保険収載―中医協総会(1)
遺伝子パネル検査の保険収載に向けた検討進む、C-CATへのデータ提出等を検査料の算定要件に―中医協総会(1)
新設される【がんゲノム医療拠点病院】要件固まる、3年で100人以上の治験等実績が「望ましい」―がんゲノム医療拠点病院等指定要件ワーキング
新設される「がんゲノム医療拠点病院」、中核病院なみの診療体制を敷きゲノム医療を自院で完結―がんゲノム医療拠点病院等指定要件ワーキング
がんゲノム医療、自分に最適な抗がん剤見つかる可能性は10-20%にとどまることなど説明を―がんゲノム医療推進コンソーシアム運営会議
がんゲノム医療を牽引する「中核拠点病院」として11病院を選定―がんゲノム医療中核拠点病院等指定検討会
がんゲノム医療を提供できる中核病院を、本年度(2017年度)中に7-10施設指定—がんゲノム医療懇談会
がんゲノム医療、当面は新設する「がんゲノム医療中核拠点病院」で提供―がんゲノム医療懇談会
がんとの闘いに終止符打つため、広く関係者が集い世界水準の「ゲノム医療」推進―厚労省




