医薬品のバーコード表示、表示義務付け項目では「100%」表示を達成―厚労省
2017.9.28.(木)
医薬品のトレーサビリティ(追跡可能性)を高めるために導入されている「バーコード表示」について、必須が義務付けられている項目では100%バーコード表示されている。ただし、2021年4月出荷分から表示が義務付けられている項目や、任意表示となっている項目については、バーコード表示割合は低い水準となっている―。
こういった状況が、厚生労働省が9月27日に公表した2016年の「医療用医薬品における情報化進捗状況調査」結果から明らかになりました(厚労省のサイトはこちら)(関連記事はこちら)。
トレーサビリティの確保や、取り違え防止に向け、バーコード表示を推進
医薬品に不純物が混入していた場合や新たな副反応が明らかになった場合などには製薬メーカーが対象商品を自主回収します(関連記事はこちら)。その際、医療機関などは当該医薬品の使用を差し控える必要がありますが、どれが対象医薬品なのかが明らかになっていなければいけません。さらに今年初めに問題となった偽造医薬品などが流通した場合に、医療機関などは備蓄医薬品が正規品か否かを判断しなければいけません(関連記事はこちらとこちらとこちら)。
こうした医薬品市販後のトレーサビリティ(追跡可能性)の確保や、医薬品の取り違え事故の発生防止、流通の効率化を促進するために、厚労省は「医療用医薬品へのバーコードの表示」を進めています。医療用医薬品の種類に応じて、バーコード表示の義務付けや、任意表示(できるだけ表示する)依頼をしています。さらに厚労省はバーコード表示が実際に行われているか否かを毎年調査し、その結果を公表しています。今般発表されたのは、2016年9月末時点の状況です。
製薬メーカーに対する調査結果を見てみましょう。 医薬品の種類や包装単位によって、必ずバーコード表示しなければいけない項目(必須表示項目)と表示しなくともよい項目(任意表示項目)とがあります。例えば、特定生物由来製品(ワクチン、遺伝子組換え製品など)では、すべての包装単位で▼商品コード▼有効期限▼製造番号または製造記号—のいずれも必須表示項目となっており(バーコード表示が義務付け)、一般の内用薬・外用薬・注射薬では、調剤包装単位における「有効期限」「製造番号または製造記号」は任意表示項目となっています。
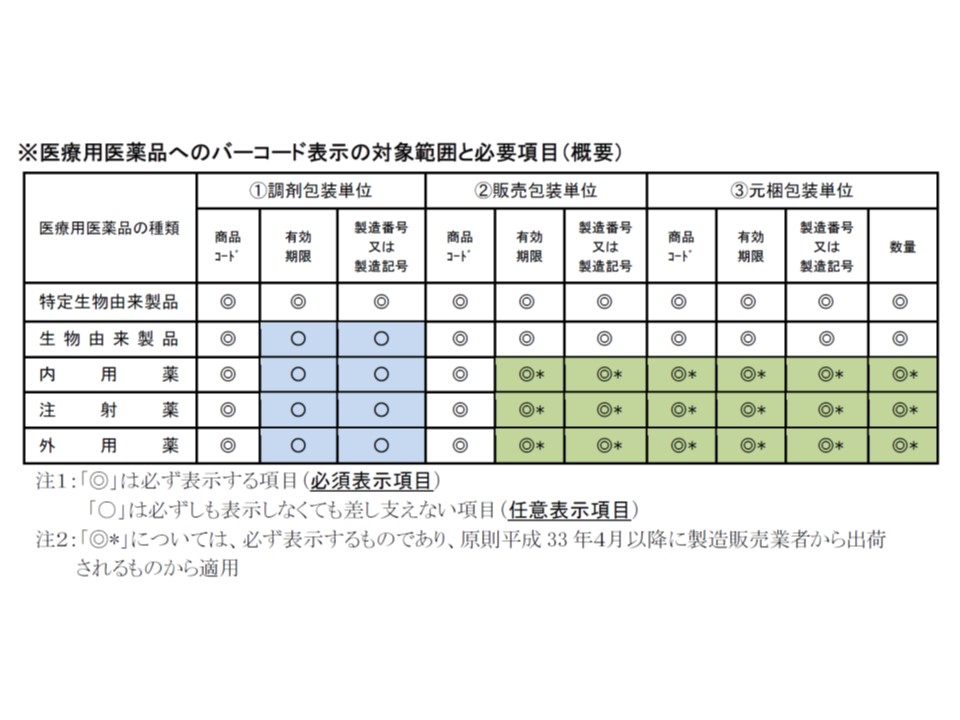
医薬品のバーコード表示は、医薬品の種類・包装単位によって表示が義務付けられているものと、任意となっているものとある
今般の調査では、すべての包装単位(▽調剤包装単位▽販売包装単位▽元梱包装単位)において「必須表示項目」についてバーコード表示割合が100%であることが分かりました。前年(2015年)調査では、内用薬の商品コード(97.5%)、外用薬の商品コード(95.6%)などで非表示がありましたが、改善が図られていることが分かります。
また生物由来製品(ヒト・動物由来の原料を用いた医薬品、特定生物由来製品以外)を除く内用薬・外用薬・注射薬では、販売包装単位における▼有効期限▼製造番号または製造記号―、元梱包包装単位における▼商品コード▼有効期限▼製造番号または製造記号▼数量―について、2021年4月出荷分(特別の事情のある場合には2023年4月出荷分)からバーコード表示が必須となり、現在は任意表示となっています。この点、2016年の9月末時点のバーコード表示割合は4.9-82.6%(前年は3.5-72.4%)にとどまっています。表示割合がとくに低いのは、外用薬における販売包装単位の「有効期限」「製造番号または製造記号」(いずれも4.9%)で、各メーカーにおける準備が急がれます。
さらに、任意表示となっている、生物由来製品・内用薬・外用薬・注射薬における▼有効期限▼製造番号または製造記号―の表示状況を見ると、0.0-21.8%(前年は0.0-18.5%)にとどまりました。とくに内用薬・外用薬において、バーコード表示割合が極めて低くなっています。任意表示とは言え、医薬品のトレーサビリティが重視される中では、製薬メーカーの積極的な取り組みに期待したいところです。
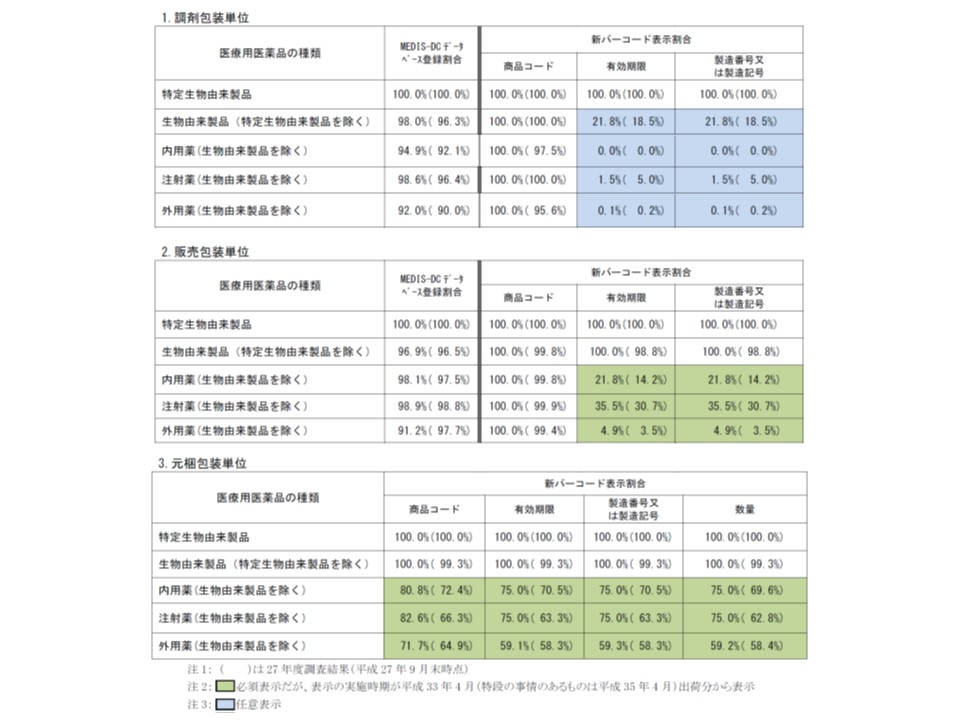
必須表示項目(色がついていない部分)については、すべての包装単位で100%を達成している
偽造ハーボニー、服用した患者はいない模様―厚労省
偽造ハーボニー、東京都でも見つかる―厚労省
ハーボニー錠の偽造品が流通、医薬品の譲り受けにおいては十分な注意を―厚労省





