既存品目からの置き換えとなる改良医療機器、機能区分をどう考えるか―中医協・材料専門部会
2017.9.14.(木)
Aという医療機器を改良したA1医療機器があり、医療現場ではAからA1への置き換えが進む場合、A1医療機器を新たな機能区分とすべきか、それとも既存機能区分の中に据え置き加算などで評価すべきか—。
9月13日に開催された中央社会保険医療協議会の保険医療材料専門部会では、こういった保険医療材料制度における「イノベーション評価」をテーマに議論が行われました。

9月13日に開催された、「第85回 中央社会保険医療協議会 保険医療材料専門部会」
改良・改善製品と、画期的製品とで評価の考え方を分ける方向か
保険医療材料においても、優れた機能を持つ製品の登場が心待ちにされており、改良・改善・画期的な製品開発を促すために、材料価格制度においては各種加算や機能区分の特例といった仕組みが用意されています。こうした仕組みをどう見直せばイノベーションが促進されるか、という点が2018年度の次期材料価格改定においても重要検討テーマの1つとなっています。
厚労省保険局医療課の古元重和企画官は、9月13日の材料専門部会で具体的な対応案を提示しました。
その1つが、「置き換わり製品に対する改良加算の運用」です。冒頭に示したような改良医療機器A1については、現在、既存の機能区分(A区分)とは異なる新機能区分(A1区分)が設定されています。すると、既存のA区分では後続品が出る機会が多いために、再算定により償還価格が大きくさがり、新規のA1区分との価格差が生じることで、「製品の置き換わりが十分に進まない」という問題が生じてしまいます。
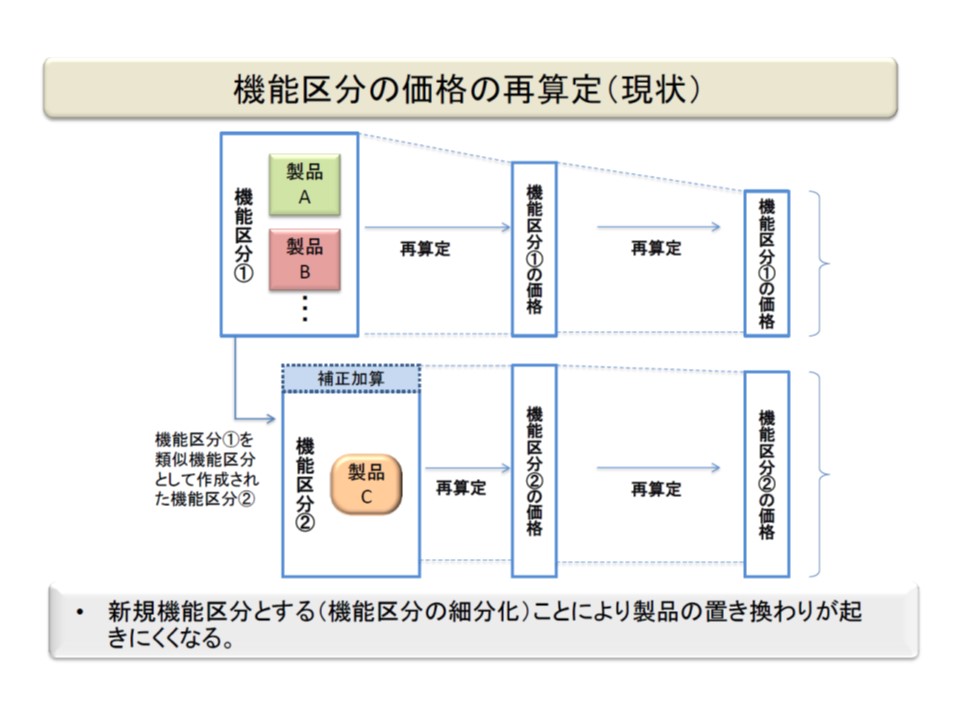
新規区分を増やしていった場合に生じる問題点
そこで古元企画官は、こうしたケースについては新機能区分を設定せず、既存A区分の中で「改良・改善について評価する仕組み」(例えば改良加算など)を検討してはどうかと提案しました。
この点、診療側の松本吉郎委員(日本医師会常任理事)は「改良品と画期的新製品とは分けて考えるべき」と述べ、厚労省提案に賛成しました。しかし、同じ診療側の万代恭嗣委員(日本病院会副会長)は、「A1医療機器に加算を設ければ、同じA区分の中で2つの価格が生じてしまう。現行どおり、新機能区分を設定するべき」と反論。診療側でも意見が分かれる状況になっています。
古元企画官は、画期的な新製品に対する「機能区分特例」(画期性加算・有用性加算を受けた機能区分が新設された場合などには、2回改定を経るまで新規機能区分を維持する仕組み。類似品の後続品出現に伴う価格低下を免れることが可能)は継続する考えを述べており、「改良・改善製品は既存区分の中で加算によって評価する、画期的製品は新規機能区分の特例によって評価する」という整理ができつつあるようです。上記論点と併せて、さらなる調整・議論が行われることになります。
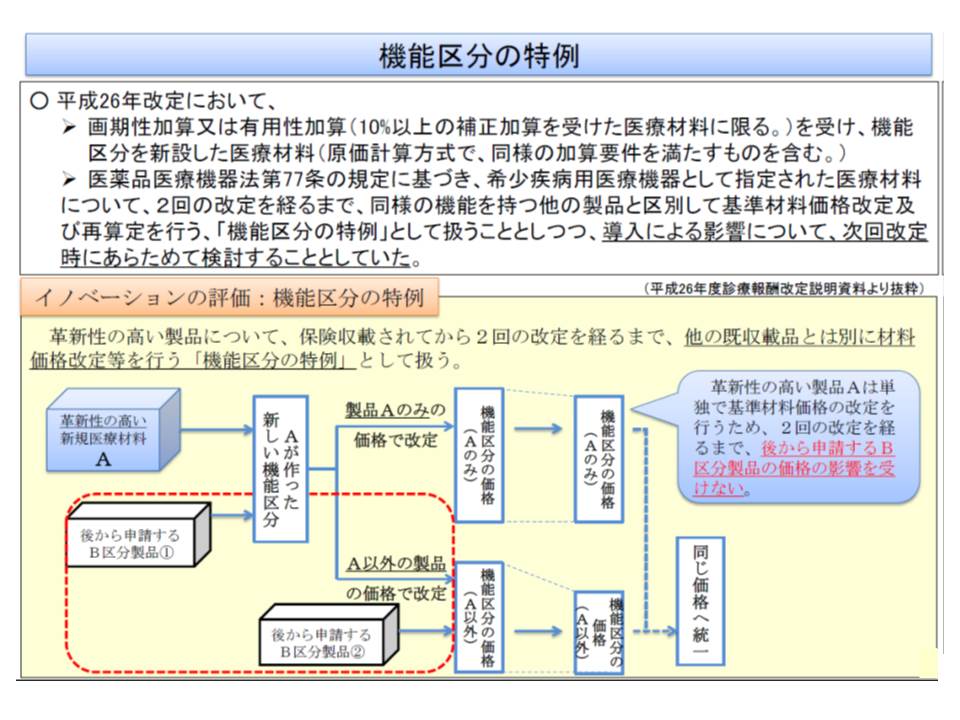
革新性の高い新規医療材料については、機能区分の特例(事実上の単独機能区分)を認め、最低でも4年間、高い価格を維持することが可能となる
新規収載時に「長期間経過後に効果出現」が分かる機器、効果出現後に再評価
ところで改良・改善などのイノベーションの効果が現れるまでに年単位の長期間がかかる医療機器もあります。こうした機器では、保険収載段階(つまり治験段階)で明確な効果を実証することは難しいため、「長期間経過し、効果が現れてから新規の機能区分を申請できる」ような仕組みを創設してほしいとの要望が医療現場から出されていました。
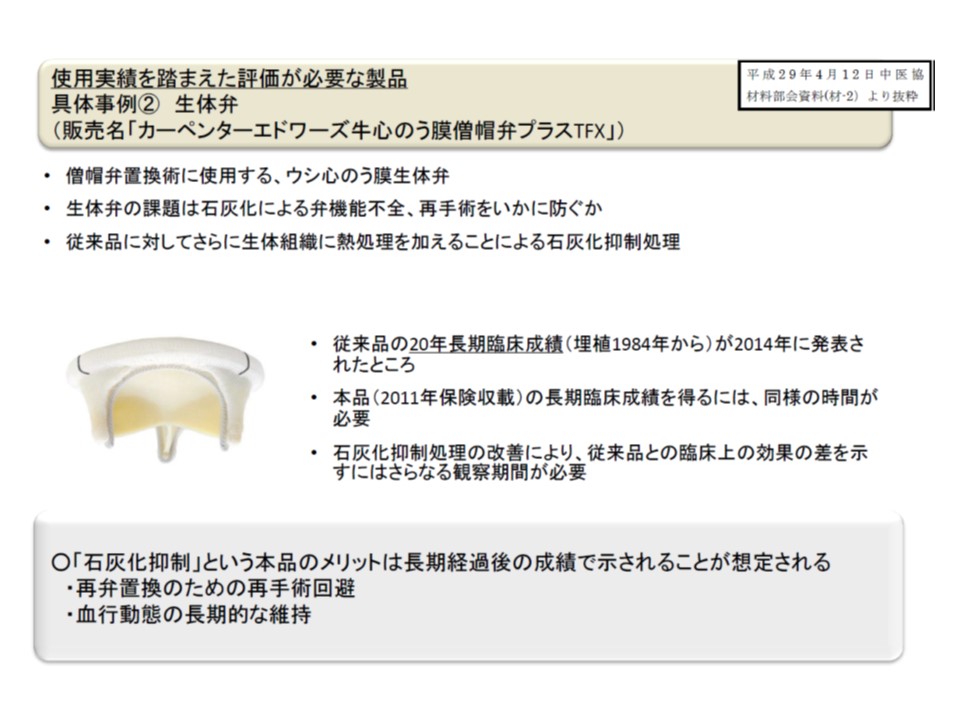
保険医療材料の中には、効果を十分把握できるまでに極めて長期間が必要なものが少なくない
古元企画官はこうした状況を踏まえ、「計画的にデータに基づき、保険適用後に再度、新機能区分の申請を行える」仕組み(再評価)を設ける考えを示しました。ただし、「新規に保険収載された時点」で、再評価の対象とするか否かを判断することになりそうです。このため、医療機器メーカー側で「本製品は改良改善の効果が出るまでに数年かかるので、再評価対象としてほしい」と保険適用希望する際に申請する必要があります。
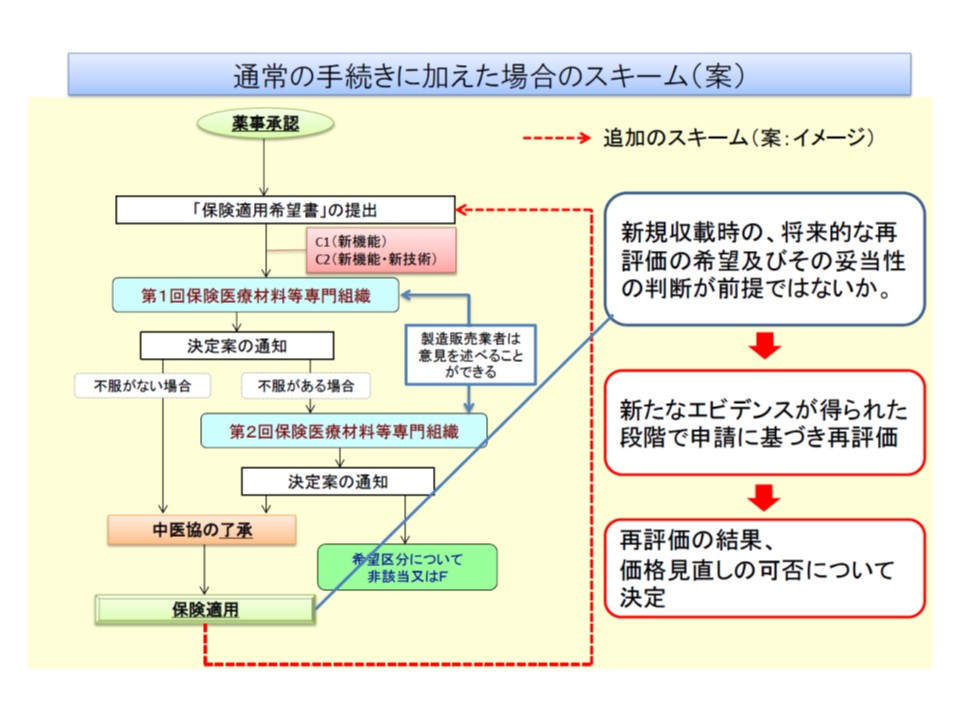
長期間経過で効果が生じるとわかる製品では、新規収載時に申請することで、効果出現後に再評価される仕組みを検討する
また古元企画官は、医薬品と同様に、医療機器においても「先駆け審査指定」された製品への加算創設も提案しています。世界に先駆けて日本で開発・承認される製品について、経済的な評価を行う仕組みで、まさに「イノベーションの推進」が期待されます。
しかし支払側の幸野庄司委員(健康保険組合連合会理事)は、「そもそも薬価制度における先駆け審査指定制度加算も『二重評価』のイメージがあり、違和感を覚える」と述べ、本提案に反対しています。ただし、医薬品・医療機器のいずれにおいても「優れた製品は高く評価する」というメリハリ付けが求められていることに鑑みれば、厚労省提案には一定の合理性があるとも考えられそうです。

先駆け審査指定制度の概要
このほか、▼医療上のニーズが高いために開発要請されたが、開発が進まない企業に対するディスインセンティブは2018年度改定では行わない▼既存製品よりも単純化した新規製品については類似機能区分に対して減額を行う▼迅速な保険導入に係る評価は条件を一部見直したうえで継続する—といった方針が古元企画官から示され、委員からは特段の反対意見は出されていません。


「医療ニーズが高い」との開発要請に応えない医療機器メーカーにペナルティなど与えるべきか—医療材料専門部会
材料価格制度も「皆保険の維持」や「イノベーション」目的に、2018年度に抜本改革―医療材料専門部会
薬価の毎年改定方針を決定、DPC点数表も毎年改定へ―厚労省
費用対効果評価、新規収載の医薬品なども対象に2018年度から本格導入へ―費用対効果評価専門部会



