高血圧症治療薬バルサルタン錠「AA」に発がん性物質混入の恐れ、メーカーが自主回収
2018.7.9.(月)
厚生労働省と東京都は7月6日、製薬メーカーのあすか製薬から高血圧症治療剤のバルサルタン錠20mg・40mg・80mg・160mg「AA」を自主回収する旨の報告があったことを公表しました(厚労省のサイトはこちら)。
中国で製造した原薬に発がん性物質が混入
医薬品医療機器等法(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律、旧薬事法)では、医薬品や医療機器の回収について厚生労働大臣(都道府県知事)に報告することを義務付けています(法第68条の11)。
今般、あすか製薬株式会社(東京都港区)が製造販売している高血圧症治療剤のバルサルタン錠について、中国で製造された原薬に発がん性物質「N-ニトロソジメチルアミン」が混入していることが分かり、製品使用が「重篤な健康被害または死亡の原因となり得るクラスI」にあたると判断。該当製品を自主回収することを決定しました。
回収対象は、2014年5月から2016年12月までに出荷された▼バルサルタン錠20mg「AA」(69万4360錠)▼バルサルタン錠40mg「AA」(371万3480錠)▼バルサルタン錠80mg「AA」(760万2040錠)▼バルサルタン錠160mg「AA」(54万1200錠)―で、製造番号等は下表のとおりです(なお当該製品は2018年4月1日時点で薬価基準から削除されている)。納入施設は1315施設で、うち1113施設は保険薬局です。
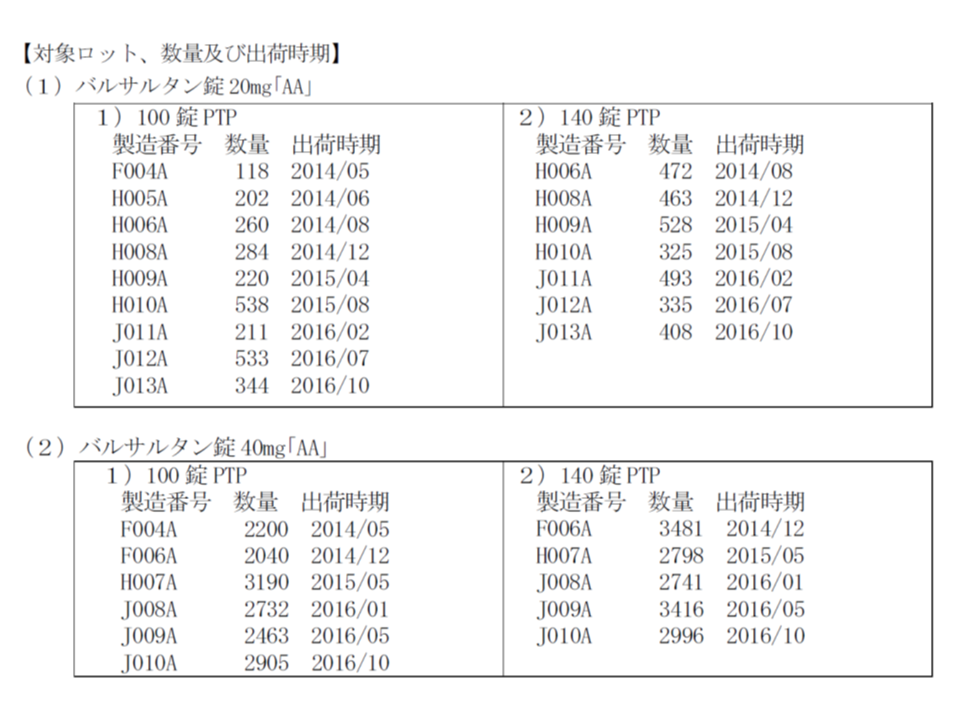
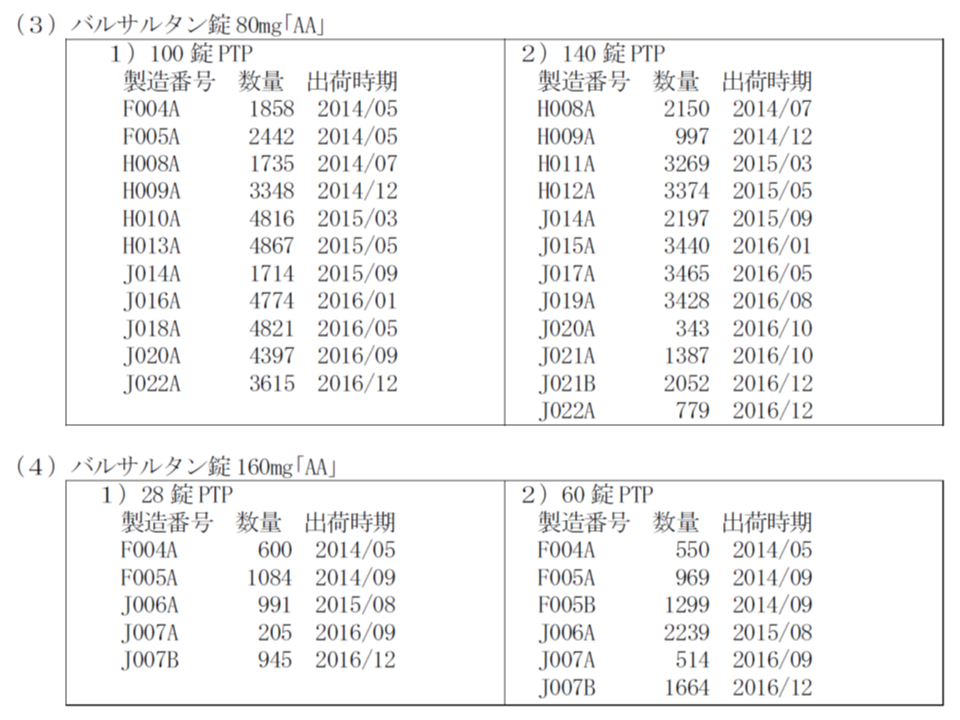
なお、7月6日時点で、健康被害は報告されていません。


【関連記事】
半自動除細動器「カーディアックレスキューRQ-5000」に不具合、メーカーが自主回収
血管造影用カテーテル「ハナコ・IRカテーテル」に不具合、メーカーが自主回収
小児用人工心肺「メラHPエクセランプライム」などに不具合、メーカーが自主回収
自動植込み型除細動器「Evera ICDシリーズ」の一部に不具合、メーカーが自主回収



