8番目の患者申出療養「遺伝子変異に対応した分子標的薬治療」、ニラパリブを対象薬剤に追加―患者申出療養評価会議
2022.6.24.(金)
1番目の患者申出療養である「腹膜播種・進行性胃がん患者へのパクリタキセル腹腔内投与および静脈内投与ならびにS-1内服併用療法」について、実施医療機関である東京大学医学部附属病院が「有効性が示唆される」との中間解析結果を報告したが、「患者の思いに応えられるよう、より科学的な評価が行える計画作成」などを行う必要があるのではないか—。
6月23日に開催された患者申出療養評価会議で、こういった議論が行われました。
なお、8番目の患者申出療養である「遺伝子パネル検査でactionableな遺伝子異常を有すると判断された固形腫瘍に対する『マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療』」において、武田薬品工業社の「ニラパリブ」(販売名:ゼジューラ)が対象薬剤に追加されるなどの計画見直しが行われます。

6月23日に開催された「第32回患者申出療養評価会議」
S-1+パクリタキセル併用療法、中間解析結果が示されたが・・・
患者申出療養は、傷病と闘う患者による「海外で開発された未承認(保険外)等の医薬品や医療機器を使用してみたい」という希望・申し出を起点に、当該医療技術(未承認の医薬品等)に一定の安全性・有効性があることを評価会議で確認した上で、保険診療との併用を許可するものです(2016年4月スタート)。
これまでに、次の12種類の患者申出療養が認められています(ただし「2」「4」「5」の技術はすでに終了。また後述するように今般「3」の技術も終了した)。
(1)腹膜播種・進行性胃がん患者への「パクリタキセル腹腔内投与および静脈内投与ならびにS-1内服併用療法」
(2)心移植不適応な重症心不全患者への「耳介後部コネクターを用いた植込み型補助人工心臓による療法」(関連記事はこちら)
(3)難治性天疱瘡患者への「リツキシマブ静脈内投与療法」(関連記事はこちら)
(4)髄芽腫、原始神経外胚葉性腫瘍または非定型奇形腫様ラブドイド腫瘍患者への「チオテパ静脈内投与、カルボプラチン静脈内投与およびエトポシド静脈内投与ならびに自家末梢血幹細胞移植術の併用療法」(関連記事はこちら)
(5)ジェノタイプ1型C型肝炎ウイルス感染に伴う非代償性肝硬変患者への「レジパスビル・ソホスブビル経口投与療法」(関連記事はこちら)
(6)進行固形がん(線維芽細胞増殖因子受容体に変化を認め、従来治療法が無効、かつインフィグラチニブによる治療を行っているものに限る)患者への「インフィグラチニブ経口投与療法」(関連記事はこちら)
(7)早期乳がん患者への「ラジオ波熱焼灼療法」(関連記事はこちら)
(8)遺伝子パネル検査でactionableな遺伝子異常を有すると判断された固形腫瘍に対する「マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療」(関連記事はこちらとこちら)
(9)HER2陽性の手術不能または再発の乳房外パジェット病患者に対する「トラスツズマブ エムタンシン(カドサイラ点滴静注用)静脈内投与療法」(関連記事はこちら)
(10)ROS1融合遺伝子陽性の進行性小児脳腫瘍患者に対する「エヌトレクチニブ(販売名:ロズリートレクカプセル)の経口投与療法」(関連記事はこちら)
(11)免疫グロブリンGサブクラス4自己抗体陽性難治性慢性炎症性脱髄性多発神経炎患者に対する「リツキシマブ追加投与療法」(関連記事はこちら)
(12)BRAFV600変異陽性の進行性神経膠腫を有する小児を対象とした「ダブラフェニブ・トラメチニブ併用療法」(関連記事はこちら)
6月23日の会合では、このうち「1」と「8」の技術が主な議題となりました。
まず「1」の技術は、腹膜播種陽性または腹腔細胞診陽性の胃がん患者に対し▼S-1(テガフール、ギメラシル、 オテラシルカリウムを配合した抗がん剤、胃がんや大腸がんへの効能・効果が認められている)の内服▼パクリタキセル(胃がんや乳がんへの効能・効果が認められている)の経静脈・ 腹腔内投与―を併用する技術です。有害事象発現状況や全生存期間、奏効割合、腹腔洗浄細胞診陰性化割合を評価項目として本技術の「有効性」や「安全性」の確認を行い、将来的な保険適用を目指すものです。
本技術は「腫瘍の進行が確認されるか、有害事象により継続困難となるまで反復(継続)する」こととされ、全111症例中「4症例」で継続されています(昨年(2021年)10月14日時点)。このため「技術の有効性・安全性の最終的な評価がいつなされるのか」は不明です(有害事象等が生じるまで治療が継続される)。
この点、患者申出療養評価会議では従前より▼安全性・有効性を適切に評価し、次のステップを考える時期に来ているのではないか▼最終解析がいつになるのか見通せないが、それが遅くなるほどエビデンス構築が遅くなり、かえって患者全体に不利益が生じる▼本技術は自由診療の中で「患者申出療養として実施されている技術である」として行われていると聞く。藁にも縋る思いの患者は、そうした謳い文句に踊らされてしまいかねない。患者申出療養についての解析がなされないために、安全性・有効性が確認されていない技術が、自由診療の中で実施されてしまうことは好ましくない—などの指摘があります。これを受け、実施医療機関である東京大学医学部附属病院では「中間解析」を実施し、今般、その概要が患者申出療養評価会議に報告されました。
中間解析では、▼重篤な有害事象が37件報告されたが、全て既知の有害事象であり治療関連死亡はなかった▼全生存期間中央値は19.6か月、腹膜播種陽性例では18.7か月、腹膜播種陰性・腹腔洗浄細胞診陽性例では37.0か月であった▼腹腔洗浄細胞診陰性化割合は70%、標的病変を有する8例における奏効割合は25%であった—などの結果を紹介。さらに「本療法で頻度が高く、治療の忍容性に影響する好中球数減少を抑えられたことが、治療の継続性と有効性につながった」「高齢者(75歳以上85歳未満)、PS 2症例、2か月以上の前治 療歴を有する症例等も登録可能とし、安全性確保のため担当医判断による投与量の調整を許容した結果、有害事象の発現を抑えることができた」と推測したうえで、「高齢者、PS不良例や既治療例等が含まれていたにもかかわらず先行研究と遜色ない結果が得られ、本療法の有効性が示唆されている」と結論づけています。
●東大病院による中間解析結果はこちら(患者申出療養評価会議資料)
この中間解析結果に対しては、▼実施医療機関サイドの「思い入れ」が強すぎないか、科学的な視点を重視した研究計画を新たに検討する必要があるのでないか(山口俊晴構成員:がん研究会有明病院名誉院長)▼自由診療で本技術が行われている。患者の気持ちに応えるためにも、科学的な視点に立ったエビデンスを構築すべき(天野慎介構成員:全国がん患者団体連合会理事長)―などの指摘が相次ぎました。
また五十嵐隆座長代理(国立成育医療研究センター理事長)は「この中間解析結果を一般の患者・国民が目にした場合、『本治療が有効である。優れている』と誤解する可能性があるのではないか」とも指摘しています。
福井次矢座長(卒後臨床研修評価機構理事・人材育成委員長)と厚生労働省とで、こうした意見も踏まえて、実施医療機関である東大病院に「科学的な解析の実施」「新たな臨床試験計画の検討」などを要請することになります。
もっとも患者申出療養には「患者の希望が起点になることから、一般的な治験などと異なり、患者の年齢や状態などを揃えることが難しく(治験に入れなかった患者が対象になるケースも多い)、症例数も限定される」という制約があります。このため「エビデンスの構築」を患者申出療養に期待することには限界もあり、今後の動きを注視していくことが必要です。
なお、治療継続中の患者もいることから(昨年(2021年)10月14日時点で4例)、「本技術の継続」が認められています。
遺伝子パネル検査に基づく患者申出療養での抗がん剤投与、対象薬剤に「ニラパリブ」追加
また3月18日の会合では、「8」の「遺伝子パネル検査でactionableな遺伝子異常を有すると判断された固形腫瘍に対する『マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療』」について、次のような実施計画の変更などが了承されました。
▽対象薬剤に、卵巣癌における初回化学療法後の維持療法などに効能効果が認められている「ニラパリブ」(販売名:ゼジューラ錠、ゼジューラカプセル、武田薬品工業社)を追加する
▽対象薬剤のうち、ALK融合遺伝子陽性の切除不能な進行・再発の非小細胞肺がん治療に効能効果が認められている「セリチニブ」(販売名:ジガディア錠、ノバルティスファーマ社)についてメーカーからの無償提供がストップされる(他のALKインヒビターが存在するため)
▽対象薬剤のうち、▼アフィニトール錠(一般名:エベロリムス、結節性硬化症への効能効果が認められている)▼テセントリク点滴静注(一般名:アテゾリズマブ、切除不能な進行・再発の非小細胞肺がんなどへの効能効果が認められている)―について、実施計画に沿って中間評価を行ったところ「有効性が示唆されており、安全性に問題がなさそうである」ことが確認されたことから、「患者申出療養としての継続」を認める
▽治療中止時検査のアローワンスについて「14日以内に実施することが望ましい」旨を明確化する
この技術は、遺伝子パネル検査の結果「未承認の分子標的薬(抗がん剤)が奏功する可能性がある」と判明したがん患者について、迅速に当該分子標的薬を用いた治療が可能となるように、予め国立がん研究センターで「患者申出療養の計画」を準備しておき、患者から希望があった場合に、すみやかに当該抗がん剤治療ん実施を可能とするものです(関連記事はこちらとこちら)。
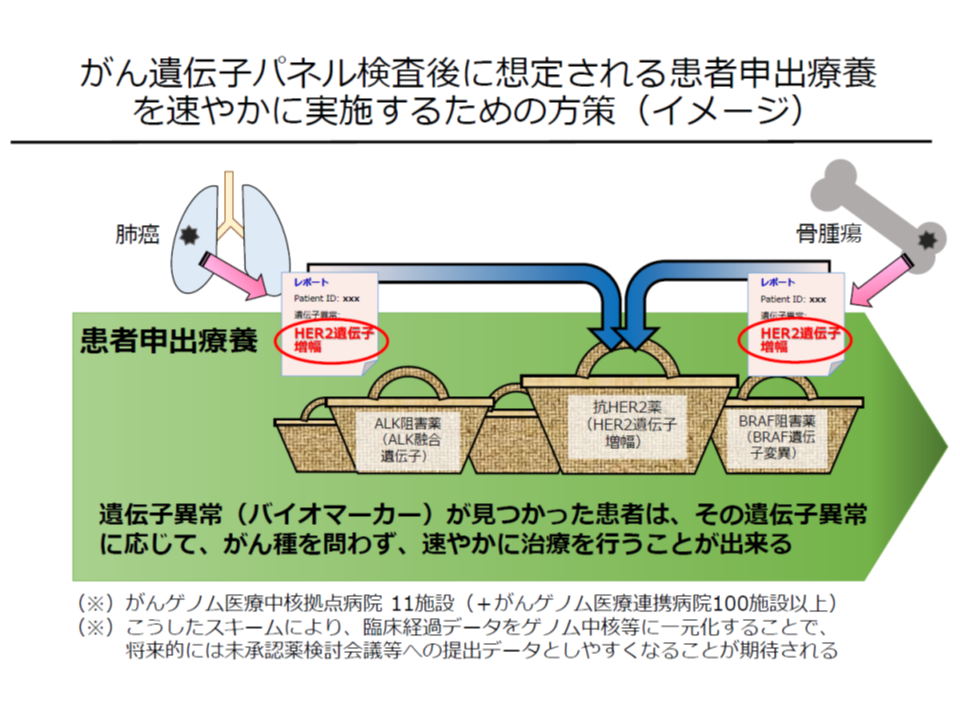
「適応外の抗がん剤」治療で効果があると判明した患者が、一刻も早く患者申出療養を申請できるよう、臨床研究中核病院で「下準備」を進めておく
通常の患者申出療養のルールに従えば、▼遺伝子パネル検査を行う→▼検査結果に基づいて病院の専門家会議(エキスパートパネル)で抗がん剤候補を明確化する→▼当該候補抗がん剤が未承認・適応外の場合、患者の希望を踏まえて「患者申出療養の計画」を作成する→▼患者申出療養評価会議に申請し、許可を待つ→▼許可を得て初めて当該抗がん剤投与が可能になる―という流れを踏まなければなりません。この場合、パネル検査・エキスパートパネル・計画作成に一定の期間がかかるため、「間に合わない」(抗がん剤投与前にがんが進行し、患者が不幸にもなくなってしまう)ケースが少なからず出ることも想定されます(遺伝子パネル検査は、標準治療を終えた患者、標準治療がない患者が対象となり、相当程度がんが進行していることが多い)。
そこで、患者の切なる希望に迅速に応えられるよう、「事前に『患者申出療養の計画』の雛形作成までを準備しておき、患者から『未承認・適応外の抗がん剤を使用したい』と要望があった場合に、速やかに抗がん剤投与が行える」仕組みが2018年11月の患者申出療養評価会議で創設されたのです。
さらに、遺伝子パネル検査・エキスパートパネルの結果を踏まえてから「この抗がん剤を患者申出療養の中で使用できるようにしてはどうか」と検討するよりも、事前に「多くの抗がん剤が患者申出療養の中で使用できる」とリスト化されていれば、より迅速に抗がん剤投与が可能になります。
今般の「ニラパリブ」追加で、より広範に「標準治療を終えた患者の思い」に応えることが可能になります。さらなる対象薬剤の追加に期待が集まります。
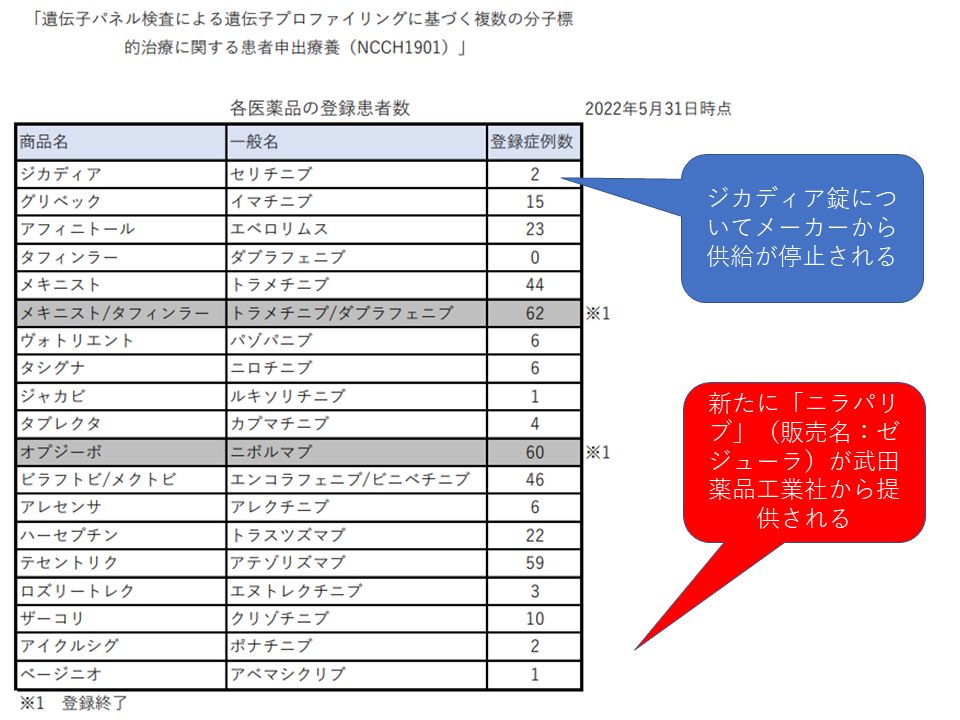
8番目の患者申出療養「遺伝子変異に対応した分子標的薬治療」において、メーカーから提供されている薬剤一覧
このほか6月23日の患者申出療養評価会議では、次の点も了承されています。
▽(7)の「早期乳がん患者へのラジオ波熱焼灼療法」について、有害事象などが生じていないことから継続を認めるとともに、都立駒込病院での実施を認める(同病院に入院する患者の希望を踏まえ、実施医療機関を追加した)
▽(3)の「難治性天疱瘡患者へのリツキシマブ静脈内投与療法」について、全症例の治療・経過観察が終了したため、患者申出療養としての実施を終了する
【関連記事】
耳介後部コネクター用いるDT療法の有効性に期待、遺伝子パネル検査による抗がん剤治療で対象薬剤追加―患者申出療養評価会議
患者申出療養から「初の薬事承認・保険適用」技術登場、抗がん剤「適応拡大」にも期待集まる―患者申出療養評価会議
8番目の患者申出療養「遺伝子変異に対応した分子標的薬治療」、リキッドバイオプシーも検査対象に追加―患者申出療養評価会議
12番目の患者申出療養、「BRAF V600変異陽性の小児神経膠腫」への抗がん剤併用療法を承認―患者申出療養評価会議
11番目の患者申出療養として、難病CIDPへのリツキシマブ追加投与療法を認める―患者申出療養評価会議
患者申出療養で実施される保険外の医療技術、しかるべき時期に安全性・有効性の評価が必要—患者申出療養評価会議
患者申出療養の計画変更を了承、ただし「野放図な期間延長」などは好ましくない―患者申出療養評価会議
10番目の患者申出療養として、小児脳腫瘍へのエヌトレクチニブ投与療法を認める―患者申出療養評価会議
小児がん患者も迅速に「適応外の分子標的薬」にアクセスできる環境を整備―患者申出療養評価会議(2)
乳房外パジェットへのカドサイラ投与、9番目の患者申出療養として導入―患者申出療養評価会議(1)
小児がん患者が「最適な抗がん剤にアクセスしやすい環境」の整備に向け、患者申出療養を拡充―患者申出療養評価会議
遺伝子パネル検査に基づく「適応外抗がん剤」使用、患者申出療養での実施を承認―患者申出療養評価会議
遺伝子パネル検査に基づく抗がん剤の適応外使用想定した事前準備、国がんで進む―患者申出療養評価会議
患者申出療養評価会議からメーカーに「薬剤等供給」協力を要請する仕組み設ける―患者申出療養評価会議
早期乳がんのラジオ波熱焼灼治療を患者申出療養に導入、再発リスク説明等が必要―患者申出療養評価会議
遺伝子パネル検査で「適応外の抗がん剤治療」の可能性ある場合、迅速に治療開始できる準備進める―患者申出療養評価会議
「非代償性肝硬変へのハーボニー投与」、5種類目の患者申出療養に―患者申出療養評価会議
阪大病院での患者申出療養すべてで死亡含む重篤事象が発生、適切な患者選択を―患者申出療養評価会議
有効性・安全性の確立していない患者申出療養、必要最低限の患者に実施を—患者申出療養評価会議
心移植不適応患者への植込み型人工心臓DT療法、2例目の患者申出療養に―患者申出療養評価会議
2018年度改定に向けて、入院患者に対する「医師による診察(処置、判断含む)の頻度」などを調査―中医協総会
患者申出療養、座長が審議の場を判断するが、事例が一定程度集積されるまでは本会議で審議―患者申出療養評価会議
患者申出療養評価会議が初会合、厚労省「まずは既存の先進医療や治験の活用を」
患者申出療養の詳細固まる、原則「臨床研究」として実施し、保険収載を目指す―中医協
患者申出療養の提案受けた臨床研究中核病院、「人道的見地からの治験」の有無をまず確認―中医協総会
大病院受診、紹介状なしの定額負担など16年度から-医療保険部会で改革案まとまる





