小児がん患者も迅速に「適応外の分子標的薬」にアクセスできる環境を整備―患者申出療養評価会議(2)
2020.5.22.(金)
お伝えしているとおり、5月21日に「患者申出療養評価会議」がオンライン形式で開催されました。
9番目の患者申出療養として、希少がんの1つである「乳房外パジェット病」患者に対するトラスツズマブ エムタンシン(販売名:カドサイラ点滴静注用)静脈内投与療法を認めたほか、▼小児がん患者が、迅速に最適な抗がん剤にアクセスできる環境の整備▼早期乳がん患者へのラジオ波熱焼灼療法の継続―などに関する議論が行われました。

5月21日に開催された、「第21回 患者申出療養評価会議」
目次
「小児の用法・用量」が存在しない分子標的薬、小児がん患者に投与を検討
患者申出療養は、2016年4月1日からスタートした新たな保険外併用療養制度(保険診療と保険外診療との併用を認める仕組み)です。患者の「海外で開発された未承認(保険外)等の医薬品や医療機器を使用した治療を受けたい」といった希望・申し出を起点に、評価会議で当該医療技術(未承認の医薬品等)の安全性・有効性を評価会議で確認し、保険診療との併用を可能とするものです。
5月21日の新技術を含めて、次の9種類の患者申出療養が認められています。
(1)腹膜播種・進行性胃がん患者への「パクリタキセル腹腔内投与および静脈内投与ならびにS-1内服併用療法」
(2)心移植不適応な重症心不全患者への「耳介後部コネクターを用いた植込み型補助人工心臓による療法」(関連記事はこちら)
(3)難治性天疱瘡患者への「リツキシマブ静脈内投与療法」(関連記事はこちら)
(4)髄芽腫、原始神経外胚葉性腫瘍または非定型奇形腫様ラブドイド腫瘍患者への「チオテパ静脈内投与、カルボプラチン静脈内投与およびエトポシド静脈内投与ならびに自家末梢血幹細胞移植術の併用療法」(関連記事はこちら)
(5)ジェノタイプ1型C型肝炎ウイルス感染に伴う非代償性肝硬変患者への「レジパスビル・ソホスブビル経口投与療法」(関連記事はこちら)
(6)進行固形がん(線維芽細胞増殖因子受容体に変化を認め、従来治療法が無効、かつインフィグラチニブによる治療を行っているものに限る)患者への「インフィグラチニブ経口投与療法」(関連記事はこちら)
(7)早期乳がん患者への「ラジオ波熱焼灼療法」(関連記事はこちら)
(8)遺伝子パネル検査でactionableな遺伝子異常を有すると判断された固形腫瘍に対する「マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療」(関連記事はこちらとこちら)
(9)HER2陽性の手術不能または再発の乳房外パジェット病患者に対する「トラスツズマブ エムタンシン(カドサイラ点滴静注用)静脈内投与療法」(関連記事はこちら)
5月21日の評価会議では、このうち(5)(7)(8)の3技術、さらに新規技術を主な議題としました((9)の技術に関しては別稿でお伝え済)。
まず(8)の「マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療」に関しては、「小児がん患者が、迅速に最適な抗がん剤にアクセスできる環境を整備する」ために、実施計画の見直し方向が承認されました。
ゲノム(遺伝情報)解析技術が進む中で、「Aという遺伝子変異の生じているがん患者にはαという抗がん剤投与が効果的、Bという遺伝子変異のある患者にはβとγという抗がん剤の併用投与が効果的である」などといった情報が明らかになってきており、こうしたゲノム情報に基づいたがん治療(がんゲノム医療)が我が国でも積極的に進められています(関連記事はこちらとこちらとこちらとこちら)。
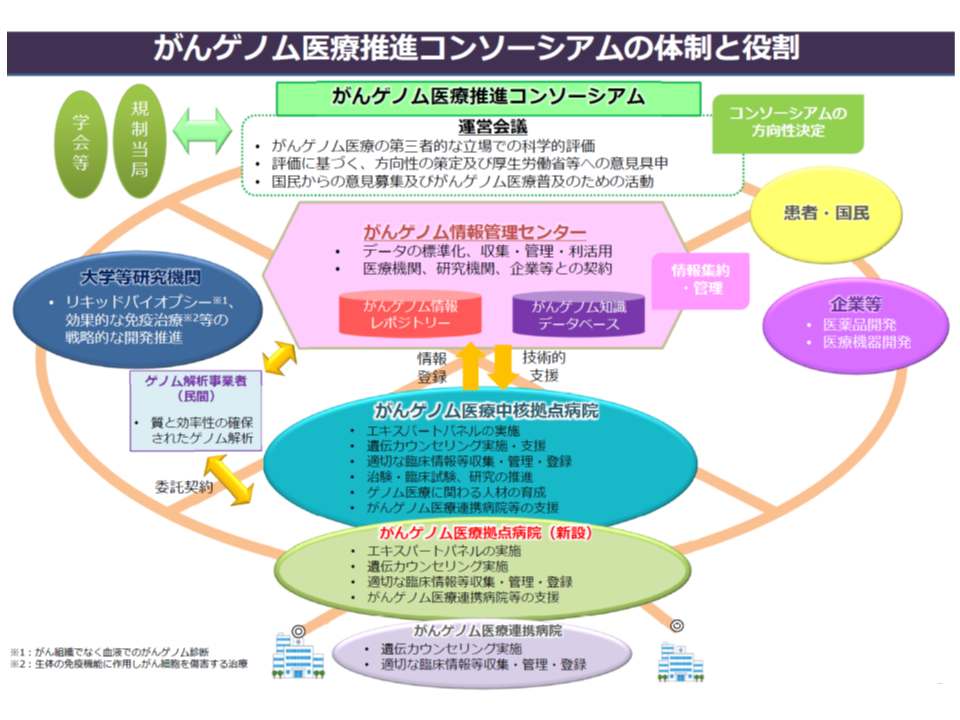
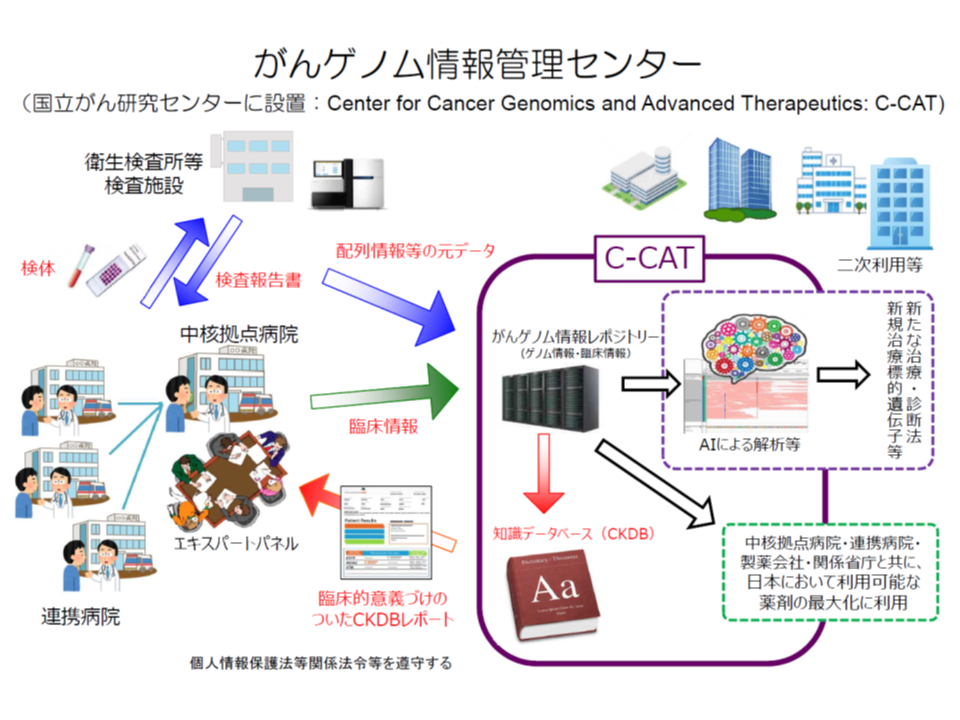
複数の遺伝子変異を網羅的に分析・検出する遺伝子パネル検査の保険適用が進められており(関連記事はこちらとこちらとこちらとこちら)、最適な抗がん剤を選択する下地が整ってきていますが、「選択された抗がん剤が適応外である」(Xがんについては有効性・安全性が確認され保険適用されているが、別のがんについては保険適用されていないなど)であるというケースが少なくありません。
医薬品の適応外使用は、原則として「完全に自費」となりますが、保険診療と保険外診療(適応外の抗がん剤使用など)を併用できる「患者申出療養」が有力かつ魅力的な選択肢となります。
もっとも、通常の患者申出療養制度では「実際に患者が現れてからプロトコルを立て、実施計画を作成する」ことになるため、実際の治療開始までに相当の時間がかかってしまいます(評価会議への申請までに時間が必要)。そこで、「一刻も早く、効果が期待される抗がん剤にたどり着きたい」という患者の思いに応えるために、(8)の「マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療」が患者申出療養として導入されました(昨年(2019年)9月)。事前に「いくつかの抗がん剤使用に基づく治療計画」を想定して準備し、その計画に該当する患者が現れた場合に、即座に治療を実施できるものです(関連記事はこちらとこちらとこちらとこちら)。
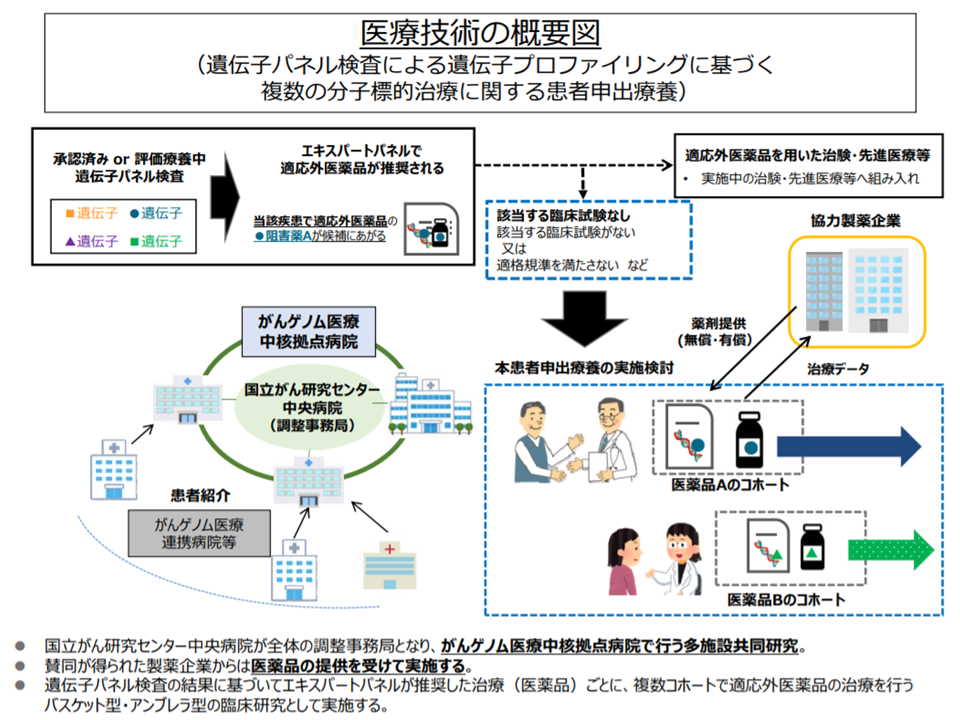
「マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療」の実施計画概要(1)(患者申出療養評価会議1 200213)
患者視点に立った極めて画期的な仕組みですが、対象患者は「16歳以上」に限定されていることから、「16歳未満の小児がん患者(対象外患者)が分子標的薬(抗がん剤)の適応外使用を希望した場合にも、迅速の治療実施できるよう、実施計画を見直す(対象患者の拡大)」ことが検討されています(関連記事はこちら)。
ここで1点、問題があります。分子標的薬(抗がん剤)の中には「小児への用法・用量が規定されていない」ものが少なくないのです。
(8)は「分子標的薬(抗がん剤)の適応外使用」をする技術であり、安全性や有効性が十分に確立されていません。このため実施計画の中では「当該薬剤の用法・用量については、添付文書に沿う」こととなっています。すると「小児への用法・用量が添付文書に規定されていない薬剤」は、現行の実施計画の中では使用できないこととになってしまいます。
これでは、小児がん患者の希望に応えることができないため、今般、(8)の技術を実施する国立がん研究センター中央病院では次のような実施計画見直し方針を立てました。
▽技術を小児に拡大する場合でも、原則として「小児に対する用法・用法が存在する薬剤」を対象とする(実施計画の中に「薬剤投与方法に関した規定」を残す)
▽ただし、「小児に対する用法・用量が存在しない薬剤」についても、海外のデータ等をもとに「小児に対する用法・用量を定めて、本技術の対象とする」ことについて製薬メーカーとの合意が得られる場合には、対象に含める
▼まず、すでに実施計画に規定される薬剤について「小児に対する用法・用量」の検証・検討を進める
▼今後、新たに実施計画に追加される薬剤については、追加の時点で「小児に対する用法・用量」の検証・検討を行う
5月21日の評価会議では、この見直し方針が承認され、今後、国立がん研究センター中央病院が示す「実施計画の具体的見直し内容」を改めて審議することになりました。
なお、当該技術を実施する医療機関として、▼国立がん研究センター東病院▼名古屋大学医学部附属病院▼北海道大学病院▼東北大学病院▼九州大学病院▼岡山大学病院―が追加されています。
小児がん患者に対する治療選択肢が大きく広がる可能性があり、今後の動きに期待が集まります。
ハーボニー錠の非代償性肝硬変患者への投与、1例ながらウイルス消失・肝機能改善
また(5)の「ジェノタイプ1型C型肝炎ウイルス感染に伴う非代償性肝硬変患者へのレジパスビル・ソホスブビル経口投与療法」については総括報告が行われました。
C型肝炎治療薬の「レジパスビル・ソホスブビル」(ハーボニー配合錠)は「非代償性肝硬変患者」には使用できませんが、申請時点で当該患者への治療薬が薬事承認されていなかったことから、患者申出療養として適応外使用することが認められました(関連記事はこちら)。
実施計画では「10例」に実施することとなりましたが、後に非代償性肝硬変患者にも投与可能なC型肝炎治療薬「ソホスブビル・ベルパタスビル」(エプクルーサ配合錠)が薬事承認・保険適用されたことから、実際に本技術が実施された患者は「1例のみ」となり、技術実施は終了しています。
当該患者について、▼C型肝炎ウイルスの消失と継続▼血清アルブミン値の正常化などの肝機能改善―が見られましたが、「1例のみ」であることから、ここから有効性・安全性を論じることは困難と総括報告されています。
ウイルスの消失や肝機能改善という極めて重要なデータが得られたことから、▼製薬メーカー等の臨床研究等を進める▼厚労省の専門家会議(医療上の必要性の高い未承認薬・適応外薬検討会議)で検討を進める―ことも期待されますが、上述のように非代償性肝硬変患者に投与可能な「エプクルーサ配合錠」が保険適用されているため、今後、どのように動くかは不透明です。
患者申出療養に相応しい実施計画・評価の在り方を検討へ
ところで、患者申出療養は「適応外薬の薬事承認・保険適用」を目指して臨床研究として実施されます。このために実施計画を定め、事後に有効性や安全性を評価することになります(関連記事はこちらとこちらとこちら)。
しかし、そもそも「患者の希望・申し出を起点とする仕組み」であることから、▼実施計画の作成(とりわけ症例数の計画など)▼事後の有効性・安全性の評価―が難しいという面もあります。
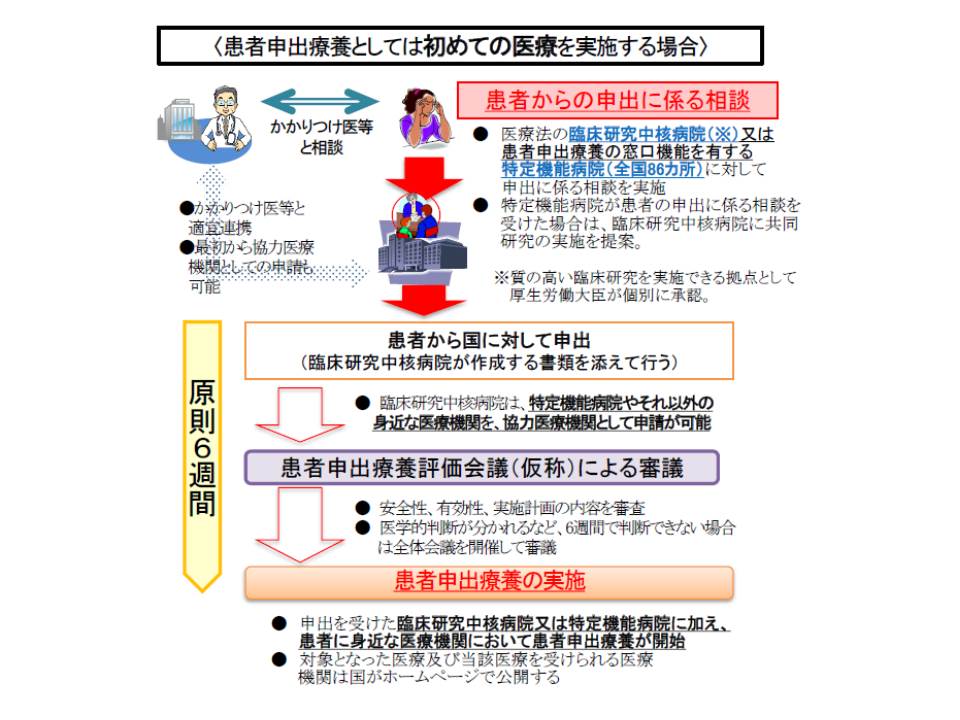
患者申出療養を初めて実施する場合、患者は国に対して申し出を行う(臨床研究中核病院が協力、支援)
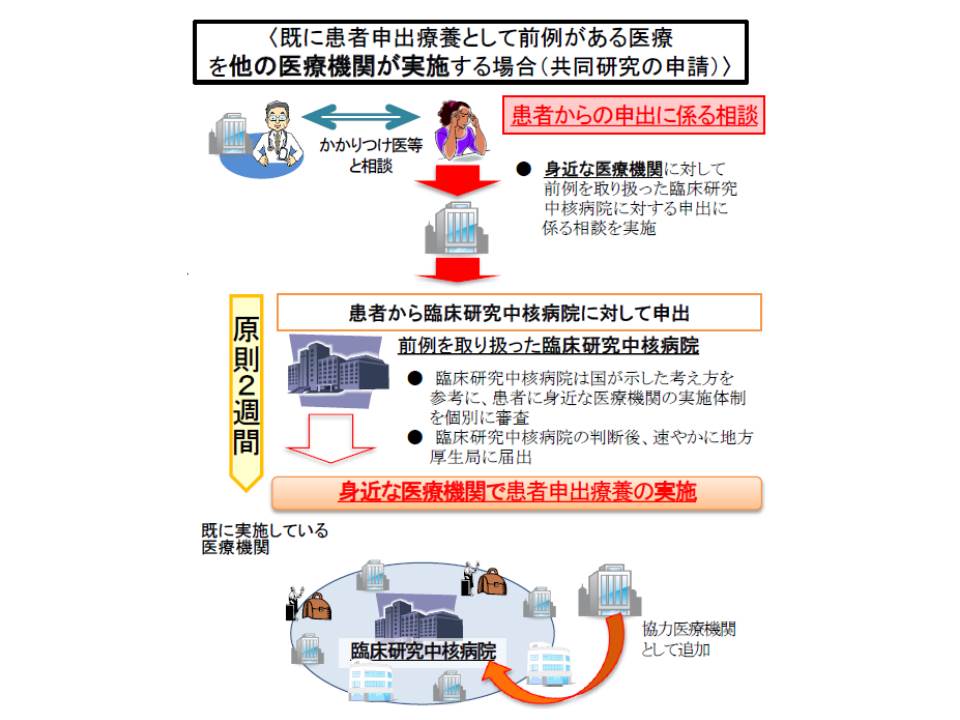
前例のある患者申出療養を実施する場合、患者は臨床研究中核病院に対して「実施を希望する医療機関」で当該医療を行いたいと申し出る
5月21日の評価会議でもこの点が改めて議論されました。上記の(5)技術(ハーボニー配合錠の投与)では、「有効性・安全性の可能性」が伺えますが(上村尚人構成員(大分大学医学部臨床薬理学講座教授)は「薬剤を投与しなければウイルス消失などは起こりえない」と指摘)、わずか1例のみのデータしかなく、「有効性・安全性を確認できない」という結論を出さざるを得ません。
このため、福井次矢座長(聖路加国際病院院長)や直江知樹構成員(名古屋医療センター名誉院長)、一色高明構成員(上尾中央総合病院心臓血管センター特任副院長)らは、「患者申出療養に相応しい実施計画や評価の在り方を検討していく」方向を示しました。例えば、第1フェーズでは「当該患者への効果や満足度」などを評価指標とし(症例数は実施計画に盛り込まない)、第2フェーズとして「治験等に結びつくデータが得られたか」などを評価指標とすることなども考えられそうです。今後の重要課題となるでしょう。
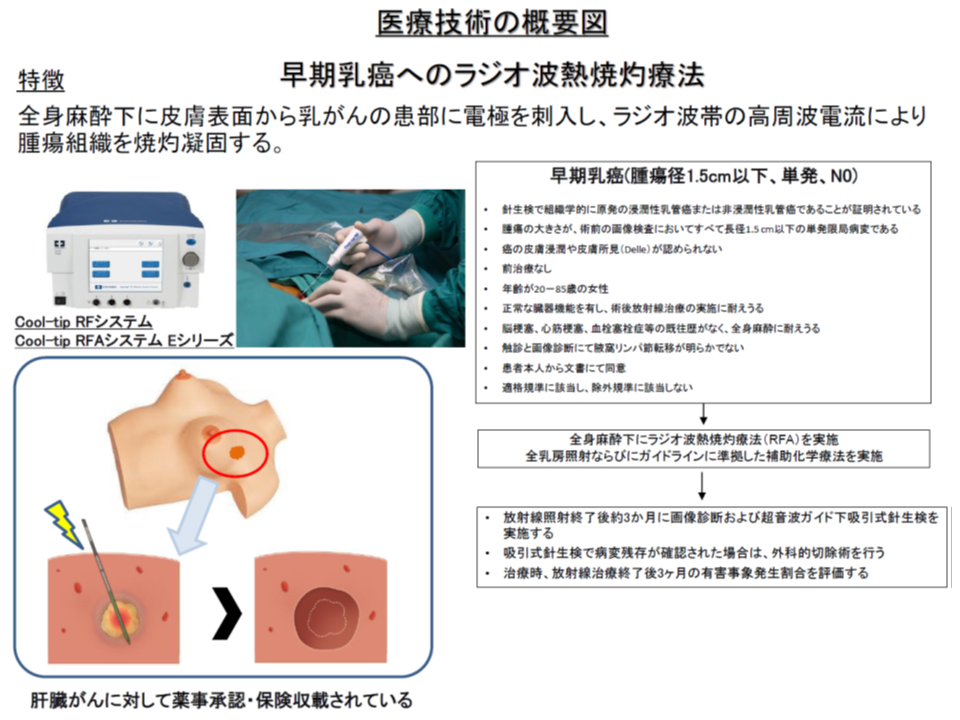
早期乳がん患者へのラジオ波熱焼灼療法、継続了承するも、再発リスクを検証
さらに(7)の「早期乳がん患者へのラジオ波熱焼灼療法」については、2019年3-4月の初年度に30症例(31乳房)に実施され、「特段の有害事象が認められず、順調に経過している」ことが国立がん研究センター中央病院から中間報告され、「継続実施」が承認されました。
ただし、本技術については、評価会議でも「標準治療(手術による病巣等の切除)に比べて、再発リスクが高いのではないか」との指摘があります(関連記事はこちら)。このため、半年ごとに中間報告を受け、継続の可否を判断することになっていますが、山口俊晴構成員(がん研究会有明病院名誉院長)や天野慎介構成員(全国がん患者団体連合会理事長)は「実施の症例のうち、どの程度にフォローアップを行ったのか、再発状況はどうなのか、などの詳細も定期的に報告してもらい、それを踏まえた評価が必要である」と要請。厚労省も「国立がん研究センター中央病院に詳細報告を求める」考えを示しています。
また、早期乳がんについては、上述のように標準治療(手術による病巣等の切除)が確立されていますが、「乳房の形状が大きく変わってしまう」という整容面でのデメリットがあります。このため「侵襲が少なく、整容面で大きなメリットがある本技術」(電極針を経皮的に乳房内の腫瘍に刺し、針から発生させたラジオ波で加熱・死滅させる技術)への希望の声が少なくないのですが、石川広巳構成員(日本医師会常任理事)は「他の患者申出療養は『代替法がない』ために認められているが、本技術は『代替法があるが、患者が整容面を踏まえて選択する』ものであり、性格が異なる。今後も、こうした整容面等に着目した患者申出療養が申請されると想定され、患者申出療養の在り方を改めて議論していく必要があるのではないか」と問題提起しています。
【関連記事】
乳房外パジェットへのカドサイラ投与、9番目の患者申出療養として導入―患者申出療養評価会議(1)
小児がん患者が「最適な抗がん剤にアクセスしやすい環境」の整備に向け、患者申出療養を拡充―患者申出療養評価会議
遺伝子パネル検査に基づく「適応外抗がん剤」使用、患者申出療養での実施を承認―患者申出療養評価会議
遺伝子パネル検査に基づく抗がん剤の適応外使用想定した事前準備、国がんで進む―患者申出療養評価会議
患者申出療養評価会議からメーカーに「薬剤等供給」協力を要請する仕組み設ける―患者申出療養評価会議
早期乳がんのラジオ波熱焼灼治療を患者申出療養に導入、再発リスク説明等が必要―患者申出療養評価会議
遺伝子パネル検査で「適応外の抗がん剤治療」の可能性ある場合、迅速に治療開始できる準備進める―患者申出療養評価会議
「非代償性肝硬変へのハーボニー投与」、5種類目の患者申出療養に―患者申出療養評価会議
阪大病院での患者申出療養すべてで死亡含む重篤事象が発生、適切な患者選択を―患者申出療養評価会議
有効性・安全性の確立していない患者申出療養、必要最低限の患者に実施を—患者申出療養評価会議
心移植不適応患者への植込み型人工心臓DT療法、2例目の患者申出療養に―患者申出療養評価会議
2018年度改定に向けて、入院患者に対する「医師による診察(処置、判断含む)の頻度」などを調査―中医協総会
患者申出療養、座長が審議の場を判断するが、事例が一定程度集積されるまでは本会議で審議―患者申出療養評価会議
患者申出療養評価会議が初会合、厚労省「まずは既存の先進医療や治験の活用を」
患者申出療養の詳細固まる、原則「臨床研究」として実施し、保険収載を目指す―中医協
患者申出療養の提案受けた臨床研究中核病院、「人道的見地からの治験」の有無をまず確認―中医協総会
大病院受診、紹介状なしの定額負担など16年度から-医療保険部会で改革案まとまる
がん遺伝子パネル検査、「主治医が標準治療終了見込み」と判断した患者にも保険で実施可能―疑義解釈16【2018年度診療報酬改定】
がん遺伝子パネル検査、米国病理医協会(CAP)の第三者認定を受けた病院・検査機関で実施を―疑義解釈15【2018年度診療報酬改定】
がん遺伝子パネル検査等、保険診療上の留意事項を整理―厚労省
がんゲノム医療の推進に向け、遺伝子パネル検査を6月から保険収載―中医協総会(1)
遺伝子パネル検査の保険収載に向けた検討進む、C-CATへのデータ提出等を検査料の算定要件に―中医協総会(1)
新設される【がんゲノム医療拠点病院】要件固まる、3年で100人以上の治験等実績が「望ましい」―がんゲノム医療拠点病院等指定要件ワーキング
新設される「がんゲノム医療拠点病院」、中核病院なみの診療体制を敷きゲノム医療を自院で完結―がんゲノム医療拠点病院等指定要件ワーキング
がんゲノム医療、自分に最適な抗がん剤見つかる可能性は10-20%にとどまることなど説明を―がんゲノム医療推進コンソーシアム運営会議
がんゲノム医療を牽引する「中核拠点病院」として11病院を選定―がんゲノム医療中核拠点病院等指定検討会
がんゲノム医療を提供できる中核病院を、本年度(2017年度)中に7-10施設指定—がんゲノム医療懇談会
がんゲノム医療、当面は新設する「がんゲノム医療中核拠点病院」で提供―がんゲノム医療懇談会
がんとの闘いに終止符打つため、広く関係者が集い世界水準の「ゲノム医療」推進―厚労省





