2018年度の材料価格改定、メーカー側は注文付けるも大枠は賛同―中医協・材料専門部会
2017.12.5.(火)
2018年度の保険医療材料価格制度改革に向けて、「保険収載後の使用実績に基づいた機能区分の再申請を可能とする」仕組みの導入方向は歓迎できるが、既存の収載品目についても一定期間、再申請を認めることとしてはどうか。また機能区分特例制度について、特例期間を現在の「2回の改定を経るまで」から「3回の改定を経るまで」に延長するなどの見直しを行ってはどうか―。
12月1日に開催された中央社会保険医療協議会の保険医療材料専門部会(材料専門部会)で、関係団体からこういった提案が行われました。

12月1日に開催された、「第89回 中央社会保険医療協議会 保険医療材料専門部会」
機能区分の特例、対象品目と期間の拡大を検討してはどうか
2018年度の診療報酬改定に合わせて、保険医療材料価格制度も見直しが行われます。これまでに材料専門部会では、厚生労働省から次のような提案が示されました。
(1)現在、保険適用時点から機能区分が固定されるが、長期間の使用を経た後に革新性などが明確になる品目もあり、「使用実績を踏まえて、保険収載後に再度、新機能区分を申請できる」仕組みを導入してはどうか(関連記事はこちら)

使用開始より数年から数十年経たなければ、有用性をきちんと評価できない医療機器もある(その1)

使用開始より数年から数十年経たなければ、有用性をきちんと評価できない医療機器もある(その2)
(2)新規の原理を有し、世界に先駆けて日本で早期開発される医療機器(先駆け審査指定)について、医薬品と同様に手厚く評価してはどうか(関連記事はこちら)
(3)従来品からの「置き換わり製品」については、機能区分を新たに作ることなく、既存の機能区分の中で「改良・改善について評価する」仕組みを設けてはどうか(関連記事はこちら)
(4)既収載品目を単純化した新規品目については、類似機能区分から減額する仕組みを導入してはどうか(関連記事はこちら)
(5)費用対効果評価を導入してはどうか(関連記事はこちら)

費用対効果評価の価格調整対象は、加算部分(類似薬効比較方式)のみとし、最大で90%の価格引き下げ(加算部分)が行われる
(6)内外価格差の是正に向けて、外国平均価格調整ルールを厳格化してはどうか(関連記事はこちら)
まず(1)の「使用実績を踏まえて、保険収載後に再度、新機能区分を申請できる」仕組みに対してメーカー側は、「歓迎」するとした上で、▼新規収載時に「後に使用実績データを収集し、新規機能区分を申請する」と宣言できる仕組みを設ける▼既に保険収載されている製品についても、一定期間「再度の申請を認める」などの配慮を行う—ことを要望しています。
また(3)の「置き換わり製品」については、▽安全性などの観点で比較的早期に置き換わりが完了する▽患者の病態など個別ニーズの違いなどから長期間かけて置き換わりが進む―場合など、さまざまなケースがあり「上市時点での予測には限界がある」として、▼置き換わりが実際に起こったかについては、個々の機能区分について一定期間後に検証する▼検証結果を踏まえて制度を適宜見直す―よう求めています。
さらに(5)の「費用対効果評価の導入」については、方向性を歓迎した上で、▼医療だけでなく、介護などへの影響も十分考慮してほしい▼機器の特性(製品サイクルが短い、医療従事者の技術習得に時間がかかるなど)からQALY推計が困難であることを踏まえた制度設計をしてほしい—と要望。具体的には、「倫理的・社会的影響等に関する観点で複数項目に該当する場合には、個別要素ごとに判断する(ICERを5%割り引き、高く評価する)のではなく、多角的に勘案する」「イノベーションも総合評価で勘案する」ことなどを求めました。
一方、(6)の「外国平均価格調整ルール厳格化」に関しては、激変緩和を求めるとともに、「すでに内外価格差はかなり縮小してきており、これ以上のルール変更は支持できない」との考えを示しています。
なお厚労省は「機能区分特例」について「継続」を提案しています。これは、「革新性の高い新規の医療機器については、2回の改定を経るまで、同様の機能を持つ他の製品と区別して、価格改定・再算定を行う」というルールで、2014年度に創設されました。
保険医療材料は、医薬品と異なり同じ機能区分の製品は同一の保険償還価格(材料価格)が設定されます。このため、画期的な医療材料を開発して高額な価格設定がなされても(製品A)、後に安価な類似品(製品B)が登場して同じ機能区分となった場合には、製品Aの価格は製品Bに引っ張られて低く見直されてしまい、メーカーの開発意欲を阻害してしまうという指摘がありました。そこで、画期的な製品について事実上の機能単独区分(機能区分の特例)を認めて、一定期間高価格を維持できるようにするものです。
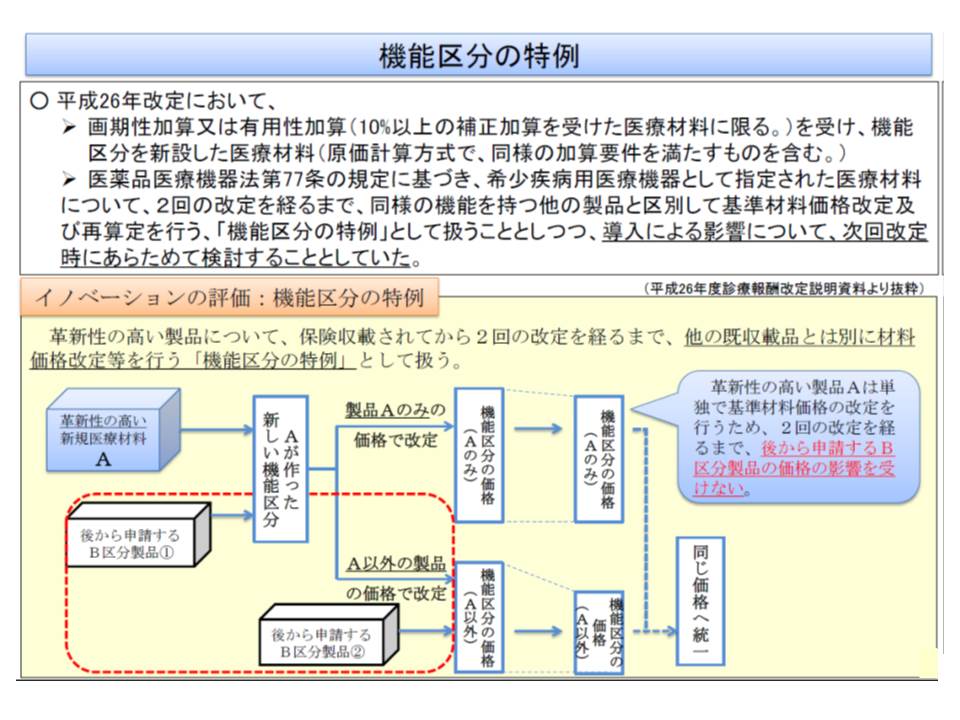
革新性の高い新規医療材料については、機能区分の特例(事実上の単独機能区分)を認め、最低でも4年間、高い価格を維持することが可能となる
厚労省はこの特例を継続する考えですが、メーカーサイドは、▼特例を受けられる期間を、現行の「2回の改定を経るまで」から「3回の改定を経るまで」に延長する▼現行の「10%以上の画期性加算または有用性加算を受けた品目」に加え、「10%以上の改良性加算を受けた品目」も対象とする—ことを要望しています。
この点、診療側の松本吉郎委員(日本医師会常任理事)は前者の要望について「価格が高止まりしてしまう」点にやや懸念を示しています。
【関連記事】
保険医療材料価格の内外価格差是正に向け、外国価格調整を強化—中医協・材料専門部会
既存品目からの置き換えとなる改良医療機器、機能区分をどう考えるか―中医協・材料専門部会
材料価格制度、イノベーション評価推進や市場拡大再算定導入などを検討—中医協・材料専門部会
「医療ニーズが高い」との開発要請に応えない医療機器メーカーにペナルティなど与えるべきか—医療材料専門部会
材料価格制度も「皆保険の維持」や「イノベーション」目的に、2018年度に抜本改革―医療材料専門部会
薬価の毎年改定方針を決定、DPC点数表も毎年改定へ―厚労省
費用対効果評価、新規収載の医薬品なども対象に2018年度から本格導入へ―費用対効果評価専門部会





