医療現場に必要不可欠な医薬品の価格下支え、対象拡大の方向―中医協・薬価専門部会
2017.10.30.(月)
長期間臨床現場で使用され「なくてはならない」存在になっている基礎的医薬品について価格の下支えが行われているが、対象を2018年度から若干拡大し、抗生物質を含有する点眼剤なども対象としてはどうか―。
10月27日に開催された中央社会保険医療協議会の薬価専門部会では、こういった考えが厚生労働省から提案されました。同日に開かれた保険医療材料専門部会では「2018年度から市場拡大再算定を導入することはせず、引き続き検討する」ことなどが固まっています。

10月27日に開催された、「第138回 中央社会保険医療協議会 薬価専門部会」
不採算に近い品目なども価格下支えし、安定供給を確保
医薬品は、薬価収載された後、2年に一度価格引き下げが行われるため、薬価収載されてから長期間が経過したものの価格は低くなります。しかし、医療現場になくてはならない医薬品について「あまりに低価格で(採算割するような)、製造販売が継続できない」事態が生じてはいけないため、薬価制度において(1)最低薬価(剤型に応じて価格の下限を設定する)(2)不採算品再算定(3)最低薬価になる前の薬価下支え(2016年度導入)―といった仕組みが準備されています。
このうち(3)は、「過去の不採算品再算定品目」と「古くから医療の基盤となっている病原生物に対する医薬品・医療用麻薬」を対象として「もっとも販売額が大きな銘柄に価格を集約して、その『薬価を維持』する」ものです。
製薬メーカー代表の立場で中医協に参画している加茂谷佳明専門委員(塩野義製薬株式会社常務執行役員)は、この仕組みについて該当メーカーから▼将来の不安が減少した▼採算割れに歯止めがかかった▼設備老朽化を改善できた—といった声が出ていることを報告。厚労省は、この仕組みを一部拡大してはどうかと提案しています。
具体的には、▼不採算または不採算に極めて近い状況が継続している分野も対象とする(過去数年の、薬価と実勢改革との乖離率を参考に判断)▼抗生物質を含有する点眼剤なども対象とする—という見直し案が、厚労省保険局医療課の中山智紀薬剤管理官から提示されました。
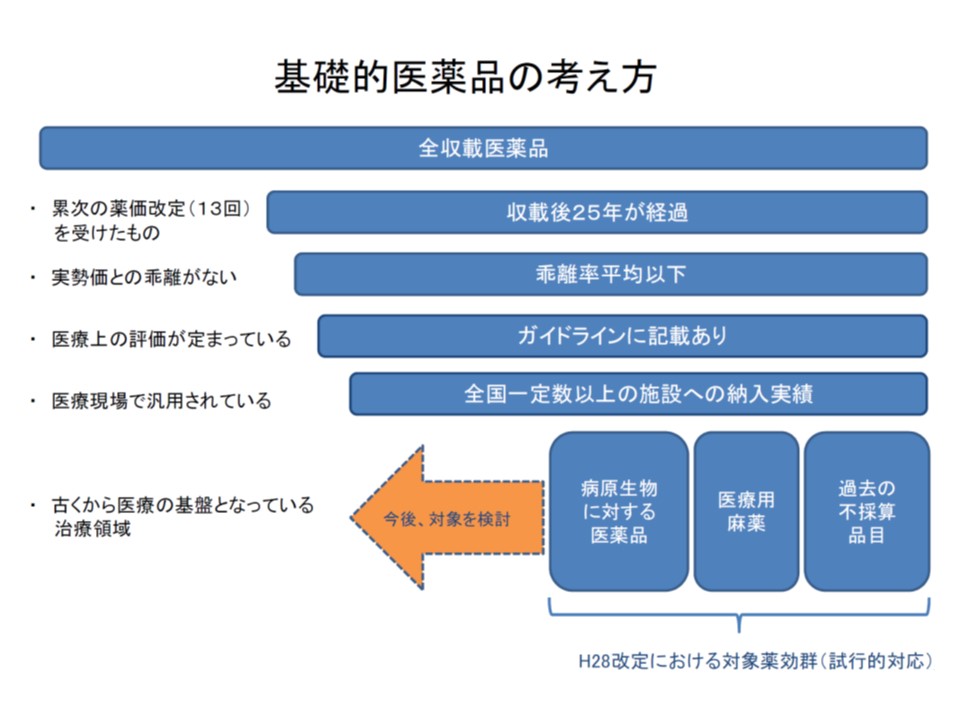
基礎的医薬品の薬価下支え制度(最低薬価になる前に)について、厚労省は対象品目の一部検討を考えている(橙色の矢印)
この点、診療側委員は「医療現場に必要不可欠な医薬品の継続供給が重要」とし、厚労省案に賛意を示しましたが、支払側の幸野庄司委員(健康保険組合連合会理事)は「対象品目がどの程度拡大されるのか、それを見なければ財政影響なども考慮できない。安易に賛否を表明できない」として、態度を保留しています。
なお幸野委員は「対象品目に長期収載品(先発品)と後発品とあり、長期収載品の販売額が大きな場合には、後発品価格も長期収載品価格に引き上げられるが、これは『長期収載品から後発品へのシフト』方針に反するのではないか」と指摘しましたが、中山薬剤管理官は「あくまで例外的な仕組みである」点に理解を求めています。
また、「用法用量変化再算定」について、「主たる効能・効果の変更に伴って、用法・用量が大幅に拡大した」品目も対象に加えてはどうかと中山薬剤管理官は提案しており、こちらには明確な反対意見は出されていません。

現在の用法・用量変化再算定、「効能の変化」に伴う用法・用量変化は対象になっていない
医療機器版の市場拡大再算定、2018年度には導入せず、引き続き検討
10月27日には中医協の保険医療材料専門部会も開催され、次の点について議論が行われました。

10月27日に開催された、「第86回 中央社会保険医療協議会 保険医療材料専門部会」
▽課題例:温度センサー付カテーテル電極は既存の機能区分では「電極数が3極以上6極未満」と定義されているが、新たに電極が7極の製品が開発された場合に、C1(心機能)として保険申請し、機能区分の定義を変更しなければならない(メーカーが新機能区分を欲していなくとも)
↓
【対応案】材料告示・算定方法告示に影響がないが、「定義、留意事項などの変更」のみが必要な品目に対応するため、保険適用区分を新設し(区分C3や区分Dを新設)、保険適用手続きを簡素化してはどうか

ごくわずかな仕様変更で、メーカーが既存機能区分への収載を希望するが、機能区分の定義に合致せず、C1(新機能)として保険適用申請しなければならないケースがある
▽課題例:【サイトケラチン19mRNA検出】検査について、従前の乳がん・胃がん・大腸がんに、新たに「非小細胞肺がん」が測定目的に追加された際、検査項目や方法に影響がないにもかかわらず、E3(改良項目)として保険適用せざるを得ない
↓
【対応案】算定方法告示への影響の有無について、保険適用評価区分により区別できるようE2(新方法)・E3(改良項目)の定義を見直し、手続きを簡素化してはどうか

測定項目や方法に変更がないが、測定対象のみが拡大された場合でもE3(改良項目)として保険適用が必要となり、手続きが煩雑である
▽課題:保険医療材料でも「市場拡大再算定」の仕組みが必要と指摘されている
↓
【対応案】「同一形状のまま適応が拡大され、市場が大幅に拡大する」ケースはなかなか想定できず、2018年度のルール設定は行わず、引き続き検討する
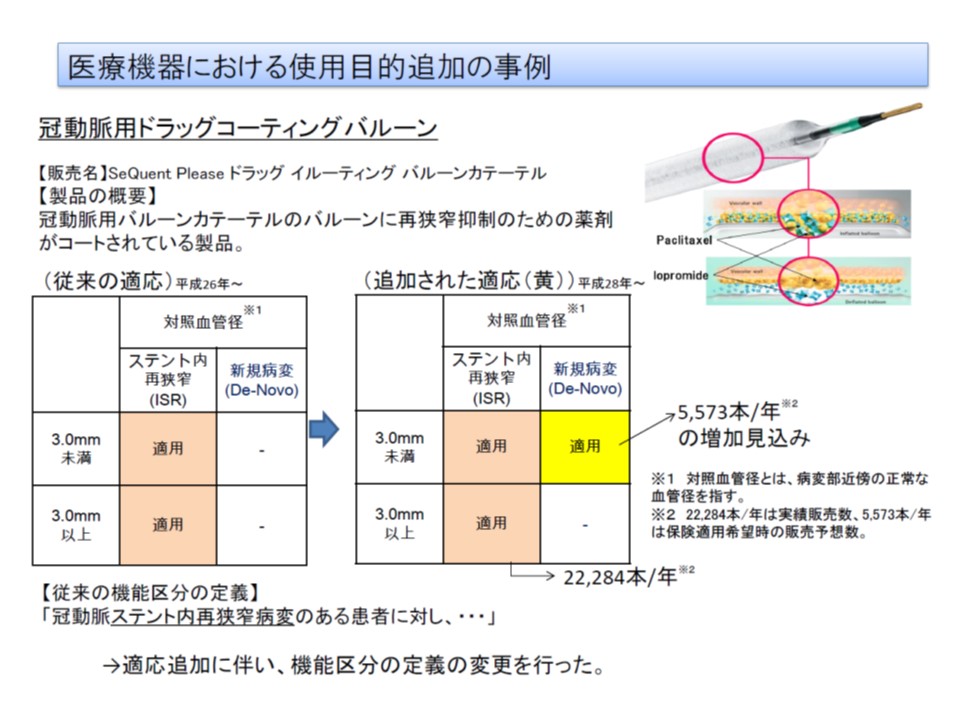
同一形状のまま適応が拡大となった、極めて稀なケース。ほとんどの場合には、適応拡大のためには形状変更などが必要となり、新機能区分設定となるので、市場拡大再算定のような仕組みの必要性は現状では低い
市場拡大再算定は、医薬であれば「成分などは変わらず、適応が拡大(例えば「メラノーマのみ」→「非小細胞肺がんに拡大」など)し、市場が大幅に増大する」ものについて、保険財政への影響などを考慮して薬価を引き下げるものです。しかし、医療機器では適応が拡大される場合には、形状・構造の変更(例えば、人工関節を「膝関節」用から「肩関節」用に拡大するには、形状・構造の見直しが必須)が必要となるケースがほとんどで、同一形状での拡大は極めて稀です。形状変更となれば、基本的に「新機能区分」が設定され、当該製品の状況を勘案した価格設定が行われるので、新ルール設定を急ぐ必要はないと考えられるのです。ただし、幸野委員や、診療側の松本吉郎委員(日本医師会常任理事)は「準備しておくにこしたことはない」と述べ、ルール設定を積極的に検討すべきと注文を付けています。
【関連記事】
新薬の原価計算方式、診療・支払双方が改めて問題点指摘—中医協・薬価専門部会
医薬品の画期性・革新性、薬価にどう公平に反映させていくべきか—中医協・薬価専門部会
新薬創出等加算、「産業構造の転換」促すため対象企業要件を厳格化してはどうか—中医協・薬価専門部会
長期収載品から後発品への置き換え促進、新薬創出等加算などとセットで議論すべき—中医協・薬価専門部会
製薬メーカーが新薬創出等加算の継続を強く要望―中医協・薬価専門部会
後発品の薬価、現在3区分の価格帯をさらに集約していくべきか-中医協・薬価専門部会
原価計算方式における薬価算定、製薬メーカーの営業利益率などどう考えるか-中医協・薬価専門部会
薬価調査において、医療機関に対する価格調査は継続すべきか-中医協・薬価専門部会
中間年の薬価見直し、対象品目の基準(乖離率など)を事前に示しておくべきか―中医協・薬価専門部会
新薬の薬価設定で、比較対象薬(類似薬)に付加された補正加算をどう考えるべきか―中医協・薬価専門部会
材料価格制度も「皆保険の維持」や「イノベーション」目的に、2018年度に抜本改革―医療材料専門部会
薬価の外国平均価格調整、診療・支払両側から「米国価格は参照対象から除外すべき」との指摘―中医協・薬価専門部会
効能追加などで市場拡大した医薬品の薬価再算定、対象や引き下げ方法の議論開始―中医協薬価専門部会
薬価の毎年改定方針を決定、DPC点数表も毎年改定へ―厚労省
既存品目からの置き換えとなる改良医療機器、機能区分をどう考えるか―中医協・材料専門部会
材料価格制度、イノベーション評価推進や市場拡大再算定導入などを検討—中医協・材料専門部会
「医療ニーズが高い」との開発要請に応えない医療機器メーカーにペナルティなど与えるべきか—医療材料専門部会
材料価格制度も「皆保険の維持」や「イノベーション」目的に、2018年度に抜本改革―医療材料専門部会





