小児がん患者、遺伝子パネル検査後に「効果が期待される未承認・適応外の分子標的薬」へ迅速投与できる仕組み検討―患者申出療養評価会議
2023.3.20.(月)
小児がん患者が、遺伝子パネル検査を経て、効果が期待される「適応外、未承認の抗がん剤」により円滑にアクセスできるような仕組みを、患者申出療養も併用して設けてはどうか―。
3月17日に開催された患者申出療養評価会議で、こういった議論が行われました。
また、同日には15番目の患者申出療養として「胸部悪性腫瘍に対する経皮的凍結融解壊死療法」を議論しました、一部確認すべき事項があり継続審議となっています。

3月17日に開催された「第38回 患者申出療養評価会議」
小児の抗がん剤選択、既存の「成人用の患者申出療養の仕組み」ではなかなか難しい
ゲノム(遺伝情報)解析技術が進み、「Aという遺伝子に変異の生じたがん患者にはαという抗がん剤を、Bという遺伝子変異のある患者にはβとγという抗がん剤を併用投与することが効果的である」などといった知見が徐々に明らかになってきています。こうしたゲノム情報に基づいた最適な治療法の選択ができるようになれば、個々のがん患者に対して「効果の低い治療法を避け、効果の高い、最適な治療法を優先的に実施する」ことが可能となり、▼治療成績の向上▼患者負担の軽減(身体的、経済的)▼医療費の軽減―などにつながります。
我が国でも、多くの遺伝子変異を一括確認できる「遺伝子パネル検査」の保険適用が進み(関連記事はこちらとこちら)、(1)患者の同意を得た上で、患者の遺伝子情報・臨床情報を、「がんゲノム情報管理センター」(C-CAT、国立がん研究センターに設置)に送付する → (2)C-CATで、送付されたデータを「がんゲノム情報のデータベース」(がんゲノム情報レポジトリー・がん知識データベース)に照らし、当該患者のがん治療に有効と考えられる抗がん剤候補や臨床試験・治験などの情報を整理する → (3)がんゲノム医療中核拠点病院・がんゲノム医療拠点病院の専門家会議(エキスパートパネル)において、C-CATからの情報を踏まえて当該患者に最適な治療法を選択し、これに基づいた医療を提供する―という【がんゲノム医療】の実施が始まり、充実・拡大が図られています。
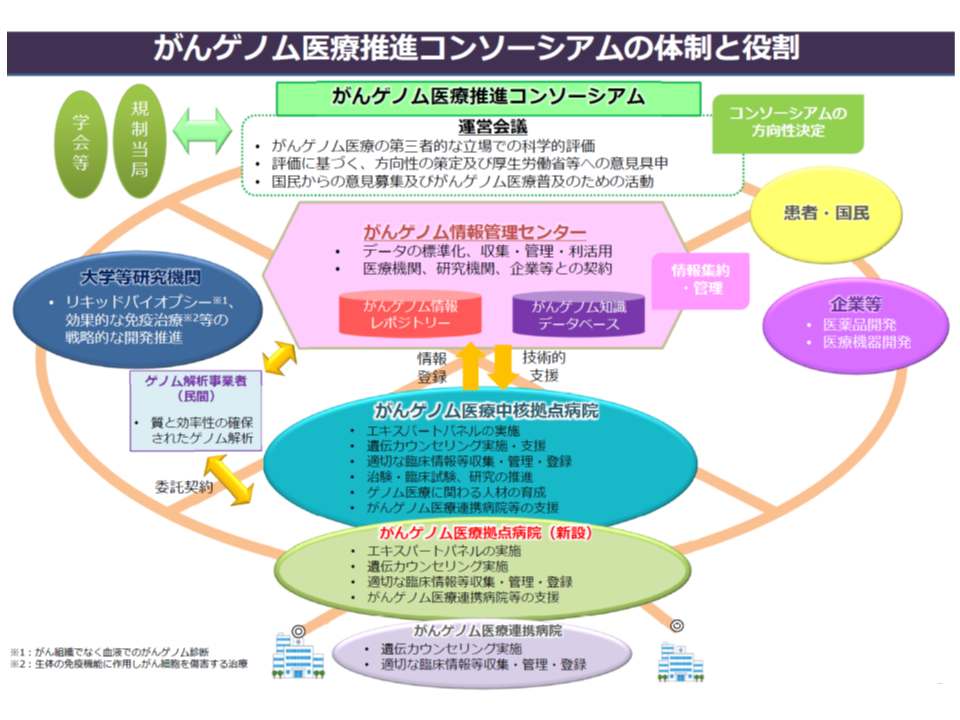
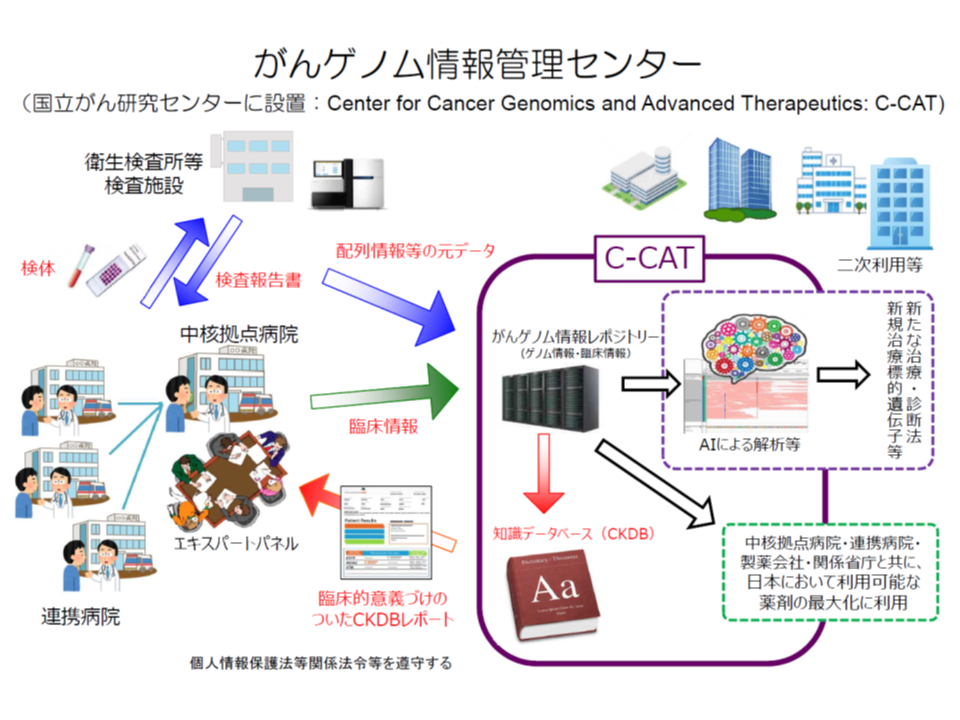
ただし、遺伝子パネル検査により有効な抗がん剤が見つかる可能性は現時点では1割弱にとどまっており(関連記事はこちら)、また「有効な抗がん剤が見つかったが、保険適応外(当該がん種への効能効果が薬事承認されていない)・未承認(本邦での使用が薬事承認されていない)であった」というケースも少なくありません。
適応外・未承認の医薬品を使用する場合「一連の治療すべてが自己負担」となるのが原則です(混合診療の禁止)が、患者負担が極めて重くなってしまうため、患者の経済的負担を軽減し、より円滑に「未承認・適応外の抗がん剤にアクセス」可能つる方法の1つとして「患者申出療養」制度が設けられています。
具体的には、2019年秋に8番目の患者申出療養として「遺伝子パネル検査でactionableな遺伝子異常を有すると判断された固形腫瘍に対する『マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療』」が設けられました(関連記事はこちら)。
患者から「我が国では保険診療の中で実施できない●●技術を受けたい」との申し出があり、▼かかりつけ医との相談▼臨床研究中核病院への相談▼臨床研究中核病院における診療計画(プロトコル)作成―などを経て、国への申請が行われるまでには、少なくとも「数か月」かかってしまうのが実際です。
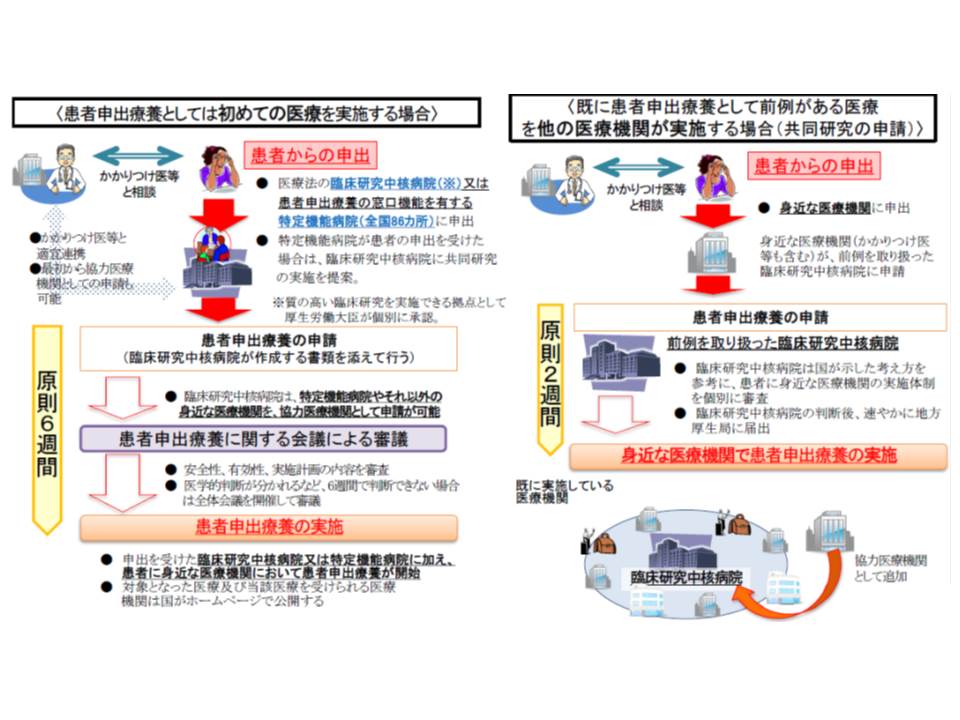
前例のない医療技術については原則6週間で保険外併用の可否を判断し、前例のある医療技術については原則2週間で「身近な医療機関での実施」の可否を判断する
遺伝子パネル検査の対象は、現在「標準治療を終えた患者」であり、こうした数か月の手続き期間に容体が急変し、最悪の場合亡くなってしまう可能性もあり、通常の患者申出療養を活用したのでは「間に合わない」こともありうるのです。
そこで、▼事前に国立がん研究センターで、いわば『患者申出療養の計画』の雛形作成までを準備しておく▼多くの抗がん剤(分子標的薬)を使用可能とする手続きを踏んでおく—ことで、実際に患者から「未承認・適応外の抗がん剤を使用したい」と要望があった際、速やかにこの仕組みに沿って「未承認・適応外の医薬品を患者申出療養の中で使用できる」ような体制が整えられたのです(通常診療部分は医療保険を使って1-3割負担、未承認・適応外の医薬品費などは保険外の自己負担)。
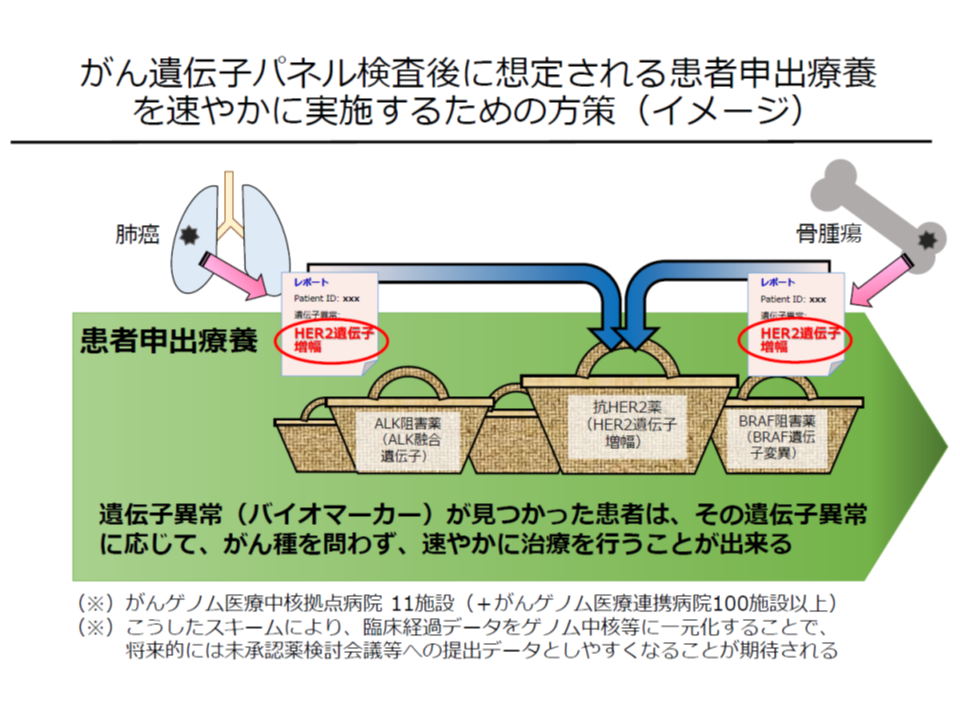
「適応外の抗がん剤」治療で効果があると判明した患者が、一刻も早く患者申出療養を申請できるよう、臨床研究中核病院で「下準備」を進めておく
すでに多くの患者が未承認・適応外薬にアクセスし、また対象薬剤の範囲もメーカーの協力で進んでいます(関連記事はこちら)。
しかし、小児がん患者・家族から「小児がん患者で、患者申出療養評価会議が使いにくい」との声が出ています。
本技術については、小児がん患者も迅速に「適応外の分子標的薬」にアクセスできる環境を整備するために、例えば「『小児に対する用法・用量が存在しない薬剤』についても、海外のデータ等をもとに『小児に対する用法・用量を定めて、本技術の対象とする』ことについて製薬メーカーとの合意が得られる場合には対象に含める」などの実施計画改善が図られてきています(関連記事はこちら)。しかし「個々の医療機関が海外論文などを踏まえて、メーカーと薬剤供給交渉を行うことなどは困難である」という現実があるようです。
こうした状況を踏まえ、国立がん研究センター中央病院小児腫瘍科の小川千登世科長が「小児に特化した、未承認・適応外の抗がん剤を患者申出療養を活用して円滑に使用可能とする」仕組みを検討していることが3月17日の患者申出療養評価会議で厚生労働省から報告されました。
上述の「成人の仕組み」と同様に、▼事前に国立がん研究センターで、いわば『患者申出療養の計画』の雛形作成までを準備しておく▼抗がん剤(分子標的薬)について、小児への用法・用量を海外データも踏まえて研究・検討・設定しておく—ことで、小児がん患者が、遺伝子パネル検査後に速やかに「適応外・未承認の抗がん剤(分子標的薬)にアクセスできる」環境を整えておくイメージです。
すでにAMED(⽇本医療研究開発機構)からの研究予算が確保されており、小川科長は「来年(2024年)早々に、実際に小児がん患者へ未承認・適応外の抗がん剤(分子標的)を投与できるようにしたい」と考えています。このためには「今秋(2023年秋)までには患者申出療養評価会議や中央社会保険医療協議会で具体的な仕組みを確立・承認しておく」ことが必要となります。

「小児がんのドラッグ・ラグに係る患者申出療養」1(検討中である点に留意)(患者申出療養評価会議1 230317)
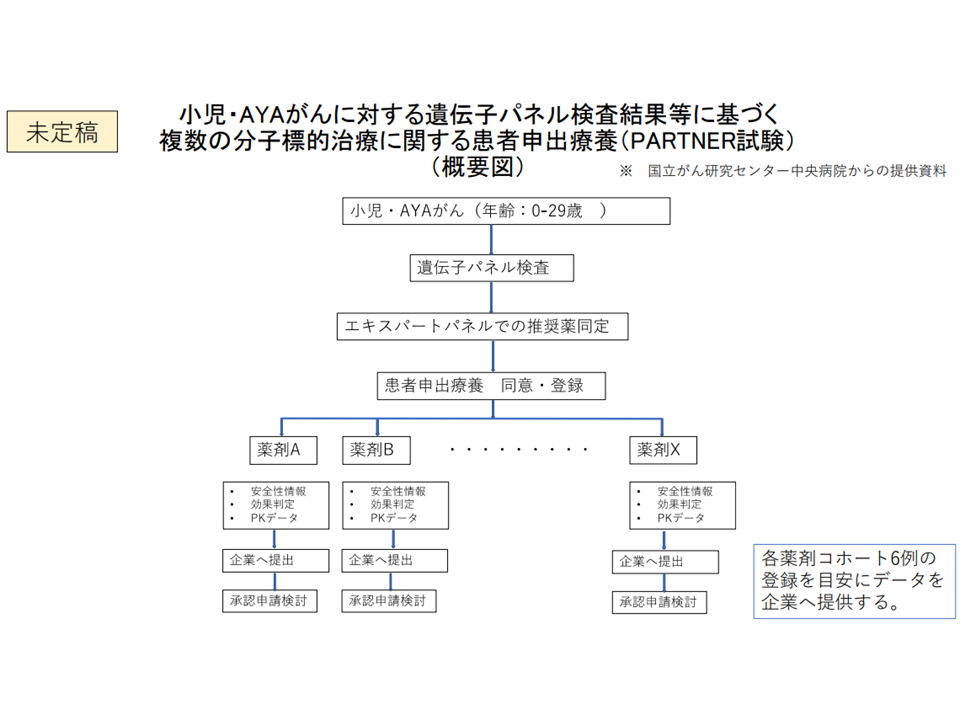
「小児がんのドラッグ・ラグに係る患者申出療養」2(検討中である点に留意)(患者申出療養評価会議2 230317)
今後、実際の国立がん研究センターからの申請を待って具体的な議論が行われますが、3月17日の会合でも、例えば患者代表の1人である天野慎介構成員(全国がん患者団体連合会理事長から「小児がん患者・家族の切なる思いに応える仕組みで、大きな期待が集まっている。しかるべき審査を経て、速やかに実現してほしい」との、小児医療の第一人者である五十嵐隆座長代理(国立成育医療研究センター理事長)から「本邦の15歳未満のがん患者は、血液がん・固形がんを含めても2000名程度、20歳未満でも同じく3500名程度と少なく、抗がん剤の開発・適応拡大が遅れている。米国では新薬開発の際に『小児適応』を合わせて検討することが義務付けられたようだが、日本ではそうした仕組みはない。国立がん研究センターが中心となり、小児への抗がん剤選択の仕組みを設けることに大きな期待が集まっている」との声が多く出されています。
ただし、「AMEDから研究費を得ており、この研究費で事務コストを賄うことが可能となる。患者申出療養で患者負担を求める際には、この点との整合性を確保・整理する必要がある」(松井健志構成員:国立がん研究センターがん対策研究所生命倫理・医事法研究部長)、「新たな仕組みは治験の第1層試験を患者申出療養の中で行うものにも見える。これは患者申出療養の本来趣旨から離れていないか、今後整理していく必要がある」(直江知樹構成員:名古屋医療センター名誉院長)との声も出ており、今後の検討課題の1つになりそうです。
もっとも、「小児への適切な抗がん剤選択を可能とする仕組み」創設に反対する意見は出ておらず、今後、前向きな検討が進むと期待されます。
「胸部悪性腫瘍へ針を刺し、凍結・融解により壊死を狙う」技術を継続審議
また同日には15番目の患者申出療養として「胸部悪性腫瘍に対する経皮的凍結融解壊死療法」の審議も行われました。
【これまでに認められている患者申出療養】(ただし「2」「3」「4」「5」「10」の技術はすでに新規患者の登録を終了)
(1)腹膜播種・進行性胃がん患者への「パクリタキセル腹腔内投与および静脈内投与ならびにS-1内服併用療法」
(2)心移植不適応な重症心不全患者への「耳介後部コネクターを用いた植込み型補助人工心臓による療法」(関連記事はこちら)
(3)難治性天疱瘡患者への「リツキシマブ静脈内投与療法」(関連記事はこちら)
(4)髄芽腫、原始神経外胚葉性腫瘍または非定型奇形腫様ラブドイド腫瘍患者への「チオテパ静脈内投与、カルボプラチン静脈内投与およびエトポシド静脈内投与ならびに自家末梢血幹細胞移植術の併用療法」(関連記事はこちら)
(5)ジェノタイプ1型C型肝炎ウイルス感染に伴う非代償性肝硬変患者への「レジパスビル・ソホスブビル経口投与療法」(関連記事はこちら)
(6)進行固形がん(線維芽細胞増殖因子受容体に変化を認め、従来治療法が無効、かつインフィグラチニブによる治療を行っているものに限る)患者への「インフィグラチニブ経口投与療法」(関連記事はこちら)
(7)早期乳がん患者への「ラジオ波熱焼灼療法」(関連記事はこちら)
(8)遺伝子パネル検査でactionableな遺伝子異常を有すると判断された固形腫瘍に対する「マルチプレックス遺伝子パネル検査による遺伝子プロファイリングに基づく分子標的治療」(関連記事はこちらとこちら)
(9)HER2陽性の手術不能または再発の乳房外パジェット病患者に対する「トラスツズマブ エムタンシン(カドサイラ点滴静注用)静脈内投与療法」(関連記事はこちら)
(10)ROS1融合遺伝子陽性の進行性小児脳腫瘍患者に対する「エヌトレクチニブ(販売名:ロズリートレクカプセル)の経口投与療法」(関連記事はこちら)
(11)免疫グロブリンGサブクラス4自己抗体陽性難治性慢性炎症性脱髄性多発神経炎患者に対する「リツキシマブ追加投与療法」(関連記事はこちら)
(12)BRAFV600変異陽性の進行性神経膠腫を有する小児を対象とした「ダブラフェニブ・トラメチニブ併用療法」(関連記事はこちら)
(13)BRAF V600変異陽性の局所進行・転移性小児固形腫瘍に対する「ダブラフェニブ・トラメチニブの第II相試験」(関連記事はこちら)
(14)「EZH2阻害薬の有効性が期待される標準治療がない、または治療抵抗性の小児・AYA悪性固形腫瘍に対するタゼメトスタット療法」(関連記事はこちら
標準治療(手術、放射線治療)の適応とならない▼最大径3.5㎝以下の肺悪性腫瘍(転移性・原発性)▼同じく10㎝以下の縦隔悪性腫瘍・胸膜悪性腫瘍・胸壁悪性腫瘍—に対し、局所麻酔下・CTガイド下に凍結針を穿刺し、凍結機器「Visual-ICE」を用いて「凍結→融解」を3サイクル施行し、壊死を狙うものです。
同機器メーカーでは、別に薬事承認を目指し準備が進められていますが、「薬事承認→保険適用」が実現するまでには一定の時間がかかります。
すでに本技術を保険外で実施している慶應義塾大学病院では「保険適用までの間にも、本技術の実施を希望する患者がおり、経済的負担を軽減するために患者申出療養として実施することを認めてほしい」と申請しています。
【対象患者】次のいずれをも満たす患者
▽胸部悪性腫瘍(原発巣あるいは転移巣の組織学的診断を得られている症例)
▼転移性肺腫瘍は、TNM分類のIV期に相当すること
▼原発性肺悪性腫瘍、縦隔・胸膜・胸壁悪性腫瘍は、初回治療以降の再発病変であること
▽標準治療の適応がない症例
▼手術への耐術能がない
▼病変の局在や放射線照射歴(2度目の放射線治療は行えない)などから放射線療法の適応がない
▼組織型から放射線療法や化学療法の効果が期待できない
▽治療標的病変数:3個以内
▽治療標的病変の最大径
▼肺悪性腫瘍:3.5cm以下
▼その他の胸部悪性腫瘍:10cm以下
▽治療標的病変以外に活動性病変がない
▽同意取得時の年齢が18歳以上79歳以下
▽ECOG performance status:0-2
▽試験治療を担当する放射線診断医、試験治療および標準治療である手術を担当する呼吸 器外科医、標準治療である放射線療法を担当する放射線治療医、標準治療である化学療法を担当する呼吸器内科医が参加する合同カンファレンスにて「適応がある」と判断すること
▽試験治療を担当する放射線診断医が技術的に施行可能と判断すること
▽患者本人から文書にて同意を得られていること
【評価項目】:主要項目は▼安全性については「Grade3以上の早期有害事象発生割合」(CTCAEver.5.0)▼有効性については「1年局所制御割合」「全生存期間」(RECISTガイドライン改訂版version 1.1)—とする
【症例数見込み】:20症例
【予定期間】:2026年9月まで
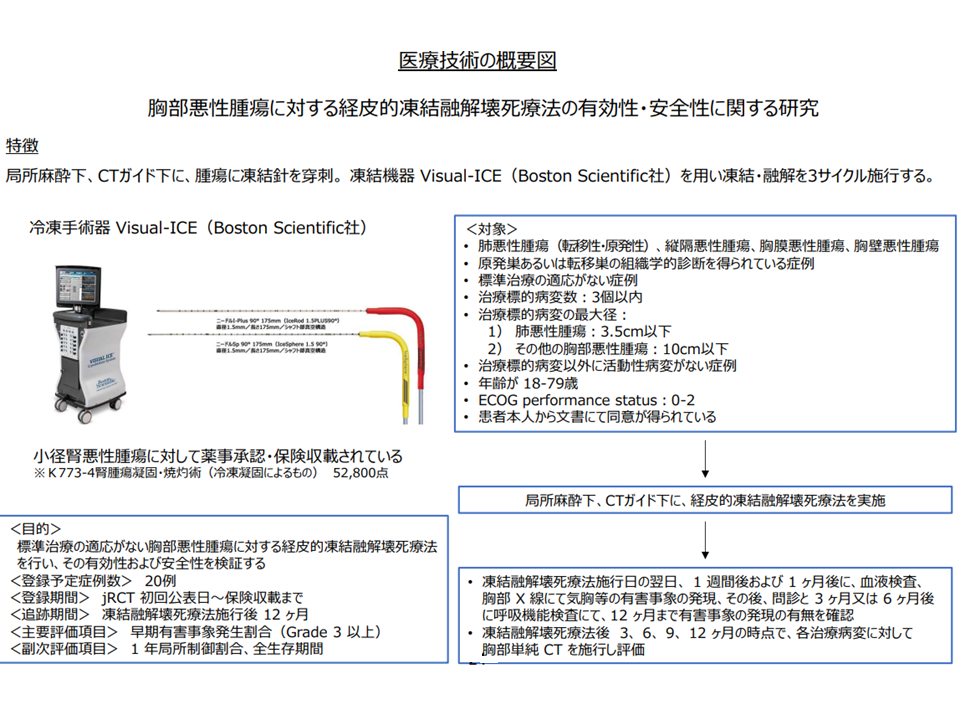
「胸部悪性腫瘍に対する経皮的凍結融解壊死療法」の概要(患者申出療養評価会議3 230317)

「胸部悪性腫瘍に対する経皮的凍結融解壊死療法」の保険適用までのロードマップ(患者申出療養評価会議4 230317)
上述のように様々な理由で標準治療を実施できない胸部悪性腫瘍患者に対し「治療法選択の幅を広げる」ものであること、海外でも一定の成果が得られている技術であることなどから、本技術の内容そのもの対し異論・反論は出ていません。
ただし、「実施計画の中に、安全性(合併症として気胸が相当程度発生しうる(胸腔ドレーン留置が必要な気胸が2割弱発生しえいる)点など)に関する記述が十分になされておらず(患者同意取得文書には十分な記載ある)、一部追加する必要がある」ことなどが問題となり、継続審議となりました。事務局(厚労省)から慶大病院に連絡し、「計画書を一部修正・変更」のうえで近く「適」と判断される見込みです。
なお、山口俊晴構成員(がん研究会有明病院名誉院長、国際医療福祉大学教授)は「術者が相当程度限定される」点を少し心配しています。本技術は、熟練した放射線科医がCTガイドを行い、熟練した外科医が、その画像を頼りに穿刺を行うものです。慶大病院では既に保険外診療での実施経験が相当程度あり、必要な手技をマスターしていますが、「経験のない他の施設への拡大」の際には、この点が高いハードルとなる可能性があります
【GHCからのお知らせ】
約200超のがん診療連携拠点病院などが参加する CQI(Cancer Quality Initiative)研究会(代表世話人:望月泉:八幡平市病院事業管理者・岩手県立病院名誉院長)では、DPCデータをもと「がん医療の質向上」に向けた研究を行っており、Gem Medを運営するグローバルヘルスコンサルティング・ジャパン(GHC)がデータ分析等を担当しています。
本年(2023年)8月26日には、第16回研究会を開催(会場+web)。研究会では、「診療の質」と「経営の質」を向上するためのデータ分析方法を議論。前立腺がんなどがん種別に内視鏡手術支援ロボットを用いた手術動向分析などをベースに議論が行われます。
参加病院には、がん診療分析ツール(Cancer Dashboard)を無償提供。また当日は「がん拠点病院の働き方改革」に関する講演も行われます。是非、ご参加ください(詳細はこちら)。
【関連記事】
14番目の患者申出療養、「EZH2阻害薬の有効性が期待される小児・AYAがん患者」へのタゼメトスタット療法を承認―患者申出療養評価会議
13番目の患者申出療養、「BRAF V600変異陽性の小児固形がん」への抗がん剤併用療法を条件付きで承認―患者申出療養評価会議
進行性胃がんへのパクリタキセル・S-1併用療法、乳房外パジェットへのカドサイラ投与など実施計画見直し―患者申出療養評価会議
8番目の患者申出療養「遺伝子変異に対応した分子標的薬治療」、ニラパリブを対象薬剤に追加―患者申出療養評価会議
耳介後部コネクター用いるDT療法の有効性に期待、遺伝子パネル検査による抗がん剤治療で対象薬剤追加―患者申出療養評価会議
患者申出療養から「初の薬事承認・保険適用」技術登場、抗がん剤「適応拡大」にも期待集まる―患者申出療養評価会議
8番目の患者申出療養「遺伝子変異に対応した分子標的薬治療」、リキッドバイオプシーも検査対象に追加―患者申出療養評価会議
12番目の患者申出療養、「BRAF V600変異陽性の小児神経膠腫」への抗がん剤併用療法を承認―患者申出療養評価会議
11番目の患者申出療養として、難病CIDPへのリツキシマブ追加投与療法を認める―患者申出療養評価会議
患者申出療養で実施される保険外の医療技術、しかるべき時期に安全性・有効性の評価が必要—患者申出療養評価会議
患者申出療養の計画変更を了承、ただし「野放図な期間延長」などは好ましくない―患者申出療養評価会議
10番目の患者申出療養として、小児脳腫瘍へのエヌトレクチニブ投与療法を認める―患者申出療養評価会議
小児がん患者も迅速に「適応外の分子標的薬」にアクセスできる環境を整備―患者申出療養評価会議(2)
乳房外パジェットへのカドサイラ投与、9番目の患者申出療養として導入―患者申出療養評価会議(1)
小児がん患者が「最適な抗がん剤にアクセスしやすい環境」の整備に向け、患者申出療養を拡充―患者申出療養評価会議
遺伝子パネル検査に基づく「適応外抗がん剤」使用、患者申出療養での実施を承認―患者申出療養評価会議
遺伝子パネル検査に基づく抗がん剤の適応外使用想定した事前準備、国がんで進む―患者申出療養評価会議
患者申出療養評価会議からメーカーに「薬剤等供給」協力を要請する仕組み設ける―患者申出療養評価会議
早期乳がんのラジオ波熱焼灼治療を患者申出療養に導入、再発リスク説明等が必要―患者申出療養評価会議
遺伝子パネル検査で「適応外の抗がん剤治療」の可能性ある場合、迅速に治療開始できる準備進める―患者申出療養評価会議
「非代償性肝硬変へのハーボニー投与」、5種類目の患者申出療養に―患者申出療養評価会議
阪大病院での患者申出療養すべてで死亡含む重篤事象が発生、適切な患者選択を―患者申出療養評価会議
有効性・安全性の確立していない患者申出療養、必要最低限の患者に実施を—患者申出療養評価会議
心移植不適応患者への植込み型人工心臓DT療法、2例目の患者申出療養に―患者申出療養評価会議
2018年度改定に向けて、入院患者に対する「医師による診察(処置、判断含む)の頻度」などを調査―中医協総会
患者申出療養、座長が審議の場を判断するが、事例が一定程度集積されるまでは本会議で審議―患者申出療養評価会議
患者申出療養評価会議が初会合、厚労省「まずは既存の先進医療や治験の活用を」
患者申出療養の詳細固まる、原則「臨床研究」として実施し、保険収載を目指す―中医協
患者申出療養の提案受けた臨床研究中核病院、「人道的見地からの治験」の有無をまず確認―中医協総会
大病院受診、紹介状なしの定額負担など16年度から-医療保険部会で改革案まとまる





