白血病等治療薬のキムリア、費用対効果評価に基づく薬価を「3264万円」に引き下げ―中医協総会(2)
2021.4.14.(水)
気管支喘息等治療薬「テリルジー」、血液がん治療薬「キムリア」について、費用対効果評価に基づき価格引き下げを行う(7月1日から適用)—。
新たな血液がん治療薬である「イエスカルタ」について、価格引き下げ後のキムリアと同額の3264万円に薬価を設定する―。
気管支喘息等治療薬の「ヌーカラ」について、医学会の要望を踏まえて「在宅自己注射の対象薬剤」に特例的に追加する―。
4月14日に開催された中央社会保険医療協議会・総会では、こういった点の承認も行われています。
目次
気管支喘息等治療薬テリルジー、血液がん治療薬キムリア、費用対効果評価に基づき価格引き下げ
安全性・有効性の確認された医療技術は「すべて保険適用する」ことが我が国の公的医療保険制度の原則です。しかし医療保険財政が厳しくなる中では、新規の医療技術を保険適用する際などに「経済面を考慮する」ことが不可欠となってきています。
そこで、中医協では2012年度から「費用対効果評価」の導入に向けた検討を進め、試行錯誤を経て2019年4月から制度化(本格運用)されました。
費用対効果評価の仕組みは非常に複雑ですが、「高額である」「医療保険財政に大きな影響を及ぼす」などの要件を満たした新薬・新医療機器について、「類似の医薬品・医療技術等に比べて、費用対効果が優れているのか、あるいは劣っているか」をデータに基づいて判断。「費用対効果が優れている」と判断されれば価格(薬価、材料価格)は据え置きとなり、「費用対効果が劣っている」と判断されれば価格の引き下げが行われます。また、「費用が少なくなる一方で、効果が優れている・あるいは同じである」という、いわば「きわめて費用対効果が優れている」製品については、価格の引き上げも行われます。従前の「安全性」「有効性」に加えて、新たに「経済性」の評価軸を設けるものです。
今般、▼気管支喘息・慢性閉塞性肺疾患(COPD)の治療等に用いる「テリルジー100エリプタ」▼白血病等治療薬の「キムリア点滴情注」—について、費用対効果評価の結果を踏まえた「新薬価」設定が中医協で行われました(関連記事はこちら)。
まず「テリルジー100エリプタ」については、さまざまな使用方法があり、「ある使用方法では費用対効果が優れているが、別の使用方法では費用対効果は優れていない」と判断され、検討の結果、次のように若干の価格引き下げが行われます。
▽テリルジー100エリプタ
▼14吸入1キット:(現行)4183.50円 → (改定後)4,160.80 円(0.54%の価格引き下げ)
▼30吸入1キット:(現行)8853.80円 → (改定後)8805.10円(0.55%の価格引き下げ)
あわせて、類似品目である「ビレーズトリエアロスフィア56吸入」「エナジア吸入用カプ セル中用量」同高用量」「テリルジー200エリプタ」についても、テリルジー100エリプタと同様の価格引き下げが行われます。
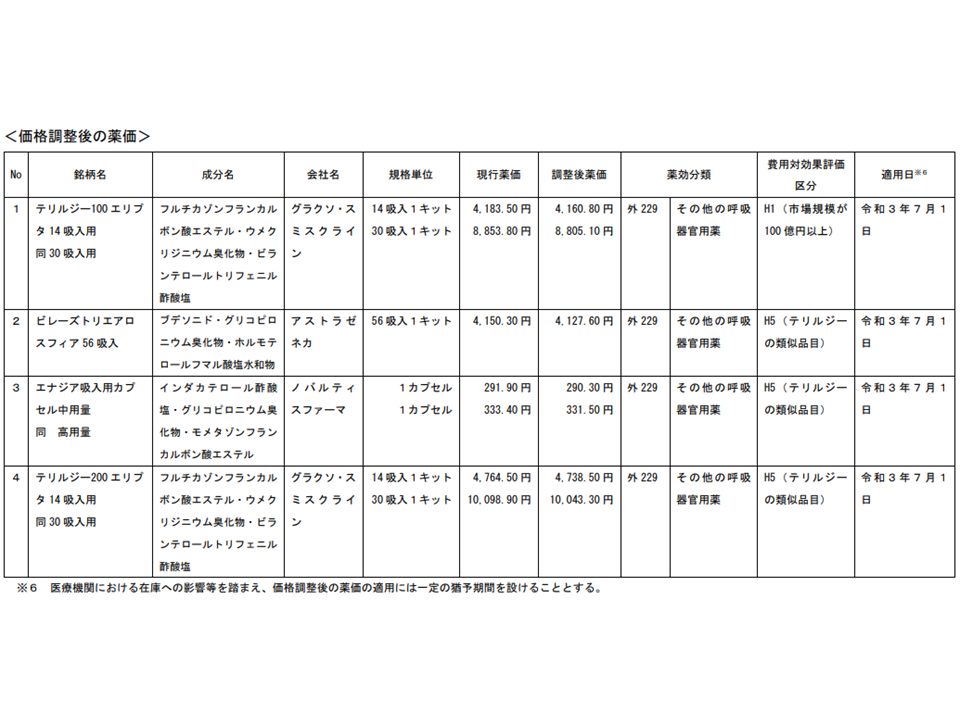
テリルジーおよび類似薬の費用対効果評価に基づく新薬価(中医協総会(2)1 210414)
なお、一部の使用方法において「従来の治療法と比べて、費用が削減され、効果が上回る」ことが確認されましたが、「価格引き上げ」の要件である「従来の治療法と比べて、改良の範囲を超えている」などといった点を満たさなかったことから、「価格引き上げ」方向での検討は行われていません。
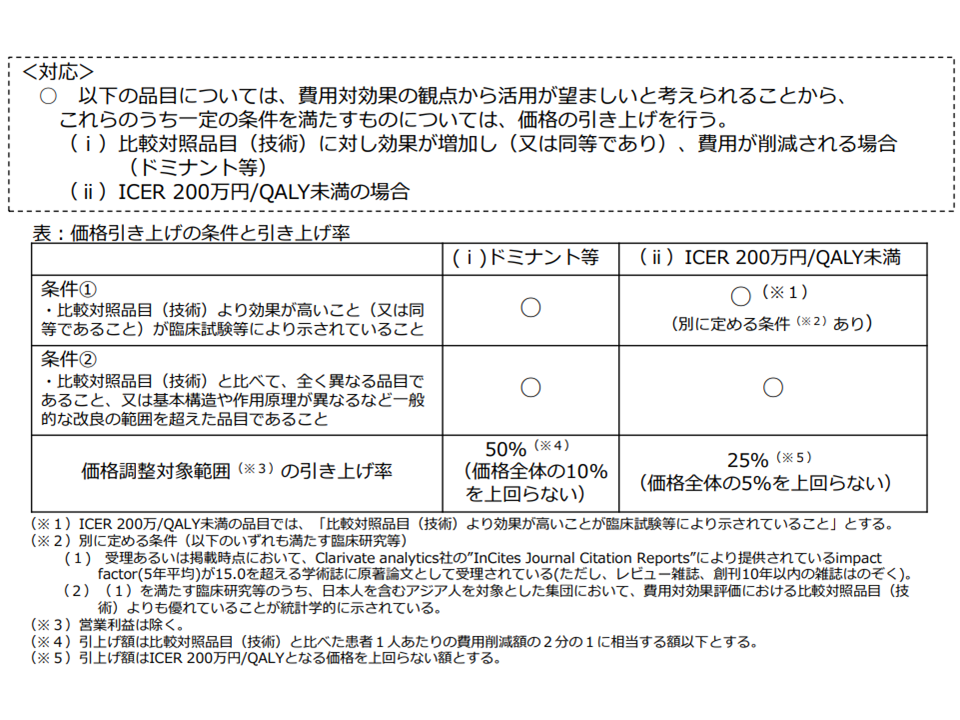
費用対効果評価の結果、価格引き上げとなるケースの要件(中医協総会(2)2 210414)
また、「キムリア点滴静注」についても、「ある使用方法では費用対効果が優れているが、別の使用方法では費用対効果は優れていない」と判断され、次のように価格引き下げが行われます。
▽キムリア点滴静注
(現行)3411万3655円 → (改定後)3264万7761円(4.3%の価格引き下げ)
これらの医薬品については、すでに医療機関等に納入されている「在庫」があります。これらは「高い旧薬価」を踏まえた価格で医療機関等が購入しているため、すぐさま「安い新薬価」を適用したのでは、医療機関等に「不測の損害」が生じてしまいます。
したがって、在庫がなくなる期間を考慮して、「安い新薬価」の適用は「2021年7月1日から」となります(6月30日まで、医療機関は「高い旧薬価」で保険償還を受けることができる)。
費用対効果評価に基づく価格設定の透明性確保に向け、どこまでのデータ公表を求めるか
ところで、「費用対効果が優れているか、劣っているか」を判断する際には、専ら「ICER」(増分費用効果)という概念を用います。ICERは、「類似技術βの費用(b)と新規医療技術αの費用(a)との差(つまりb-a)」を「類似技術βの効果(B)と新規医療技術αの効果(A)との差(つまりB-A)」で除したもので、いわば「高い効果を得るために、どれだけ余分な費用がかかるのか」と表現することができます。
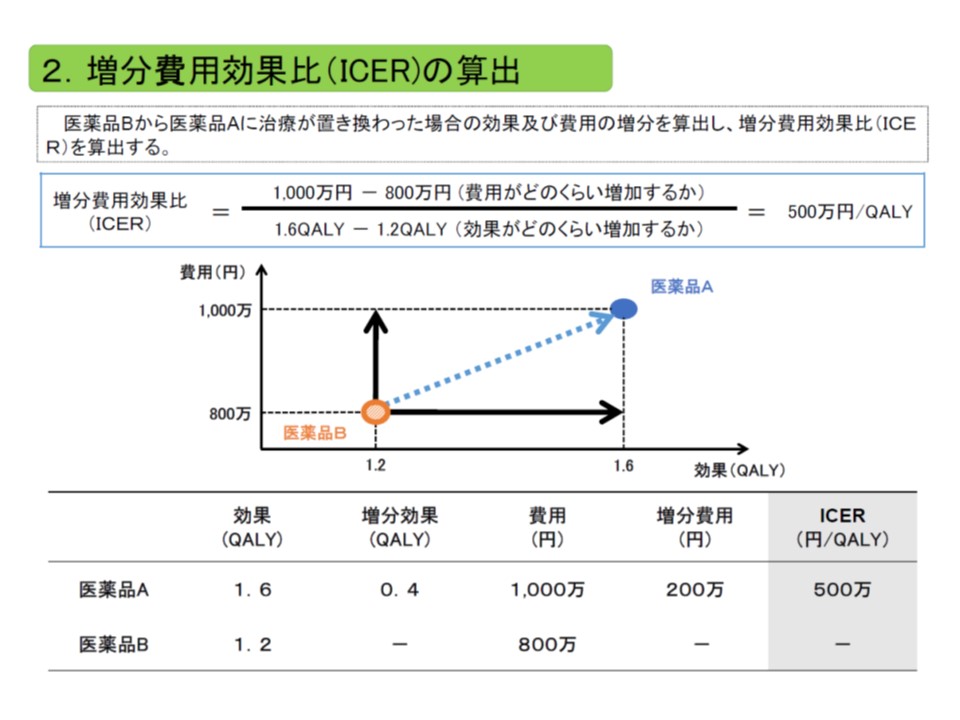
ICERは、「費用の増加分」を「効果の増加分」で除して計算する。費用には主に公的医療費が含まれ、効果のある医療技術で生存年が伸びれば、その分、医療費が増加し、費用が増加することになる点も考慮される
同じ効果を得るために大きな費用がかかる(ICERが高い)技術は、「費用対効果が劣っている」と判断され、逆に小さな費用で済む(ICERが低い)技術は「費用対効果が優れている」と判断し、その基準は次のように設定されています。
▽ICERが500万円未満の場合(総合的評価で指定難病等の適応がある場合には750万円未満に緩める):「費用対効果が優れている」と判断し、価格を維持する(試行段階と同じ)
▽ICERが500万円以上750万円未満の場合(同750万円以上1125万円未満に緩める):「費用対効果が劣っている」と判断し、有用性等加算部分については価格を30%、営業利益部分については17%引き下げる
▽ICERが750万円以上1000万円未満の場合(同1125万円以上1500万円未満に緩める):「費用対効果がさらに劣っている」と判断し、有用性等加算部分については価格を60%、営業利益部分については33%引き下げる
▽ICERが1000以上の場合(同1500万円以上に緩める):「費用対効果が非常に劣っている」と判断し、有用性等加算部分については価格を90%、営業利益部分については50%引き下げる
ところで、医薬品についてはさまざま使用方法があります。例えば「適応症が複数ある」場合には、類似技術(類似薬)が変わってくることもあり、「ICERの値が複数になる」ケースが生じえます。
また、「対象患者の年齢によって使用方法が異なる」こともあり、この場合に類似技術が変わるなどとして「ICERの値が複数になる」ケースが生じえます。
この場合、「それぞれの集団で費用対効果評価を分析し、患者割合に応じた加重平均を行ったうえで価格調整を行う」というルールが設けられています。
「テリルジー100エリプタ」では、下表のような患者割合が製薬メーカーから公開され、これに基づいた価格調整が行われたことが明らかにされました。
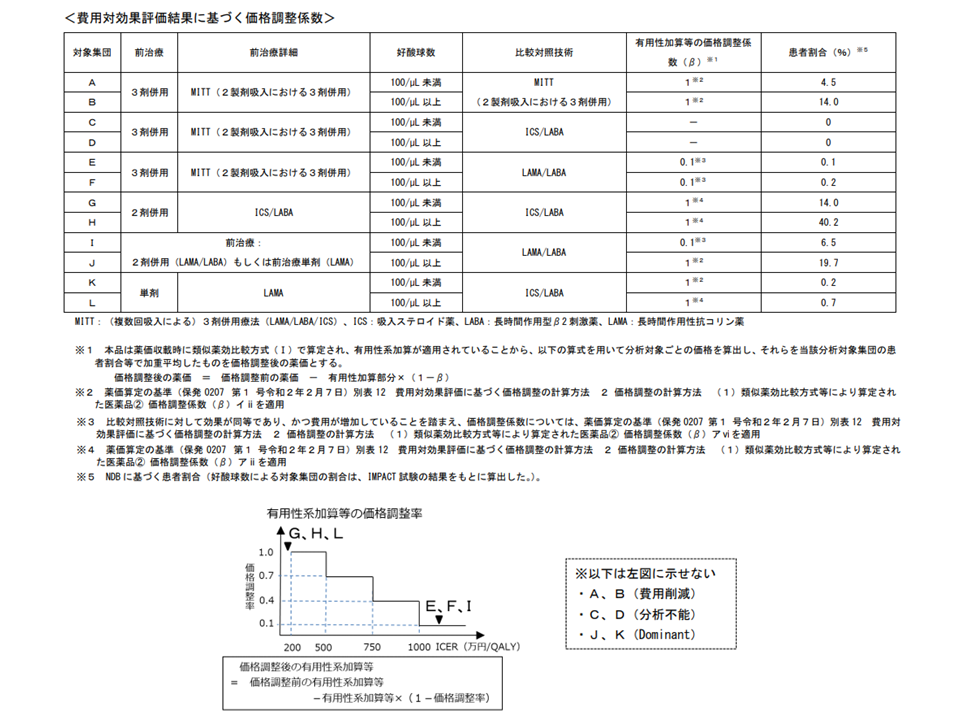
テリルジーに関する費用対効果評価(中医協総会(2)3 210414)
しかし、「キムリア点滴静注」に関しては、患者割合が「企業秘密に該当する」として公開されませんでした。このため中医協では、支払側の幸野庄司委員(健康保険組合連合会理事)から「価格設定(費用対効果評価に基づく薬価の再評価)にあたって不透明な部分があることは好ましくない。キムリア点滴情注を前例として、今後の価格調整が行われるため、今後も『企業秘密で良い』と不透明な部分が残ってしまう」との指摘がなされました。
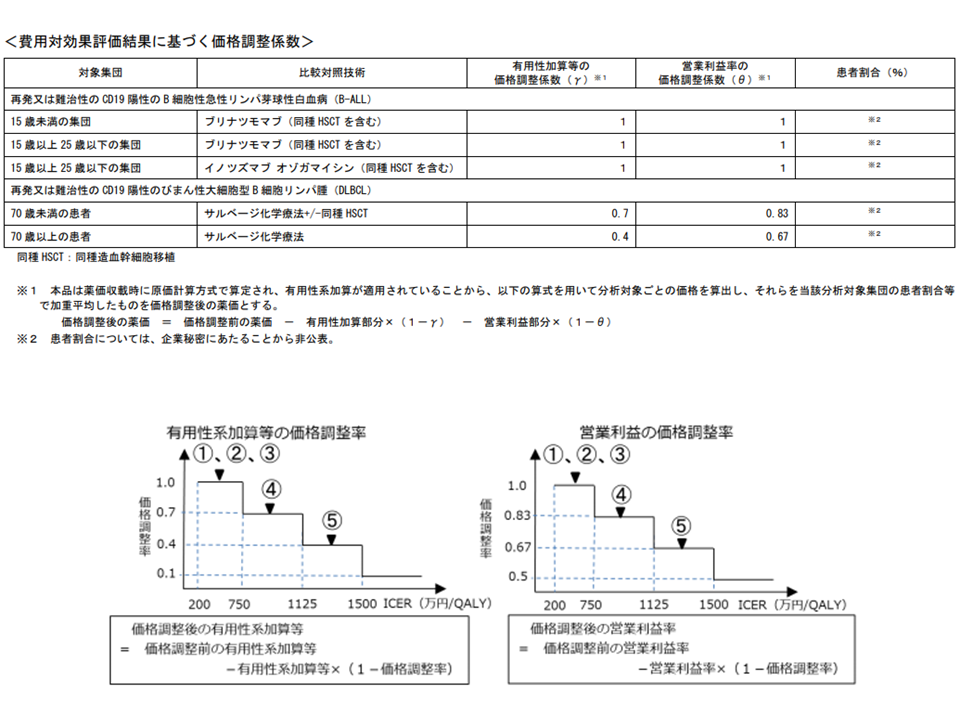
キムリアに関する費用対効果評価(中医協総会(2)4 210414)
厚生労働省保険局医療課医療技術評価推進室の岡田就将室長は「患者の需要予測ロジックが企業秘密に当たるために非公開となっている。しかし、下部組織である費用対効果評価専門組織では、製薬メーカーから示された患者割合をもとに計算している。今後、事例を重ねる中で、どこまで患者割合の公表を求めるのか検討していきたい」と理解を求めました。
費用対効果評価の仕組みは始まったばかりであり、こうした意見も踏まえて、今後、「改善」が重ねられていくことになります。
新たな血液がん治療薬「イエスカルタ」を保険適用、キムリアと同額の3264万円の薬価
4月14日の中医協総会では、血液がん(再発・難治性の▼びまん性大細胞型B細胞リンパ腫▼原発性縦隔大細胞型B細胞リンパ腫▼形質転換濾胞性リンパ腫▼高悪性度B細胞リンパ腫—)の新たな治療薬「イエスカルタ点滴静注」(成分名:アキシカブタゲン シロルユーセル)の保険適用が承認されています。
キムリア点滴静注を類似薬として薬価が設定されましたが、上述のように「キムリア点滴情注について費用対効果評価に基づく価格引き下げ」が行われたことを踏まえ、イエスカルタについても価格引き下げが行われ「1患者当たり3264万7761円」(キムリア点滴静注と同薬価)に設定されています。
本剤は4月21日に薬価基準に収載されることから、「医療機関等の在庫」は存在しません。このため、調整後の薬価が同日(4月21日)から適用されます。
なお、血液がん(再発・難治性の▼びまん性大細胞型B細胞リンパ腫▼原発性縦隔大細胞型B細胞リンパ腫▼形質転換低悪性度非ホジキンリンパ腫▼高悪性度B細胞リンパ腫—、さらに再発・難治性の濾胞性リンパ腫)の治療に用いる新たな再生医療等製品(ヒトなど細胞を加工した医薬品・医療機器等)である「ブレヤンジ静注」(成分名:リソカブタゲン マラルユーセル)について、「医薬品として保険適用を検討する」方針も固められています。上述したキムリアやイエスカルタと同様の「血液がん治療薬」であり、患者にとって治療の幅が大きく広がることが期待されます。
ただし、再生医療等製品ゆえに「極めて高額になる」と予想され、医療保険財政への影響も気にかかります。事例の積み重ねを待って、「高額となる再生医療等製品の価格設定ルール」論議が行われていきます。
発作性夜間ヘモグロビン尿症等治療薬の「ユルトミリス」、費用対効果は芳しくない
また、4月14日の中医協総会には、発作性夜間ヘモグロビン尿症・非典型溶血性尿毒症症候群の治療に用いる「ユルトミリス点滴静注」(成分名:ラブリズマブ(遺伝子組換え))についての費用対効果評価の状況報告も行われています。
同じく発作性夜間ヘモグロビン尿症等の治療に用いる「ソリリス点滴静注」と比べたところ、「効果に優越性はなく、費用が高くなる」(つまり費用対効果が劣っている)と判断されています。上記の基準に照らせば「ICERが1500万円を超過している」もので、「費用対効果が非常に劣っている」ことになり、▼有用性等加算部分については価格を90%▼営業利益部分については50%—引き下げるルールが適用される見通しです。具体的な価格は今後、中医協で議論され、決定されます。
なお、本剤については薬価専門組織で「ソリリスに比べて投与間隔が広がり、患者のQOL向上に資する」として有用性加算が付されました(つまり価格の引き上げ)。しかし、費用対効果評価専門組織では「投与間隔の延長で患者のQOLが向上する可能性があるものの、企業提出のデータからは、その点(QOL向上)の定量的評価はできない」と判断されています。支払側の幸野委員と公益代表の中村洋委員(慶應義塾大学大学院経営管理研究科教授)は「専門組織によって異なる見解が示された」点に注目し、今後の制度設計(薬価算定ルール、費用対効果評価ルールの改善)に活かすよう求めています。
気管支喘息等の治療に用いる「ヌーカラ」、在宅自己注射の対象薬剤に追加
【在宅自己注射指導管理料】の対象薬剤は、▼新薬については「薬価収載の時期」に合わせて▼新薬以外の医薬品について「診療報酬改定」に合わせて―追加すべきか否かが検討されます。
この点、新型コロナウイルス感染症が蔓延する中で、患者の医療機関受診控えが生じており、医学会から「適切な薬剤治療が可能となるよう、医師の指導の下で患者が自身で注射を行える薬剤を、より迅速に、かつ広く認めてほしい」との要望があがっています。基礎疾患を抱える患者であり、新型コロナウイルス感染症に罹患すれば「重症化・重篤化」の恐れがあることから、「医療機関を受診して薬剤注射を受ける」ことを避けるケースが増えているためです。治療を控えれば、当然「悪化」が懸念されることから、「在宅で自己注射できる薬剤」の範囲を広め、「感染防止」と「適切な治療機会の確保」との両立を目指すものです。
今般、日本呼吸器学会・日本アレルギー学会・日本リウマチ学会からの要望を踏まえて、気管支喘息(既存治療で喘息症状をコントロールできない難治患者に限る)・既存治療で効果不十分な好酸球性多発血管炎性肉芽腫症の治療に用いる▼ヌーカラ皮下注用100mg▼同100mgシリンジ▼同100mgペン(成分名:メポリズマブ(遺伝子組換え))について、「【在宅自己注射指導管理料】の対象に加える」ことが中医協で了承されました。4月21日(新薬収載のタイミング)で適用される見通しです。
【関連記事】
2022年度診療報酬改定論議、コロナ感染症の影響など見据え7・8月に論点整理―中医協総会(1)
2022年度診療報酬改定に向け「新規医療技術の保険適用」を検討、間もなく学会提案書受け付けスタート―中医協総会(2)
医薬品等の価格設定における「費用対効果評価」の概要固まる、2019年4月から実施―中医協総会(1)
費用対効果評価の骨子案、費用対効果評価が高い(ICER200万円未満)品目も価格引き上げ―中医協・費用対効果評価合同部会
医薬品の費用対効果評価、厳しすぎれば「日本市場の魅力」が減退―中医協・費用対効果評価合同部会
医療技術の費用対効果、500万・750万・1000万の3基準値に沿い「良し悪し」を判断へ―中医協・費用対効果評価合同部会
費用対効果評価、企業と公的機関の分析に齟齬が出ないよう、適宜「協議」を行う―中医協・費用対効果評価合同部会
医療技術の費用対効果、「連続的に評価」すべきか、「他技術より劣れば一律に評価」すべきか―中医協・費用対効果評価合同部会
費用対効果評価、「補正加算があり市場規模の大きな新薬・新規医療機器」を主な対象に―中医協・費用対効果評価合同部会
費用対効果データが複数ある場合、評価には一定の「幅」を持たせてはどうか―中医協・費用対効果評価専門部会
費用対効果評価、試行導入結果踏まえ「データ提出」や「再分析」の在り方検討―中医協・費用対効果評価合同部会(2)
費用対効果評価、「健康のためにいくら支払えるか」との調査は国では行わない―中医協・費用対効果評価合同部会(1)
費用対効果評価、オプジーボは価格引き下げ、川澄化学のステントグラフトは引き上げ―中医協・費用対効果評価合同部会
費用対効果評価、試行結果の検証踏まえ2019年度以降に制度化―中医協
使用実績を踏まえ材料機能区分を再申請(チャレンジ申請)できる仕組み新設―中医協・材料専門部会
薬価制度抜本改革案を修正、新薬創出等加算の厳格化を一部緩和―中医協薬価専門部会
新薬創出等加算の見直し、「容認できない」と製薬メーカー猛反発—中医協薬価専門部会
薬価制度抜本改革の具体案、費用対効果評価による価格引き上げも—中医協薬価専門部会
既存製品よりも費用が安く済み、効果の高い製品の価格は引き上げるべきか―費用対効果評価合同部会
医薬品などの費用対効果評価、業界は「加算のみへの反映」を切望—中医協・費用対効果評価合同部会
医薬品などの費用対効果評価、結果は加算のみに反映させるか、価格全体に及ぼすか—中医協・費用対効果評価関係
費用対効果評価、10月までに試行導入の詳細、年内に制度化の骨子を固める—中医協・費用対効果評価専門部会
費用対効果、試行導入には「支払い意思額調査」結果は用いず—中医協・費用対効果評価専門部会
費用対効果を判断するための「支払い意思額調査」、聞き方も含めて再検討—中医協・費用対効果評価専門部会
新医療技術の恩恵を受ける国民を対象に「いくらまで支払えるか」を調査—中医協・費用対効果専門部会
費用対効果評価の結果、どのタイミングで薬価などに反映させるか—中医協・費用対効果専門部会
費用対効果評価の結果、「保険償還価格の調整」に活用—中医協・費用対効果専門部会
医療技術の費用対効果評価、厚労省が仮想具体例で詳説—中医協・費用対効果評価専門部会
医療技術の費用対効果評価、「感染症対策への有用性」など6要素も勘案—中医協・費用対効果評価専門部会
医療技術の費用対効果、評価のための基準値を設定する方針に転換―中医協・費用対効果評価専門部会
費用対効果評価、新規収載の医薬品なども対象に2018年度から本格導入へ―費用対効果評価専門部会
2018年度の費用対効果評価に基づく再算定、オプジーボやハーボニーなど12品目に決定―中医協総会
2016年4月以降、費用対効果評価の対象として補正加算が高いものなど8品目程度を選定―中医協総会
費用対効果の良し悪しを判断する基準値、2016年度改定では定めず―費用対効果評価専門部会
費用対効果評価、対象は「保険収載後、1-2回の改定を経たもの」に―費用対効果評価専門部会
費用対効果評価、試行段階では社会的影響を評価する特別ルールは定めず―費用対効果評価専門部会
費用対効果評価の結果は医薬品・医療機器の再算定に活用―費用対効果評価専門部会
費用対効果評価はQALYを基本に実施、他の指標の使用も認める―中医協・専門部会
薬などの費用対効果、まず既収載品の再算定に活用、価格への反映は18年度改定時か―中医協・専門部会
超高額薬剤等の保険収載、薬価制度だけでなく税制等も含め幅広い対応を―社保審・医療保険部会
2019年10月の消費税率引き上げ、薬価等の見直しは同時に行うべきか―中医協総会





