オプジーボ、費用対効果評価の制度化骨子など踏まえ、2019年5月に改めて価格調整―中医協総会(3)
2019.3.29.(金)
オプジーボについて、費用・効果等に関するデータ範囲などを企業・公的分析班で協議して設定するとともに、費用対効果評価の制度化骨子に踏まえた評価を行うと、2018年度の試行時点での価格調整(引き下げ)とは異なる結果が得られた。これを踏まえて2019年5月に、オプジーボについて改めての価格調整を行う―。
3月27日に開催された中央社会保険医療協議の「総会」および、「費用対効果評価専門部会」「薬価専門部会」「保険医療材料専門部会」の合同部会(以下、合同部会)で、こういった点が了承されました(関連記事はこちらとこちら)。
ただし、医療機関等の在庫を考慮し、新価格適用までには2か月間程度の猶予期間が設けられる見込みです。

3月27日に開催された、「第19回 中央社会保険医療協議会 費用対効果評価専門部会・薬価専門部会・保険医療材料専門部会 合同部会」

3月27日に開催された、「第411回 中央社会保険医療協議会 総会」
2018年度の費用対効果評価の試行、企業と分析班の分析結果が異なった7品目を検証
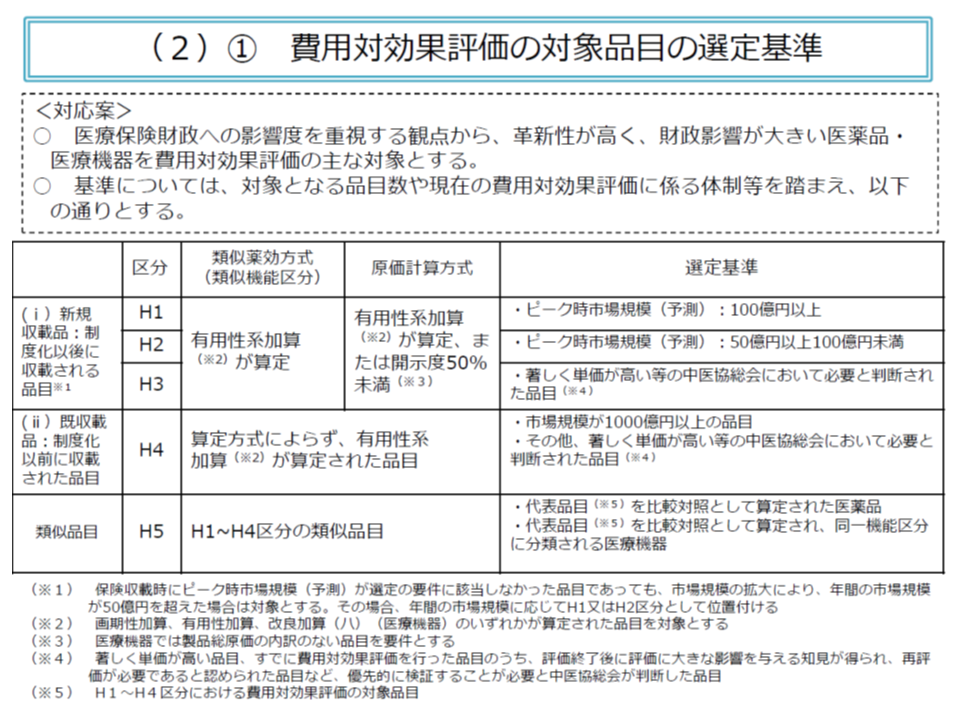
医薬品・医療機器をはじめとする医療技術の値決めにあたり、費用対効果評価結果を活用する仕組みが導入されます。「安全性」「有効性」というこれまでの評価軸に、新たに「費用対効果評価」という評価軸を加え、価格設定を行う仕組みです。
高額な医薬品・医療機器や、市場規模が非常に大きい医薬品・医療機器を主な対象として、「類似の医薬品・医療機器と比べて費用対効果が優れているのか、劣っているのか」を分析。費用対効果が劣っている場合には価格の引き下げを行い、優れている場合には価格の引き上げを行うものです(関連記事はこちらとこちら)。
これまでに、既収載品13品目等を対象に費用対効果評価を試行導入するとともに、先般、制度化(本格導入)に向けた骨子が取りまとめられました。
前者の「試行」については、一部品目(7品目)に関して、「企業側の分析」と「専門家で構成される分析班による再分析」とで分析結果が異なることが判明。2018年度の薬価・材料価格改定では「暫定的な値決め(再算定)」を実施するにとどめ、併せて結果の検証(再検証)を行うことになっていました(関連記事はこちら)。
「費用」や「効果」をどう捉え、どう分析するかについては、試行段階でもガイドラインが定められていましたが、企業側と分析班側とでデータの取り方などに違いがあったことが齟齬の原因です。例えば、「オプジーボ」(ニボルマブ製剤)については、企業側が投与期間を「最大24か月」と設定して分析を行ったのに対し、公的分析チーム(再分析チーム)では一律の投与期間上限を設けずに分析を行ったため、結果に齟齬が出てしまいました。制度化に向けては、こうした齟齬が出ないように、事前に企業側と分析班側とで協議(事前協議)を十分に行うことになっています。
今般、暫定的に価格設定が行われた試行7品目について結果検証(再検証)が終了し、その内容が3月27日の中医協に報告されました。検証結果に基づき、オプジーボのみについて「改めての価格見直しが必要」と結論付けられています。
検証対象となったのは、次の7品目です。
【医薬品】
▼ハーボニー(C型慢性肝炎治療薬)▼ヴィキラックス(C型慢性肝炎治療薬)▼ダクルインザ(C型慢性肝炎治療薬)▼スンベプラ(C型慢性肝炎治療薬)▼オプジーボ(肺がん等治療薬)
【医療機器】
▼サピエンXT(経カテーテルウシ心のう膜弁)▼カワスミ Najuta 胸部ステントグラフトシステム(大動脈用ステントグラフト)
オプジーボについては、企業側・分析側で取扱いデータを協議した上で、費用対効果を判断するための指標である「ICER」(いわば「高い効果を得るために、どれだけ余分な費用がかかるのか」を見る指標。数値が小さいほど費用対効果が良いと判断される)を計算。
その結果を、制度化骨子で定められた判断基準に当てはめると、「試行時点」とは異なる薬価引き下げ幅が算出され、改めて薬価見直しを行うことが中医協で了承されました。
【ICERの値の判断基準】
▽ICERが500万円未満の場合(総合的評価で指定難病等の適応がある場合には750万円未満に緩める):「費用対効果が優れている」と判断し、価格を維持する(試行段階と同じ)
▽ICERが500万円以上750万円未満の場合(同750万円以上1125万円未満に緩める):「費用対効果が劣っている」と判断し、有用性等加算部分については価格を30%、営業利益部分については17%引き下げる
▽ICERが750万円以上1000万円未満の場合(同1125万円以上1500万円未満に緩める):「費用対効果がさらに劣っている」と判断し、有用性等加算部分については価格を60%、営業利益部分については33%引き下げる
▽ICERが1000万円以上の場合(同1500万円以上に緩める):「費用対効果が非常に劣っている」と判断し、有用性等加算部分については価格を90%、営業利益部分については50%引き下げる
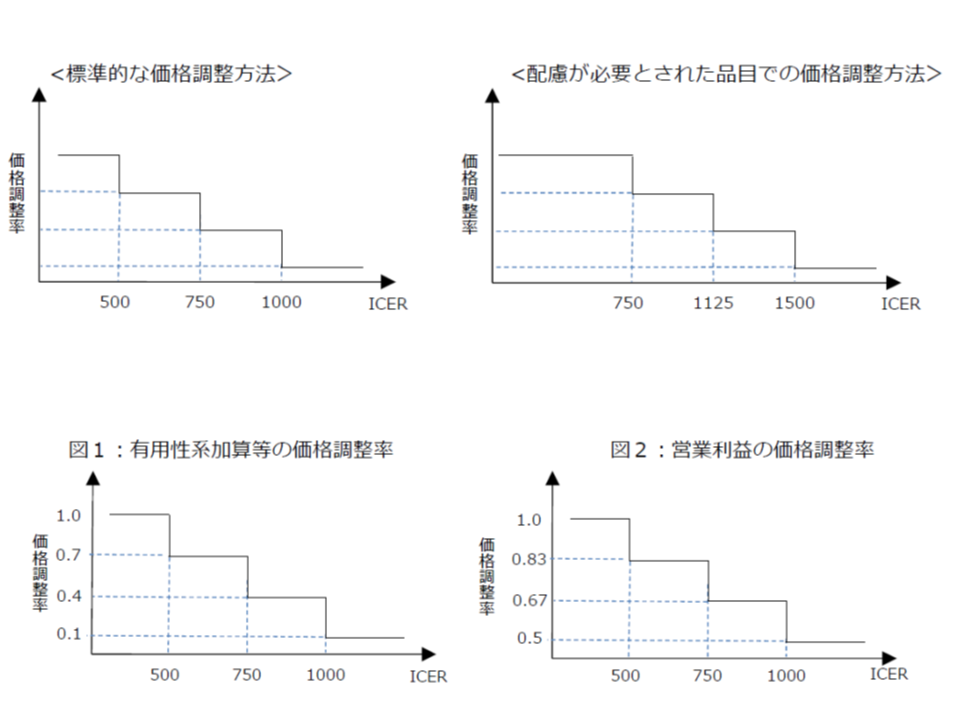
費用と効果の統一指標となる「ICER」を品目ごとに計算し、その数値が「500万円」未満であれば費用対効果は良く価格は維持する、500万円以上であれば、費用対効果は悪く価格を引き下げる

薬価・材料価格のうち、「有用性加算等の部分」や「営業利益率」などが費用対効果評価に基づく価格調整の対象となる
厚労省では、今年5月(2019年5月)の新薬収載のタイミングで、オプジーボについて改めての価格設定(新価格)を行います。ただし、医療機関等の在庫にも配慮し、新価格を適用するまでに2か月程度の猶予期間が設けられる見込みです。なお、新価格が、現在の薬価よりも低くなるのか否かについて、厚労省は明らかにしていません(2019年5月の告示を待つ必要がある)。
また、▼ダクルインザ▼スンベプラ―の2品目については、いずれもICERが500万円未満となり、上記基準に照らして「価格調整しない」こととなりました。
一方、▼ハーボニー▼ヴィキラックス―の2品目は、制度化骨子における「H5(類似品目)」に該当します。制度化骨子ではH5の品目について「費用対効果評価の分析は行わず、比較対照薬(代表品目)に準じた価格調整を行う」としています。両医薬品の比較対象薬である▼ダクルインザ▼スンベプラ―などについて上記のとおり「価格調整しない」と判断されており、制度化骨子の規定(比較対象薬に準ずる)に基づいて「価格調整しない」こととされました。
また、サピエンXTについてはICERが500万円未満となったことから、上記基準に照らして「価格調整しない」こととなりました。
さらに、カワスミ Najuta 胸部ステントグラフトシステムについては、「効果が同等で、かつ費用削減」(ICERは算出できない)となり、制度化骨子に沿っても、2018年4月の「価格引き上げ」と同じ結果が得られるため、「今回は新たな価格調整は行わない」こととされました。
 190327の図表.png)
中医協では、厚労省保険局医療課の古元重和企画官から示された、制度化骨子の内容を踏まえた通知案も了承しています(近く発出)。そこでは、▼過去に費用対効果評価の対象になった品目は、新たに「価格評価に大きな影響を与える」事項が判明した場合を除き、費用対効果の対象としない▼企業側は中医協決定までの間、分析データを公表せず、中医協決定内容なども公表しない―ことなどが明確化されています。
なお、医薬品・医療機器とは別に「高額な医療機器を用いる医療技術」についても、厚労省は費用対効果評価の手法を研究しています。
しかし、医療技術そのものについては、▼診療報酬の中に、医療機器の費用に加えて、医師の技術なども含めた評価が行われており、機器の費用が点数に占める割合はさまざまである▼新たな医療技術の保険収載に当たっては、有効性・安全性だけでなく、「普及性」「技術的成熟度」「施設基準の必要性」なども勘案して総合的な評価が行われている―などといった特性があることから、「医薬品や医療機器と同様の『一律の価格調整』方法設定は非常に難しい」ことが、3月27日の中医協総会と費用対効果評価専門部会で確認されました。
このため、「高額な医療機器を用いる医療技術」の費用対効果評価については、今後も手法を継続して検討していくことになりました。また医療技術については、先進医療会議や医療技術評価分科会(中医協の下部組織、学会等からの要望を踏まえて新医療技術の保険収載の是非を検討する)においても評価に向けた検討を行っており、これら会議体とも歩調を合わせて検討していくことになるでしょう。

3月27日に開催された、「第52回 中央社会保険医療協議会 費用対効果評価専門部会」
【関連記事】
先行バイオ医薬品とまったく同一の「バイオセイム」登場、薬価の在り方など検討―中医協総会(2)
2020年度診療報酬改定に向け、「医師働き方改革」等のテーマ別や患者の年代別に課題を議論―中医協総会
医薬品等の価格設定における「費用対効果評価」の概要固まる、2019年4月から実施―中医協総会(1)
費用対効果評価の骨子案、費用対効果評価が高い(ICER200万円未満)品目も価格引き上げ―中医協・費用対効果評価合同部会
医薬品の費用対効果評価、厳しすぎれば「日本市場の魅力」が減退―中医協・費用対効果評価合同部会
医療技術の費用対効果、500万・750万・1000万の3基準値に沿い「良し悪し」を判断へ―中医協・費用対効果評価合同部会
費用対効果評価、企業と公的機関の分析に齟齬が出ないよう、適宜「協議」を行う―中医協・費用対効果評価合同部会
医療技術の費用対効果、「連続的に評価」すべきか、「他技術より劣れば一律に評価」すべきか―中医協・費用対効果評価合同部会
費用対効果評価、「補正加算があり市場規模の大きな新薬・新規医療機器」を主な対象に―中医協・費用対効果評価合同部会
費用対効果データが複数ある場合、評価には一定の「幅」を持たせてはどうか―中医協・費用対効果評価専門部会
費用対効果評価、試行導入結果踏まえ「データ提出」や「再分析」の在り方検討―中医協・費用対効果評価合同部会(2)
費用対効果評価、「健康のためにいくら支払えるか」との調査は国では行わない―中医協・費用対効果評価合同部会(1)
費用対効果評価、オプジーボは価格引き下げ、川澄化学のステントグラフトは引き上げ―中医協・費用対効果評価合同部会
費用対効果評価、試行結果の検証踏まえ2019年度以降に制度化―中医協
使用実績を踏まえ材料機能区分を再申請(チャレンジ申請)できる仕組み新設―中医協・材料専門部会
薬価制度抜本改革案を修正、新薬創出等加算の厳格化を一部緩和―中医協薬価専門部会
新薬創出等加算の見直し、「容認できない」と製薬メーカー猛反発—中医協薬価専門部会
薬価制度抜本改革の具体案、費用対効果評価による価格引き上げも—中医協薬価専門部会
既存製品よりも費用が安く済み、効果の高い製品の価格は引き上げるべきか―費用対効果評価合同部会
医薬品などの費用対効果評価、業界は「加算のみへの反映」を切望—中医協・費用対効果評価合同部会
医薬品などの費用対効果評価、結果は加算のみに反映させるか、価格全体に及ぼすか—中医協・費用対効果評価関係
費用対効果評価、10月までに試行導入の詳細、年内に制度化の骨子を固める—中医協・費用対効果評価専門部会
費用対効果、試行導入には「支払い意思額調査」結果は用いず—中医協・費用対効果評価専門部会
費用対効果を判断するための「支払い意思額調査」、聞き方も含めて再検討—中医協・費用対効果評価専門部会
新医療技術の恩恵を受ける国民を対象に「いくらまで支払えるか」を調査—中医協・費用対効果専門部会
費用対効果評価の結果、どのタイミングで薬価などに反映させるか—中医協・費用対効果専門部会
費用対効果評価の結果、「保険償還価格の調整」に活用—中医協・費用対効果専門部会
医療技術の費用対効果評価、厚労省が仮想具体例で詳説—中医協・費用対効果評価専門部会
医療技術の費用対効果評価、「感染症対策への有用性」など6要素も勘案—中医協・費用対効果評価専門部会
医療技術の費用対効果、評価のための基準値を設定する方針に転換―中医協・費用対効果評価専門部会
費用対効果評価、新規収載の医薬品なども対象に2018年度から本格導入へ―費用対効果評価専門部会
2018年度の費用対効果評価に基づく再算定、オプジーボやハーボニーなど12品目に決定―中医協総会
2016年4月以降、費用対効果評価の対象として補正加算が高いものなど8品目程度を選定―中医協総会
費用対効果の良し悪しを判断する基準値、2016年度改定では定めず―費用対効果評価専門部会
費用対効果評価、対象は「保険収載後、1-2回の改定を経たもの」に―費用対効果評価専門部会
費用対効果評価、試行段階では社会的影響を評価する特別ルールは定めず―費用対効果評価専門部会
費用対効果評価の結果は医薬品・医療機器の再算定に活用―費用対効果評価専門部会
費用対効果評価はQALYを基本に実施、他の指標の使用も認める―中医協・専門部会
薬などの費用対効果、まず既収載品の再算定に活用、価格への反映は18年度改定時か―中医協・専門部会
超高額薬剤等の保険収載、薬価制度だけでなく税制等も含め幅広い対応を―社保審・医療保険部会





